На Рис.1 показана диаграмма энергетических уровней атома водорода.
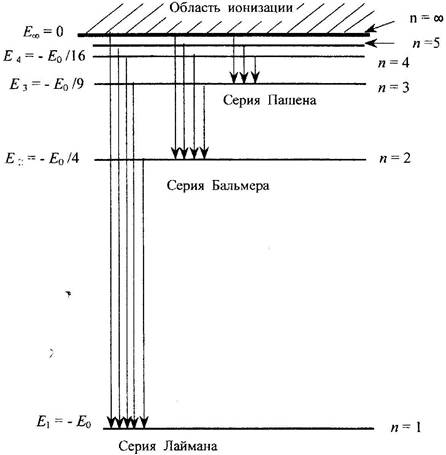
Рис.1 Диаграмма энергетических уровней атома водорода.
Частоты всех спектральных линий в спектре атома водорода, возникающие при переходе с верхнего уровня Ek на уровень En, описываются формулой Бальмера:
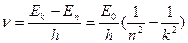 , (1)
, (1)
где E0=2,176 × 10-18 Дж = 13,6 эВ, n=1, 2, 3…..; k=n+ 1, n+ 2,. n+ 3..
Спектральные линии, соответствующие переходам с любых верхних энергетических уровней Ek на один и тот же нижний уровень Еn (k>n), образуют спектральную серию в излучении.
Серия Лаймана наблюдается в ультрафиолетовом диапазоне спектра, содержит спектральные линии, соответствующие переходам на основной уровень (n= 1).
Частоты линий получают из формулы (1) при n= 1 и k=2,3,4…:
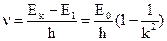 ,
,
где k=2,3,4…
Серия Бальмера наблюдается в ближнем УФ и видимом диапазоне и соответствует переходам на второй уровень Е2 (n=2) со всех верхних уровней (k=3,4,5,…).
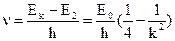 ,
,
где k= 3,4,5,6…
Серия Пашена наблюдается в ИК диапазоне длин волн и соответствует переходам на третий уровень Е3 (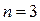 ) со всех верхних уровней (k=4,5,6,…).
) со всех верхних уровней (k=4,5,6,…).
Частоты определяются формулой:
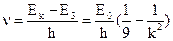 ,
,
где k= 4,5,6,7…
Указанные серии представлены на рис. 1. Эти серии характерны и для спектров поглощения атома водорода, где им соответствуют переходы с одного нижнего уровня на все верхние уровни.
 2015-06-28
2015-06-28 1790
1790






