| 1 вариант | 2 вариант | 3 вариант | ||||||||||||||||
| Задание №1. Получение газов и изучение их свойств. 1. Зарисуйте прибор и подпишите все используемые реактивы для получения: | ||||||||||||||||||
| водорода | кислорода | углекислого газа | ||||||||||||||||
| 2. Как распознать полученный газ? Напишите уравнения реакции. 3. Напишите уравнения реакций, характеризующие свойства данного газа. 4. Сделайте вывод о свойствах получаемого газа.
| ||||||||||||||||||
| Задание №2. Задачи по теме «Гидролиз. Реакции ионного обмена». 1. Определить, будут ли протекать реакции между веществами. Ответ подтвердить уравнениями реакций в молекулярном и ионном виде. | ||||||||||||||||||
| Карбонат натрия+серная кислота; Гидроксид натрия+сульфат цинка. | Хлорид бария+сульфат железа (II); Карбонат калия+соляная кислота. | Хлорид натрия+нитраь серебра; Сульфат меди+гидроксид калия. | ||||||||||||||||
| 2. Какую среду будут иметь растворы солей. Как измениться окраска синего лакмуса и метилоранжа в данных растворах? Ответ подтвердить уравнениями реакций в молекулярном и ионном виде. Таблица для записи ответа:
| ||||||||||||||||||
| Сульфат цинка Нитрат калия Карбонат натрия | Сульфат натрия Хлорид железа (III) Сульфит калия | Нитрат натрия Фосфат калия Хлорид алюминия | ||||||||||||||||
| Задание №3.Решение практических задач по неорганической химии. 1. Докажите качественный состав следующих соединений. Запишите реакции в молекулярном и ионном виде. | ||||||||||||||||||
| Сульфат алюминия Сульфид натрия Сульфит калия | Карбонат калия Сульфат железа(III) Хлорид аммония | Сульфат аммония Хлорид алюминия Нитрат калия | ||||||||||||||||
| 2. Напишите не менее 3-х уравнений реакций, с помощью которых можно получить: | ||||||||||||||||||
| Сульфат железа(III) | Хлорид алюминия | Карбонат калия | ||||||||||||||||
| Задание №4. Решение практических задач по органической химии. 1. С помощью каких реакций можно распознать следующие вещества? Напишите уравнения реакций. | ||||||||||||||||||
| Этанол Уксусная кислота | Фенол Формальдегид | Этилен Этаналь | ||||||||||||||||
| 2. С помощью какого одного реактива распознать водные растворы (описать происходящие изменения): | ||||||||||||||||||
| Мыла Белка Соды | Глицерина Формальдегида Белка | Этаналя Этиленгликоля Уксусной кислоты | ||||||||||||||||
| 1 вариант | 2 вариант | 3 вариант |
| Задание №5. «Скорость химической реакции, химическое равновесие». 1.Как изменится скорость гомогенной химической реакции 2А + В = С, если: | ||
| Концентрацию вещества А увеличили в 2 раза, концентрация вещества В осталась прежней. | Концентрацию вещества А увеличили в 3 раза, концен-трацию вещества В уменьшили в 6 раз | Концентрацию вещества А увели-чили в 2 раза, концентрацию вещества В уменьшили в 4 раза |
|
2.Как изменится скорость химической реакции: | ||
| при понижении температуры от 40˚ до 20˚ С, если температурный коэффициент равен 4? | при повышении температуры от 40˚ до 80˚ С, если температурный коэффициент равен 2? | при понижении температуры от 50˚ до 20˚ С, если температурный коэффициент равен 3? |
| 3.На основании принципа Ле-Шателье определите, куда сместится равновесие при одновременном понижении температуры и давления в системах: | ||
| С(т) + O2(г) D СO2(г) + Q Н2(г) + I2(т) D 2 HI(г) - Q | 6 HF(г) + N2(г) D 2 NF3(г) + 3 H2(г) - Q 2 O3(г) D 3 O2(г) + Q | 2 CO(г) D 2 C(т) + O2(г) - Q I2(т) + 5 CO2(г) D I2O5(т) + 5 CO - Q |
| Задание №6. «Генетическая связь между классами неорганических и органических веществ».
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
| ||
1.CaC2 → этин → этаналь 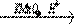 X1 X1 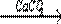 X2 X2 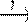 X3
2.Mg → MgO → MgCl2 → Mg(OH)2 →
MgO → Mg X3
2.Mg → MgO → MgCl2 → Mg(OH)2 →
MgO → Mg
| 1.Al4C3 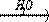 X1 X1  X2 X2  этаналь этаналь 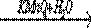 X3 X3  X1
2.Zn → ZnO → ZnCl2→Zn(OH)2 →
ZnO → Zn X1
2.Zn → ZnO → ZnCl2→Zn(OH)2 →
ZnO → Zn
| 1.ацетат калия → этан → X → этанол → диэтиловый эфир 2.C → CO2 → CaCO3 → CO2 → CaCO3→Ca(NO3)2 |
 2020-05-21
2020-05-21 138
138






