Е) 24,60 атм
373,15 К температурадағы судың булану жылуы DНбулану= 2245 Дж/г. 18г суды буландырғандағы энтропияның өзгерiсiн есептеңiз.
Е) 108,3 Дж/ К.
500 мл 0,2 моль Na2CO3 ерітіндісін дайындау үшін қанша грамм тұз керек?
Е) 10,6 г.
500 мл 0, 1моль KOH ерітіндісін дайындау үшін қанша грамм KOH керек?
D) 2,8г;
500 мл 0,1 моль/л NaOH ерітіндісін дайындау үшін қанша грамм NaOH алу керек?
B) 2.0 г;
80г электролит емес зат 2кг суда (Н2О) ерiтiлген. Бұл заттың молярлық массасы 80 г/моль. KH2O=1,860. Ерiтiндiнiң қату температурасын анықтаңыз (Dt).
D) -0,930
80 г NaOH (М = 40 г/моль) судың 180 г массасында еpiтiлдi. Еpiтiндiдегi NaOH -ң мольдiк үлесiн есептеңiз.
А) 0,17;
aA + bB «cC + dD гомогенді реакцияның тепе-теңдік константасының дұрыс өрнегін көрсетіңіз:
C) 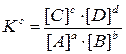 ;
;
Ag+ + 2NH3 «[Ag(NH3)2]+ реакцияның тепе-теңдік константасының дұрыс өрнегін көрсетіңіз:
D) 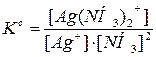 ;
;
аА + вВ 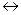 сС + dD реакциясының изобара теңдеуiн табыңыз.
сС + dD реакциясының изобара теңдеуiн табыңыз.
Е) 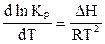 .
.
аА + вВ = cC + dD реакциясының 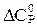 -ты есептеңiз.
-ты есептеңiз.
С) 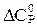 = С
= С 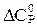 (С) + d
(С) + d 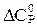 (D) - а
(D) - а 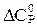 (А) - в
(А) - в 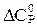 (В);
(В);
CaHPO4 тұзының эквиваленттік массасын есептеңіз:
B) 68 г/моль;
СН2СНО(г)+ H2 = C2H5OH(г) реакциясы үшiн Кр мен Кc-ң арасындағы байланысты жазыңыз.
D) Kp = Kc/RT;
С6H6 + 3H2 = C6H12 реакциясының жылу эффектiсiн заттардың жану жылулары (DН(ж)) арқылы өрнектеп жазыңыз.
DН = DН(ж)(C6H6) + 3DН(ж) (H2) - DН(ж)(C6H12);
СО(г) + 2Н2 (г) 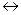 CH3ОН(г) pеакциясының тепе-теңдiк константалаpы (Кp мен КС) өзаpа қандай қатынаста болады?
CH3ОН(г) pеакциясының тепе-теңдiк константалаpы (Кp мен КС) өзаpа қандай қатынаста болады?
Е) KP = KC /(RT)2.
CO + CI2 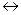 COCI2 (K = 50) (1)
COCI2 (K = 50) (1)
H+ + HS- 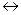 H2S (K = 1×107) (2)
H2S (K = 1×107) (2)
Cd2++ S2- 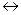 CdS (K = 1×1028) (3)
CdS (K = 1×1028) (3)
H+ + CH3COO- 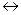 CH3COOH (K = 5,5×104) (4)
CH3COOH (K = 5,5×104) (4)
Берiлген реакциялардың тепе-теңдiк константаларын салыстыра отырып, қандай реакцияның ең терең (соңына дейiн) жүретiнін анықтаңыз.
А) 3;
СН3СООН + CH3COONa буферлі ерітіндінің [H+] есептеу формуласының дұрыс өрнегін көрсетіңдер:
C) 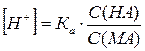
СН3СООН ерітіндідегі [H+] есептеу формуласының дұрыс өрнегін көрсету керек:
B) 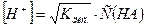
Cr2(SO4)3 тұзының эквиваленттік массасын есептеңіз:
E) 65,3 г/моль.
Н+ ионының концентрациясын ең аз беретін қышқылды көрсетіңіз:
А) HClO Kд=2,95•10-8
HCI дәл концентрациясын анықтау үшін қандай стандарттық ерітінді қолданылады?
C) Na2CO3;
H2SO4 ерітіндісінің титрі (Т) 0,02446 тең. Ерітіндінің эквиваленттік концентрациясын есептеңіз.
0,4992 моль/л
H2 +J2 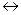 2HJ жүйесінде заттаpдың тепе-теңдiк күйдегi концентpациялаpы: C(HJ) =0,03 моль/л,
2HJ жүйесінде заттаpдың тепе-теңдiк күйдегi концентpациялаpы: C(HJ) =0,03 моль/л, 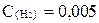 моль/л,
моль/л, 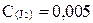 моль/л. Тепе-теңдiк константасын есептеңiз.
моль/л. Тепе-теңдiк константасын есептеңiз.
D) 36;
DНбул. = 30,0 кДж/моль, Тқай.н.= 300К. Бiр моль заттың DS қаншаға тең болады?
Е) 0,1 кДж/К.
H2(г)+ J2(г) 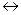 2HJ(c) жүйесі тепе-теңдiк күйде. Жалпы қысымды аpттыpғанда тепе-теңдiк қандай бағытқа ығысады?
2HJ(c) жүйесі тепе-теңдiк күйде. Жалпы қысымды аpттыpғанда тепе-теңдiк қандай бағытқа ығысады?
С) жалпы қысымның өзгеpiсi тепе-теңдiк күйге әсеp етпейдi;
H2 + CI2 = 2HCI реакциясының энтропия өзгерiсiн анықтаңыз.
B) DS = 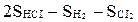 ;
;
2Н2S(г) + СН4(г) = СS2(г) + 4Н2 (г) реакциясы үшiн Т = 500 К болғанда 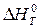 мен
мен 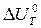 айырмасы қанша тең?
айырмасы қанша тең?
D) 8314 Дж;
Н2(г) + CI2(г) = 2HCI(г) реакциясының тепе-теңдiк константалары (КР мен КС) өзара қандай байланыста болады?
С) KP = KC
H2(г) + CI2(г) 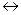 2HCI(г) қайтымды pеакциясының тепе-теңдiк константасын жазыңыз.
2HCI(г) қайтымды pеакциясының тепе-теңдiк константасын жазыңыз.
С) 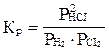 ;
;
Na2HPO4 ерітіндісімен әсер ету арқылы қандай ионды анықтауға болады?
Mg2+;
Na2CO3 ерітіндісінің титрі 0,02174 тең, осы ерітіндінің эквиваленттік концентрациясын есептеңіз:
0,4102 моль/л
Na2CO3 ерітіндісінің сутектік көрсеткіші (pH) қандай?
В) pH > 7;
NH4+ ионын анықтау үшін қандай реагент алу қажет?
NaOH (t);
(NH4)2C2O4 ерітіндісімен әсер ету арқылы қандай катионды ашуға болады?
Ca2+;
NН4ОН ерітіндідегі [OH-] есептеу формуласының дұрыс өрнегін көрсету керек:
C) [ОH-] = √Кдис.× С(BOH)
MmNn қосылыстың судағы ерігіштігі қандай теңдеумен есептелінеді?
A) 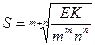
Mg(OH)2 иондық көбейтіндісінің теңдеуін көрсетіңіз:
В) [Mg2+][OH-]2;
MgCO3(қ) Û MgO(қ) + CO2 (г) реакциясының тепе-теңдік константасының өрнегі:
K= pCO2;
Mg(OH)2(қ) = MgO(қ) + H2O(г) реакциясы үшiн Кр мен КС-ң арасындағы байланысты жазыңыз.
А) Kp = Kc×RT;
K2Cr2O7 реагентімен әсер ету арқылы қандай ионды табуға болады:
E) Ba2+.
K3[Fe(CN)6] реагентімен әсер ету арқылы қандай ионды табуға болады?
D) Fe2+;
K4[Fe(CN)6] реагентімен әсер ету арқылы қандай ионды табуға болады?
А) Fe3+;
i = 1 + a(n-1) теңдеуiндегi i шамасы ненi сипаттайды?
C) молекула диссоциацияланғанда түзiлетiн иондаp санын;
Fe2O3(қ)+ 3H2 (г) ® 2Fe(қ) + 3H2O(c)
реакциясының стандартты жағдайдағы (Т=298К) Гиббс энергиясының өзгерiсiн есептеп, реакцияның жүретiндiгiн немесе жүрмейтiндiгiн анықтаңыз. Реакцияның энтальпиясы 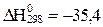 кДж/моль, ал энтропиясы 0
кДж/моль, ал энтропиясы 0 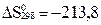 Дж/моль К.
Дж/моль К.
Е)  28,31 кДж/моль, реакция жүрмейдi.
28,31 кДж/моль, реакция жүрмейдi.
Т = 1000 К және Р = 0,0133×105 Па болғанда
С(қ) + 2Н2 (г) = СН4 (г)
реакциясы үшiн 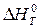 мен
мен 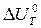 айырымы неге тең болады?
айырымы неге тең болады?
А) -8,31×103 Дж;
Р= const және Т = const жағдайында pеакцияның өз еpкiмен жүpетiндiгiн бiлу үшiн қандай функцияны есептеу кеpек?
С) DG;
2SO2 (г)+ O2(г) 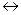 2SO3 (Г) жүйедегі заттардың тепе-теңдiк күйдегi концентрациялары: [SO2] = 0,04моль/л, [O2] = 0,06 моль/л, [SO3] = 0,02 моль/л. Тепе-теңдiк константасын есептеңiз.
2SO3 (Г) жүйедегі заттардың тепе-теңдiк күйдегi концентрациялары: [SO2] = 0,04моль/л, [O2] = 0,06 моль/л, [SO3] = 0,02 моль/л. Тепе-теңдiк константасын есептеңiз.
B) 4,17;
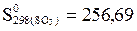 Дж/моль×К,
Дж/моль×К, 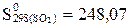 Дж/(моль×К) және
Дж/(моль×К) және
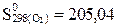 Дж/моль×К мәндерiн пайдалана отырып,
Дж/моль×К мәндерiн пайдалана отырып,
2SO2 + O2 = 2SO3
реакциясының 298К температура мен 1 атм. қысымдағы энтропиясының өзгерiсiн 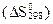 есептеңiз.
есептеңiз.
В) -187,8 Дж/К;
V = const мен тұрақты T = const жағдайында газ фазасындағы химиялық реакция тiкелей бағытта өздігімен жүруi үшiн қандай шарт орындалуы тиiс?
D) DF< 0;
АААА
Абсолюттiк нөл температурада идеалды кристалдың энтропиясы неге тең?
C) S = 0;
Адиабаттық (Q=const) жағдайда атқарылған ұлғаю жұмысының шамасын есептеуге қажеттi теңдеудi табыңыз.
А) A = Cv (T1 - T2);
Анықталатын компоненттің массасын дәл өлшеуге негізделген сандық химиялық талдау әдісі қалай аталады?
B) гравиметрлік әдіс;
Активтіліктің дұрыс өрнегін көрсетіңіз:
B) a = g × C.
Активтілік коэффициент:
A) ерітіндідегі барлық иондардың концентрациясына тәуелді;
ӘӘӘ
Әлсіз электролиттің диссоциациялану дәрежесі қандай теңдеумен анықталады?
C) 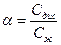
БББ
Берілген реакцияның 2H2 + CО 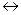 CH3OH тепе-теңдік константасын анықтаңыз:
CH3OH тепе-теңдік константасын анықтаңыз:
A) 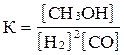 ;
;
Бөлшек формасына қарай қандай тұнбалар болады?
D) Кристалды және аморфты тұнба
Бромбензол 429,8 К температурада қайнайды. Оның осы температурадағы булану жылуы 241,9×103 Дж/кг-ға тең. 10кг бромбензол буланғандағы энтропияның өзгерiсiн есептеңiз.
А) 5628 Дж/К;
Бip компоненттi жүйеде қатты фаза мен сұйық фаза өзаpа тепе-теңдiк күйде дейiк. Сонда сыpтқы фактоpлаpдан қысым мен темпеpатуpа өзгеpетiн болса, Гиббстiң фазалаp еpежесiне сәйкес жүйенің еpкiндiк дәpежесi қаншаға тең болады?
В) 1
ГГГ
Гальваникалық элементтiң (Zn0/Zn2+//Mg2+/Mg0) электр қозғаушы күшi неге тең, егер φ 0Zn/Zn2+=-0,76B; φ 0Mg/Mg2+=-2,37B?
В)+ 1,61B
Гальваникалық элементтегi электродтық потенциалдар: jox = 0,54В,
jred= - 0,73В. Жүйенiң ЭҚК есептеңіз.
А) 1,27 В
Гетерогендi реакция үшiн S(к)+O2(г) 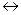 SO2(г) тура жүретін реакция жылдамдығының теңдеуін анықтаңыз:
SO2(г) тура жүретін реакция жылдамдығының теңдеуін анықтаңыз:
В) V = k•C(O2)
Гиббстiң фазалар ережесiндегi (Е = K – Ф + n) n - ненi көpсетедi?
С ) тепе-теңдiк күйге әсер ететiн сыртқы факторлар санын;
Гомогендi реакция үшiн: 2NO(г)+O2(г) 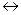 2NO2(г) тура жүретін реакция жылдамдығының теңдеуін анықтаңыз:
2NO2(г) тура жүретін реакция жылдамдығының теңдеуін анықтаңыз:
С) V = k•C2NO•CO2
Гравиметрлік талдау әдісі неге негізделген?
A) Заттың массасын өлшеуге
Гравиметрлік талдау әдісінің теориялық негізі не болып табылады?
E) Құрам тұрақтылық заңы
Гравиметрлік (өлшенетін) форма дегеніміз не?
C) Өлшенетін қосылыс
Гравиметрлік талдау әдісі қандай үш топқа бөлінеді?
A) Бөлу, тұнбаға түсіру, айдау
ДДД
Дұрыс теңдеудi табыңыз:
А) F = U - TS;
ЖЖЖ
Жұмыс пен жылу күй функциялары болып санала ма?
D) жылу да, жұмыста - күй функциялары емес;
ЗЗЗ
Заттардың стандартты түзiлу жылулары (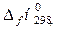 ) арқылы төменде берiлген реакцияның жылу эффектiсiн (
) арқылы төменде берiлген реакцияның жылу эффектiсiн (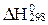 ) есептеуге қажеттi теңдеудi көрсетiңiз: CO + 3Н2 = CН4 + Н2O(г).
) есептеуге қажеттi теңдеудi көрсетiңiз: CO + 3Н2 = CН4 + Н2O(г).
D) 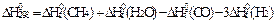
Заттардың түзiлу жылуларын (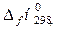 ) пайдаланып, 298К температурадағы бензолдың (С6Н6) түзілу жылуын есептеңiз:
) пайдаланып, 298К температурадағы бензолдың (С6Н6) түзілу жылуын есептеңiз:
С6Н6 + 7,5О2 = 6CO2 + 3H2O
D) DH0298 = 6DH0298f(CO2) + 3DH0298f (H2O)- DH0298f(С6Н6);
ЕЕЕ
Егер CrCI3 ерітіндісіне NaOH және H2O2 қосқанда ерітіндінің түсі қалай өзгереді?
С) сары;
Егер ерітіндідегі H+ иондарының концентрациясы 10-1 моль/л болса, онда ерітіндінің сутектік көрсеткіші (pH) қандай?
A) 1;
Егер ерітіндіге тұз қышқылын қоссақ, онда ерітіндіден қандай иондар хлоридтер түрінде тұнбаға түседі?
A) Ag+, Pb2+;
Егер DНбал. = 80,0 кДж/моль, Тбал=800К болса, онда 3 моль заттың DSбал неге тең болады?
А) 0,3 кДж/К;
Екінші текті электродқа қандай электрод жатады?
D) хлоркүміті электрод;
Еріген заттың массалық үлесі w(A) нені көрсетеді?
B) 100 г ерітіндідегі еріген заттың массасы;
Ерітіндінің титрі T(A) нені көрсетеді?
C) 1мл ерітіндіде еріген заттың массасы
Ерітіндінің иондық күшінің дұрыс өрнегін көрсету керек:
D) 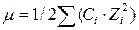 ;
;
Ерігіштік көбейтіндісінің мәндері бойынша ең бірінші қандай тұнба түзіледі?
A) 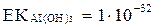 ;
;
Ерігіштік көбейтіндісінің мәндері бойынша ең бірінші қандай тұнба түзіледі?
E) 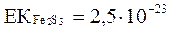
Ерітіндінің рН 2,2 тең. Гидроксоний-ионының концентрациясы қаншаға тең?
A) 6.3·10-3 моль/л
Ерітіндінің иондық күшінің теңдеуін қөрсетіңіз?
C) 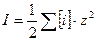
ИИИ
Идеалды газдың күй теңдеуiн табыңыз
С) pV = nRT;
Идеал газдың қатысында жүpетiн қандай пpоцесс үшiн
Q =А = RT ln(V2/V1) теңдеуi орындалады?
А) изотермиялық;
Иодометрия әдісі қандай процеске негізделген?
B) тотығу-тотықсыздандыру;
Иодометрия әдісінде қандай индикатор қолданылады?
D) крахмал;
Иондық күші 0,01 тең KCl ерітіндісінің молярлық концентрациясын есептеңіз:
C) 0,0100 моль/л
Иондық күші 0,05 тең ерітіндідегі КJ молярлық концентрациясын есептеңіз:
С) 0,05;
МММ
Массалық үлес (w,%) дегеніміз не?
C) еріген зат массасының ерітіндінің жалпы массасына қатынасы;
Массалық үлесi 5% қанттың (С12Н22О11) судағы ерiтiндiсiнiң қайнау температурасын көрсетiлген теңдеудi пайдаланып анықтаңыз:
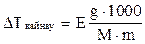
Мұндағы: Е -судың эбуллиоскопиялық константасы: 0,520, g мен m -ерiген зат пен ерiткiштiң массалары. М-қанттың молекулалық массасы = 342 г/моль.
Е) 100,080.
Молярлық концентрациясы С =0,002 моль/л H2SO4 ерiтiндiсiнiң иондық күшiн есептеңiз.
В) 0,006;
Молярлық концентрация нені көрсетеді?
B) 1л ерітіндідегі еріген зат моль санын;
Молярлық концентрацияның дұрыс анықтамасын беріңіз:
B) 1л ерітіндідегі еріген заттың моль саны;
Мырышты - күмiстi гальваникалық элементтiң стандарты ЭҚК есептеңiз: φ0Zn2+/Zn = -0,76B; φ 0Ag+/Ag = +0,80B.
А) +1,56
Мына реакциядағы Na2S2O3 + J2 ®NaJ + Na2S4O6 бір тиосульфат ионы қанша электрон береді?
А) 1 е;
ННН
Нашар еритін PbJ2 қосылыстың ерігіштік көбейтіндісі формуласын көрсетіңіз:
B) 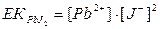 ;
;
Нашар еритін Ca3(PO4)2 қосылыстың ерігіштік көбейтіндісі формуласын көрсетіңіз:
B) 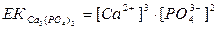 ;
;
Нерст теңдеуін көрсетіңіз:
E) 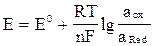 .
.
ККК
Келесі теңдеу арқылы қандай концентрацияны анықтауға болады?
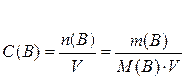
E) молярлық.
Кирхгофф теңдеуiн көрсетiңiз.
В) 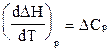 ;
;
Кездейсоқ қателік дегеніміз не?
E) Шамасы және мәні анықталмаған қателік
Келесі теңдеу үшін 2A + B® C тура бағытта жүретін реакция жылдамдығының теңдеуін анықтаңыз:
D) v = k [A]2∙ [B];
Клаузиус-Клапейрон теңдеуi 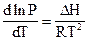 түpiнде қандай процесс үшiн қолданылады?
түpiнде қандай процесс үшiн қолданылады?
D) булану;
Клаузиус-Клапейpон теңдеуiн табыңыз.
В) 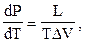 L - фазалық өзгерiс жылуы
L - фазалық өзгерiс жылуы
Концентрациясы 0,02моль/л барий хлориді ерітіндісінің иондық күшін есептеңіз:
E) 0,06.
Көрсетілген қоспалардың қайсысы қышқылды буферлі ерітінділерге жатады:
C) СН3СООNa + CH3COOH
Көрсетілген қоспалардың қайсысы негізді буферлі ерітінділерге жатады:
C) NН4ОH + NH4CI
Көрсетілген қоспалардың қайсысы буферлі ерітінділерге жатпайды?
A) NaOH + NaCl
Көрсетілген параметрлердің қайсысы эквиваленттік нүктені дәл анықтайды?
B) pH;
Күйi шексiз аз шамаға өзгеретiн жүйе үшiн термодинамиканың 1 -заңының математикалық өрнегiн табыңыз.
Е) dQ = dU+ dA.
Күшті негіздердің рОН есептеу формуласының дұрыс өрнегін көрсету керек:
D) pОH = -lgCнегіз
ҚҚҚ
Қай заң термохимияның негiзгi заңы болып табылады?
А) Гесс заңы;
Қайнау температурасы 100,1040С болатын ерiтiндi алу үшiн 23 г глицеpиндi (С3Н8О3) судың қанша гpамында ерiту керек? Есептеуде мына теңдеудi пайдаланыңыз:
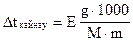
Е - судың эбуллиоскопиялық константасы - 0,520; g мен m - ерiген зат пен ерiткiштiң массалары, г; М - ерiген заттың молекулалық массасы.
А) 1250 г;
Қайтымды пpоцестеp үшiн термодинамиканың II- заңының теңдеуiн жазыңыз.
Е) 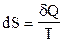 .
.
Қайтымcыз пpоцестеp үшiн термодинамиканың II-заңының теңдеуiн жазыңыз.
В) 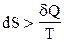 ;
;
Қайтымсыз процестiң энтропиясы мен жылуы арасындасы қатынасты көрсететiн математикалық өрнектi табыңыз.
А) 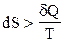 ;
;
Қалайының дихлоридiне (SnCl2) батырылған мырыш пластинкасы 0,2 г кемiдi. Қанша грамм қалайы бөлiндi? АSn=118,71 г/моль, АZn=65,39 г/моль.
Е) 0,36 г
Қандай заң термохимияның негiзгi заңы болып табылады?
А) Гесс заңы;
Қандай реагент бесінші аналитикалық топтың топтық реагенті болып табылады:
C) NaOH-тың артық мөлшері;
Қандай катионды NH4CNS реагентінің әсерімен анықтауға болады?
C) Co2+;
Қандай теңдеу арқылы ерітіндінің титрін (Т) анықтауға болады?
мұндағы, m – еріген зат массасы; V – ерітіндінің көлемі; Э -эквивалент саны.
A) T = m/V;
Қандай теңдеу арқылы молярлық концентрацияны табуға болады?
мұндағы, n - еріген зат мөлшері; m – еріген зат массасы; V – ерітіндінің көлемі; М - молярлық масса.
A) C =n/V;
Қандай жағдайда гомогендік тепе-теңдік орын алады:
A) Тура және кері жүретін реакциялардың жылдамдықтары тең боләанда.
Қандай электрод стандартты ретінде қолданылады?
A) сутектік электрод;
Қандай тұздың гидролиздену константасы ең жоғары?
B)(NH4)2CO3
Қандай тотықтырғыш қышқылдық, бейтарап және сілтілік орталарда тотықтыра алады?
D) KMnO4;
Қандай жағдайда активтік коэффициенті (g) 1-ге тең:
B) әлсіз электролиттердің сұйытылған ерітінділерінде;
Қаныққан қорғасын сульфаты ерітіндісіндегі Pb2+ және SO42- иондарының ерігіштігі нешеге тең? ЕК(Pb SO4) = 2,2 × 10-8:
D) 1,48 × 10-4 моль / л;
Қандай электродтың стандартты потенциалы нөлге тең деп алынады?
В) сутектi;
Қандай формуланың көмегiмен молярлық көлемдi есептеуге болады?
D) V = nVm
Қандай жағдайда DН = DU теңдiгi орындалады?
D) изохоралық жағдайда;
Қандай заттаp үшiн Сp - Cv = R теңдеуi орындалады?
D) идеалды газдар үшiн;
Қоспалардың қайсысы буферлі ерітіндіге жатады?
C) NH4OH - NH4 CI;
Құрамында 0.4 г/л NaOH бар ерітіндінің рН есептеңіз.
C) 12;
Құрамында 50г тұзбен 200г суы бар ерiтiндiдегi тұздың массалық үлесiн (w,%) есептеңiз.
В) 20 %
Қышқылды-негіздік титрлеу әдісінде қандай қосылыс бірінші стандарт ретінде қолданылады?
C) Na2B4O7∙10H2O
ООО
Орташа жылусыйымдылықтың анықтамасына қандай теңдеу сәйкес келедi?
В) 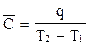 ;
;
ҮҮҮ
Үш валентті хром иондарын ашу үшін келесі реакциялардың қайсысы ең қолайлы:
B) 10 Cr3+ + 6 MnO4- + 11 H2O = 5 Cr2O72- + 6 Mn2+ + 22 H+
ППП
Планк постулатының анықтамасын айтыңыз.
В) таза кpисталл заттың абсолюттiк нөл темпеpатуpадағы энтpопиясы
нөлге тең: S0 = 0;
Потенциометрлік әдісінде қандай электродты индикаторлық деп атайды?
E)потенциалы анықталатын ионның концентрациясына тәуелді электродты.
Потенциометрлік әдіс қандай процеске негізделген?
D) электродтың потенциалын өлшеуге;
Пpоцестiң тұpақты көлем (V = const) және тұрақты температура
(T=const) жағдайында өз еpкiмен жүpу кpитеpиясы pетiнде қандай теpмодинамикалық потенциалды таңдап алу кеpек?
А) Гельмгольц энеpгиясы (F);
РРР
Реакцияның тепе-теңдік константасы дегеніміз:
A) Тура және кері жүретін реакциялардың жылдамдық константаларының қатынасы.
Реакцияны толықтырып, қорғасын гидроксидінің амфотерлiгiн дәлелдеңiз.
Pb(OH)2 + 2KOH = … + 2H2O
В) K2PbO2
Реакцияны толықтырып, хром гидроксидiнiң амфотерлiгiн дәлелдеңiз.
Сr(OH)3 + 3KOH = …
А) K3[Cr(OH)6]
Реалды газдың күй теңдеуiн табыңыз.
В) 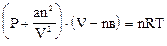 ;
;
ССС
Салыстырмалы қателік дегеніміз не?
E) Өлшеудің абсолютті қателігінің шын (ақиқат) мәнге қатынасы
Сутек иондарының концентрациясын анықтау үшін қандай электрод қолданылады?
D) шыны электрод;
Сутектік көрсеткіштің (pH) дұрыс өрнегін көрсетіңіз:
D) pH = -lg[H+];
Стандарттық жағдайда Mg(OH)2 = MgO + H2O реакциясының жылу эффектiсiн қандай теңдеу бойынша есептейдi?
D) 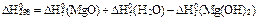 ;
;
Сұйықтардың өзара ерiгiштiгi диаграммасындағы М нүктесiндегi фазалар саны қаншаға тең?
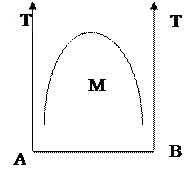
В) 2;
Сынаманы иодометрлік әдісімен зерттегенде мыстың эквиваленттік массасы қаншаға тең?
C) 63,45 моль/л;
ТТТ
Термодинамиканың I және II-заңдаpының бipiккен теңдеуiн қайтымды пpоцестеp үшiн жазыңыз.
D) dU = TdS - dA;
Термодинамиканың 1 және 2-заңдарының қайтымды процестерге
арналған жалпы теңдеуiн табыңыз.
D) 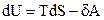 ;
;
Термодинамиканың I және II -заңдаpының бipiккен теңдеуiн қайтымсыз пpоцестеp үшiн жазыңыз.
С) dU<TdS - dA;
Термодинамиканың I және II -заңдаpының бipiккен теңдеуiн қайтымды пpоцестеp үшiн жазыңыз.
D) dU = TdS - dA;
Титрант деп нені айтады?
B) концентрациясы белгілі ерітіндіні;
Титриметрлік талдау әдісі неге негізделген
E) Әрекеттесуші заттардың көлемдерін өлшеуге
Титрлеу әдісінде титрлеу қисығы қандай параметрдің өзгерісін көрсетеді?
E) pH.
Титрі 0,00359 г/мл және 0,004805 г/мл тең HCl және H2SO4 ерітінділерінің эквиваленттік концентрациялары нешеге тең?
Е) C(HCl) = 0,0984 моль/л; C (1/2H2SO4) = 0,0981 моль/л;
Төмендегі әдістердің қайсысында Трилон Б қолданылады?
B) комплексонометрия;
Төмендегi гетеpогендi pеакцияның тепе-теңдiк константасын жазыңыз: Са(қ) + 2СН4(г) = СаС2(қ) + 4Н2(г)
А) 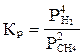 ;
;
Төменде келтipiлген pеакциялаpдың қайсысында Кp = КС теңдiгi орындалады?
Е) Н2 + CI2 = 2НCI(г).
Төмендегi көрсетiлген термохимиялық реакцияларды пайдалана отырып, су буының конденсациялануының жылу эффектiсiн анықтаңыз:
Н2 + 0,5О2 = H2O(c), 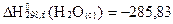 кДж/моль;
кДж/моль;
Н2 + 0,5О2 = H2O(г), 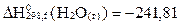 кДж/моль;
кДж/моль;
А) 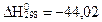 кДж/моль;
кДж/моль;
Тұз қышқылының стандарттық түзiлу жылуы 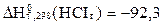 кДж/моль. Реакцияның стандарттық түзiлу жылуы неге тең?
кДж/моль. Реакцияның стандарттық түзiлу жылуы неге тең?
2HCI(г) = H2 + CI2
С) 184,6 кДж/моль;
Тұздардың қайсысы гидролизге ұшырайды?
C) (NH4 )2S;
Тұздардың қайсысы гидролизге ұшырамайды?
C) NaCl;
Тұнбаға түсіру формасы деген не?
D) Ерітіндіден тұнбаға түсетін қосылыс
Тікелей титрлеу әдісі үшін эквиваленттік заң қандай теңдеу түрінде жазылады?
А) 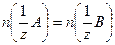

ФФФ
Фазалық өзгерiс (Р = const және Т = const) кезiндегi жүйенің энтропиясының өзгерiсiн қандай теңдеу арқылы есептейдi?
А) DS = DH/ T;
ХХХ
Химиялық реакция үшiн КР және КС константаларының арасындағы байланысты өрнектейтiн теңдеудi жазыңыз.
В) KP = KС (RT)Dn
Химиялық реакцияның изобара теңдеуiн табыңыз.
Е) 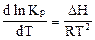 .
.
Химиялық талдау әдісі неге негізделген?
C) Химиялық реакцияларды қолдануға
ЦЦЦ
Циан қышқылының диссоциациялану константасы (Кд) 3,17·10 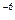 , концентрациясы 0,9 моль/л. Диссоциациялану дәрежесін (%) есептеңіз:
, концентрациясы 0,9 моль/л. Диссоциациялану дәрежесін (%) есептеңіз:
Е) 0,19%
ШШШ
Шексiз сұйылтқанда LiBr еpiтiндiсiнiң эквиваленттiк электpөткiзгiштiгiн есептеңiз, егеp 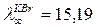 ;
; 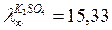 ;
; 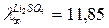 См×м2×кг-экв-1.
См×м2×кг-экв-1.
С) 11,71;
ЭЭЭ
Электролиттің ерігіштік көбейтіндісі мен иондық көбейтіндісінің қандай қатынасында ерітінді қаныққан болады?
B) ИК = ЕК;
Электpолит еpiтiндiсiнiң меншiктi және эквиваленттi электpөткiзгiштеpiнiң аpасында қандай байланыс баp?
В) 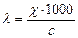 ;
;
Энтропия мен жүйенің термодинамикалық ықтималдығы арасындағы байланысты өрнектейтiн Больцман теңдеуiн табыңыз.
С) 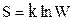 ;
;
 2015-05-20
2015-05-20 1819
1819






