Базы знаний в интеллектуальной системе
Ниже перечислены интересные особенности, которые могут (но не обязаны) быть у интеллектуальной системы, и которые касаются баз знаний.
1. Машинное обучение: Это модификация своей БЗ в процессе работы интеллектуальной системы, адаптация к проблемной области. Аналогична человеческой способности «набирать опыт».
2. Автоматическое доказательство (вывод): Способность системы выводить новые знания из старых, находить закономерности в БЗ. Некоторые авторы считают, что БЗ отличается от базы данных наличием механизма вывода.
3. Интроспекция: Нахождение противоречий, нестыковок в БЗ, слежение за правильной организацией БЗ.
4. Доказательство заключения: Способность системы «объяснить» ход её рассуждений по нахождению решения, причем «по первому требованию».
Математическая формулировка задачи базируется на системе уравнений неразрывности многокомпонентной среды при наличии химических реакций:
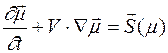
где 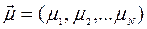 - вектор отношений смеси рассматриваемых примесей, N - число рассматриваемых примесей,
- вектор отношений смеси рассматриваемых примесей, N - число рассматриваемых примесей, 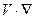 - линейный дифференциальный оператор, описывающий пространственный перенос примеси, S - скорость фотохимического изменения, которая определяется протекающими в атмосфере процессами фотодиссоциации, бимолекулярными и трехмолекулярными химическими реакциями, мономолекулярным распадом и гетерогенными процессами.
- линейный дифференциальный оператор, описывающий пространственный перенос примеси, S - скорость фотохимического изменения, которая определяется протекающими в атмосфере процессами фотодиссоциации, бимолекулярными и трехмолекулярными химическими реакциями, мономолекулярным распадом и гетерогенными процессами.
Отношение смеси представляет собой безразмерную величину, соответственно, размерность источникова члена в правой части уравнения будет с-1. В химической же кинетике, которая используется для параметризации химических процессов в атмосфере, применяются скорости химических реакций в размерности мол/(см3с). Т.е. химия атмосферы рассматривается в абсолютных единицах, т.к. скорости реакций зависят от концентраций, а не от отношений смеси. Поэтому после параметризации скоростей химических реакций в абсолютных единицах для подстановки в систему уравнений баланса нужно перейти в относительные единицы путем деления на концентрацию воздуха, т.к.
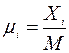
Реакция фотодиссоциации представляет собой первичный процесс, с которого, по сути, начинаются химические реакции в атмосфере. Фотодиссоциация представляет собой реакцию первого порядка вида:
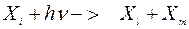
Скорость фотодиссоциации Si компоненты с концентрацией Xi описывается, согласно реакцией первого порядка в абсолютных единицах:
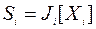
где Ji - коэффициент фотодиссоциации, 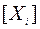 концентрация воздуха. Это скорость разрушения
концентрация воздуха. Это скорость разрушения 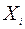 и, одновременно, скорость образования
и, одновременно, скорость образования 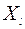 и
и 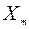 :
:
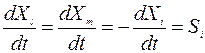
Коэффициент фотодиссоциации определяется условиями прохождения солнечной радиации через атмосферу
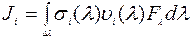
где 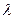 - длина волны солнечного излучения,
- длина волны солнечного излучения,
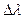 - спектральная область фотодиссоциации i-й компоненты,
- спектральная область фотодиссоциации i-й компоненты,
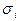 - сечения поглощения,
- сечения поглощения,
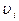 - квантовый выход реакции,
- квантовый выход реакции,
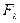 - суммарный поток радиации с длиной волны
- суммарный поток радиации с длиной волны 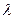 в данной точке пространства.
в данной точке пространства.
Скорости химических реакций и мономолекулярного распада параметризуются в терминах химической кинетики. При этом скорости бимолекулярных реакций типа
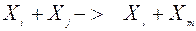
описываются выражением
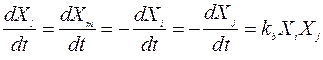
где 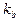 - лабораторная константа данной химической реакции, рассчитываемая по формуле Аррениуса:
- лабораторная константа данной химической реакции, рассчитываемая по формуле Аррениуса:
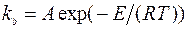
Здесь A - лабораторная константа, E - энергия активации данной реакции, R - универсальная газовая постоянная, T - температура.
Более сложным образом описываются скорости протекающих в атмосфере трехмолекулярных реакций типа
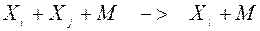
где M - концентрация воздуха. Фактически эти реакции происходят в два бимолекулярных этапа. Сначала происходит реакция образования промежуточного неустойчивого энергизированного (возбужденного) комплекса:
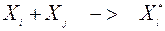
Далее этот комплекс может или дезактивироваться, или распадся:
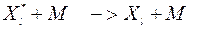
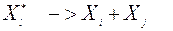
Реакции такого типа сильно зависят от давления. При низких давлениях время между столкновениями образующегося на первой стадии реакции возбужденного комплекса с дезактивирующей молекулой больше или сравнимо со временем жизни возбужденного комплекса и реакция является тримолекулярной. При высоких давлениях время между столкновениями мало по сравнению со временем жизни возбужденного комплекса и он успевает дезактивироваться до распада. Реакция при этом является бимолекулярной.
Если скорость реакции образования возбужденного комплекса обозначить 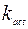 , скорость деактивации -
, скорость деактивации - 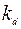 , а скорость распада -
, а скорость распада - 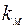 , то баланс образующейся компоненты
, то баланс образующейся компоненты 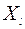 определяется по формуле
определяется по формуле
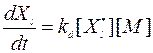
А концентрация возбужденного комплекса определяется их условия равновесия между продукцией и разрушением:
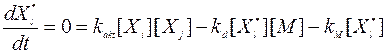
Откуда можно рассчитать равновесную концентрацию
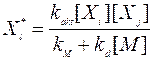
С учетом этого скорость трехмолекулярной реакции описывается по аналогии с бимолекулярными реакциями:
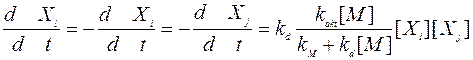
где кр описывается универсальной формулой Линдемана-Хиншельвуда [76]:
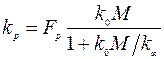
где
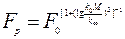
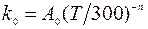
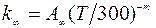
а F0, A0, 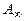 , n, m - лабораторные константы данной химической реакции.
, n, m - лабораторные константы данной химической реакции.
Процессы мономолекулярного распада типа
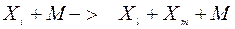
являются обратными по отношению к трехмолекулярным и рассматриваются как реакции второго порядка и их скорости записываются в виде
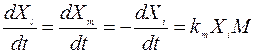
где k определяется по формуле Аррениуса (1.5).
Гетерогенные процессы на атмосферном аэрозоле в фотохимических моделях описываются уравнениями первого порядка:
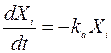
Константы гетерогенных реакций k a вычисляются в предположении свободномолекулярного режима.
Таким образом, слагаемые в правой части системы (1.1), выражающие скорости фотохимического изменения рассматриваемых малых газов, можно записать в виде:
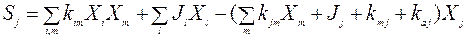
j=1,2,...N,
где члены в правой части с положительным знаком описывают фотохимическую продукцию (за счет химических реакций и фотодиссоциационных процессов), а члены с отрицательным знаком - фотохимическое разрушение (за счет химических реакций, фотодиссоциационных процессов, мономолекулярного распада и гетерогенных процессов).
 2014-02-09
2014-02-09 511
511






