В соответствие с уравнением Вант-Гоффа:
· концентрация раствора С 1 до разбавления: 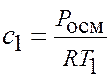 .
.
· осмотическое давление раствора Р' осм. после разбавления и повышения Т:
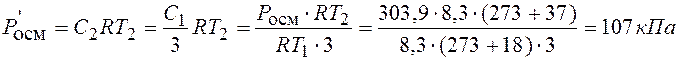
ПРИМЕР
Оцените степень диссоциации a по 1-й ступени в 0,005 М и 0,05 М растворах сернистой кислоты Н2SО3.
Решение.
Н2SО3 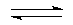 Н+ + НSО3-, К Д1 = 1,7×10 -2 (1-я ступень)
Н+ + НSО3-, К Д1 = 1,7×10 -2 (1-я ступень)
! значение К Д1 относительно велико (> 10-4) Þ
расчет a по строгой формуле Оствальда:
К Д = a2 с 0/(1 - a).
·
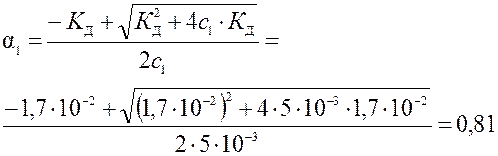 |
Для 0,005 М раствора:
! Расчет по приближенной формуле (К Д» a2 с 0) приводит к величине a > 1, что не имеет смысла.
· Для 0,05 М раствора
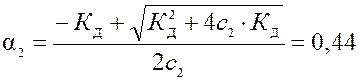 |
Значение a, рассчитанное по приближенной формуле (» 0,58) сильно отличается и неверно!
a - уменьшается с ↑ концентрации
 2015-05-26
2015-05-26 1222
1222








