Воспользовавшись одной из величин [H+] или [OH-], можно количественно охарактеризовать кислотные и щелочные свойства растворов. Обычно для этого используют концентрацию катионов водорода [Н+], но эта величина выражается дробными и часто очень малыми числами, которыми неудобно оперировать. Поэтому для количественной характеристики кислотности или щелочности раствора пользуются особой величиной, называемой водородным показателем (рН):
pH = - lg [H+].
Тогда для нейтральной среды рН = 7, для кислотной среды pH < 7, для щелочной среды рН > 7.
В табл. 2.1. показана взаимосвязь концентраций ионов Н+, ОН-и рН в кислых и щелочных растворах.
Таблица 2.1. Водородный показатель растворов
| Концентра- ция ионов | Усиление щелочных свойств ------------------------- | Нейтраль-ная среда | Усиление кислотных свойств ---------------------® |
| [OH- ] | 1(10O) 10-2 10-4 10-6 | 10-7 | 10-8 10-10 10-12 10-14 |
| [H+] | 10-14 10-12 10-10 10-8 | 10-7 | 10-6 10-4 10-2 10O |
| рH | 14 12 10 8 | 6 4 2 0 |
Простым методом оценки величины рН является метод, основанный на применении индикаторов - веществ, изменяющих свою окраску в зависимости от концентрации ионов Н+, т.е. величины рН раствора.
Изменение окраски каждого индикатора наблюдается только в некоторых пределах значений рН (табл.2.2).
Интервал значений рН, в котором окраска индикатора изменяется в соответствии с изменением рН, называется областью перехода или интервалом индикатора.
Таблица 2.2. Важнейшие индикаторы
| Название индикатора | Цвет при значении рН ниже интервала индикатора | Интервал индикатора рН | Цвет при значении рН выше интервала индикатора |
| Метилоранж | Красный | 3,2 - 4,4 | Желтый |
| Метилрот | Красный | 4,2 - 6,2 | Желтый |
| Лакмус | Красный | 5,0 - 8,0 | Синий |
| Фенолрот | Желтый | 6,8 - 8,2 | Красный |
| Фенолфталеин | Бесцветный | 8,2 - 10,0 | Малиновый |
На практике определение рН сводится к тому, что к исследуемому раствору добавляется индикатор и полученная окраска раствора сравнивается с окраской эталонных растворов серии, содержащей тот же индикатор или с эталонами цветной шкалы, где указан рН для каждого эталона. Вместо раствора индикатора часто применяют пропитанные им полоски фильтровальной бумаги. Эти полоски смачивают раствором, рН которого необходимо определить, и сравнивают образующуюся окраску со шкалой.
Приведем несколько примеров вычисления рН по концентрации ионов водорода и, наоборот, расчета концентрации ионов водорода по известному значению рН.
В разбавленных растворах сильных кислот и оснований типа НCl, HNO3, KOH, NaOH молярная концентрация ионов водорода и гидроксил-ионов совпадает с молярной концентрацией кислоты или основания. Поэтому в 0,001М растворе НCl концентрация ионов водорода [H+]=0,001 моль/л и рН = - lg0,001 = 3. В 0,001М растворе КОН концентрация гидроксил-ионов равна [OH-] = 0,001 моль/л, значит
[H+]= 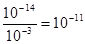 моль/л и рН = -lg 10-11= 11.
моль/л и рН = -lg 10-11= 11.
 2015-05-26
2015-05-26 643
643








