dQ=dU= 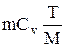 . (2.5.1)
. (2.5.1)
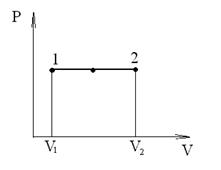
Изобарный процесс (p=const). Диаграмма этого процесса (изобара) в координатах р, V изображается прямой, параллельной оси V. При изобарном процессе работа газа при расширении объема от V1 до V2 равна
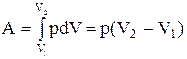 (2.5.2)
(2.5.2)
и определяется площадью прямоугольника, выполненного в цвете на рис. 60. Если использовать уравнение Клапейрона - Менделеева для выбранных нами двух состояний, то
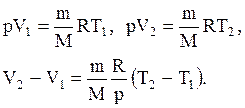
Тогда выражение для работы изобарного расширения примет вид
 |
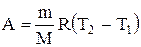 . (2.5.3)
. (2.5.3)Рис. 2.5.2
Из этого выражения вытекает физический смысл молярной газовой постоянной R: если Т2-T1 =1 К, то для 1 моля газа R = А, т.е. R численно равна работеизобарного расширения 1 моля идеального газа при нагревании его на 1 К.
В изобарном процессе при сообщении газу массой m количества теплоты
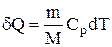
его внутренняя энергия возрастает на величину
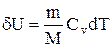 .
.
При этом газ совершит работу, определяемую выражением (2.5.3).
Изотермический процесс (T=const). Изотермический процесс описывается законом Бойля - Мариотта: PV=const.
Диаграмма этого процесса (изотерма)в координатах р, V представляет собой гиперболу (рис. 2.5.3), расположенную на диаграмме тем выше, чем выше температура, при которой происходил процесс.
Исходя из выражений (2.5.3) и (2.5.2) найдем работу изотермического расширения газа:
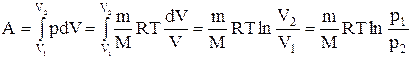 .
.
Так как при T=const внутренняя энергия идеального газа не изменяется
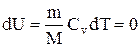
то из первого начала термодинамики (dQ=dU+dA) следует, что для изотермического процесса
dQ=dA,
т.е. все количество теплоты, сообщаемое газу, расходуется на совершение им работы против внешних сил:
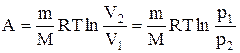 . (2.5.4)
. (2.5.4)
Следовательно, для того, чтобы при работе расширения температура не уменьшалась, к газу в течение изотермического процесса необходимо подводить количество теплоты, эквивалентное внешней работе расширения.
 2015-06-04
2015-06-04 460
460








