Внутренняя энергия. Работа в термодинамике.
Если потенциальная энергия взаимодействия молекул равна нулю, то внутренняя энергия равна сумме кинетических энергий движения всех молекул газа 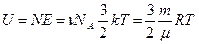 . Следовательно, при изменении температуры изменяется и внутренняя энергия газа. Подставив в уравнение для энергии уравнение состояния идеального газа, получим, что внутренняя энергия прямо пропорциональная произведению давления газа на объем.
. Следовательно, при изменении температуры изменяется и внутренняя энергия газа. Подставив в уравнение для энергии уравнение состояния идеального газа, получим, что внутренняя энергия прямо пропорциональная произведению давления газа на объем. 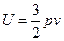 . Внутренняя энергия тела может изменяться только при взаимодействии с другими телам. При механическом взаимодействии тел (макроскопическом взаимодействии) мерой передаваемой энергии является работа А. При теплообмене (микроскопическом взаимодействии) мерой передаваемой энергии является количество теплоты Q. В неизолированной термодинамической системе изменение внутренней энергии DU равно сумме переданного количества теплоты Q и работы внешних сил А. Вместо работы А, совершаемой внешними силами, удобнее рассматривать работу А`, совершаемую системой над внешними телами. А=–А`. Тогда первый закон термодинамики выражается как
. Внутренняя энергия тела может изменяться только при взаимодействии с другими телам. При механическом взаимодействии тел (макроскопическом взаимодействии) мерой передаваемой энергии является работа А. При теплообмене (микроскопическом взаимодействии) мерой передаваемой энергии является количество теплоты Q. В неизолированной термодинамической системе изменение внутренней энергии DU равно сумме переданного количества теплоты Q и работы внешних сил А. Вместо работы А, совершаемой внешними силами, удобнее рассматривать работу А`, совершаемую системой над внешними телами. А=–А`. Тогда первый закон термодинамики выражается как 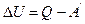 , или же
, или же 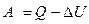 . Это означает, что любая машина может совершать работу над внешними телами только за счет получения извне количества теплоты Q или уменьшения внутренней энергии DU. Этот закон исключает создание вечного двигателя первого рода.
. Это означает, что любая машина может совершать работу над внешними телами только за счет получения извне количества теплоты Q или уменьшения внутренней энергии DU. Этот закон исключает создание вечного двигателя первого рода.
Количество теплоты. Удельная теплоемкость вещества. Закон сохранения энергии в тепловых процессах (первый закон термодинамики).
Процесс передачи теплоты от одного тела к другому без совершения работы называют теплообменом. Энергия, переданная телу в результате теплообмена, называется количеством теплоты. Если процесс теплопередачи не сопровождается работой, то на основании первого закона термодинамики 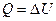 . Внутренняя энергия тела пропорциональна массе тела и его температуре, следовательно
. Внутренняя энергия тела пропорциональна массе тела и его температуре, следовательно 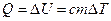 . Величина с называется удельной теплоемкостью, единица –
. Величина с называется удельной теплоемкостью, единица – 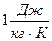 . Удельная теплоемкость показывает, какое количество теплоты необходимо передать для нагревания 1 кг вещества на 1 градус. Удельная теплоемкость не является однозначной характеристикой, и зависит от работы, совершаемой телом при теплопередаче.
. Удельная теплоемкость показывает, какое количество теплоты необходимо передать для нагревания 1 кг вещества на 1 градус. Удельная теплоемкость не является однозначной характеристикой, и зависит от работы, совершаемой телом при теплопередаче.
При осуществлении теплообмена между двумя телами в условиях равенства нулю работы внешних сил и в тепловой изоляции от других тел, по закону сохранения энергии 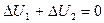 . Если изменение внутренней энергии не сопровождается работой, то
. Если изменение внутренней энергии не сопровождается работой, то 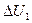 , или же
, или же 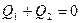 , откуда
, откуда 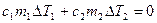 . Это уравнение называется уравнением теплового баланса.
. Это уравнение называется уравнением теплового баланса.
 Уравнение теплового баланса – количество теплоты, отданное одним телом, равно по модулю количеству теплоты, полученному другим телом.
Уравнение теплового баланса – количество теплоты, отданное одним телом, равно по модулю количеству теплоты, полученному другим телом.
Удельная теплоёмкость вещества – количество теплоты которое, нужно сообщить единице массы вещества, чтобы изменить его температуру на 1 0С.
Закон сохранения энергии – энергия в природе не возникает из ничего и не исчезает: количество энергии неизменно. Она только переходит из одной формы в другую.
Внутренняя энергия -сумма кинетических энергий хаотичного движения всех молекул относительно центра масс тела и потенциальных энергий взаимодействия всех молекул друг с другом.
Первый закон термодинамики - изменение внутренней энергии системы при переходе ее из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданного системе, и оно не зависит от способа, которым осуществляется этот переход.
Адиабатный процесс – это процесс, протекающий в теплоизолированной системе.
Коэффициентом полезного действия теплового двигателя называют отношение работы А`, совершаемой двигателем, к количеству теплоты, полученному от нагревателя.
Тепловые двигатели – устройства, превращающие внутреннюю энергию топлива в механическую энергию движения.
1) Q=cmΔt Количество теплоты необходимое для нагревания тела.
2) Q=λm Количество теплоты необходимое для плавления тела.
3) Q=Lm Количество теплоты необходимое для парообразования тела.
4) Q=qm Количество теплоты выделяемое при полном сгорании топлива.
5) ΔU = i/2·m/m/MRT Изменение внутренней энергии.
6) A=pΔV Работа над телом.
7) Q=ΔU+A΄ I закон термодинамики.
8) Q1 + Q2 + Q3 + …= 0 Уравнение теплового баланса.
9) η = (Q1 - Q2) / Q1 · 100% КПД теплового двигателя.
10) η = (T1-T2)/T1·100% КПД Карно.
 2015-06-05
2015-06-05 778
778








