1. Определить количество моль воды в формуле кристаллогидрата Na2CO3·хH2O, если в результате прокаливания его масса изменилась от 1,43 до 0,53 г. Определить объем выделившейся парообразной воды при 200оС и давлении 98,2 кПа.
Дано: 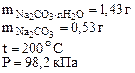 | РЕШЕНИЕ: При прокаливании кристаллогидрата протекает реакция: Na2CO3·nH2O 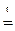 Na2CO3 +nH2O↑ (1.1) Находим массу воды ( Na2CO3 +nH2O↑ (1.1) Находим массу воды (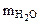 ), выделившейся при разложении кристаллогидрата: ), выделившейся при разложении кристаллогидрата: |
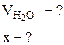 |
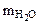 = 1,43 - 0,53 = 0,9 г
= 1,43 - 0,53 = 0,9 г
Расчет n ведем по уравнению реакции (1.1)
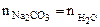 или
или 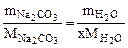 , тогда
, тогда
х = 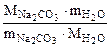 =
= 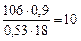
где 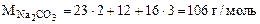
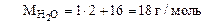
Формула кристаллогидрата Na2CO3·10H2O
Рассчитываем объем выделившейся газообразной воды при
Т = 273 + 200 = 473 К и Р = 98,2 кПа по уравнению Менделеева-Клапейрона
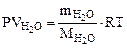
где Р – Па, V – м3, m – кг, М 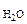 – кг/моль, R – 8,314 Дж/моль·К,
– кг/моль, R – 8,314 Дж/моль·К,
Т – К.
Откуда 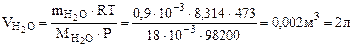
Ответ: формула кристаллогидрата: Na2CO3·10Н2О; 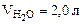
2. Определить состав смеси (% масс.), содержащей карбонат магния (15 г) и оксид магния. Если после прокаливания смеси, полученный продукт вступил в реакцию с ортофосфорной кислотой и образовалось 80 г ортофосфата магния. Составить уравнения реакций.
Дано: MgO и MgCO3 m 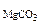 = 15 г m = 15 г m 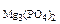 = 80 г = 80 г | РЕШЕНИЕ: 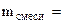 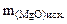 + + 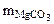 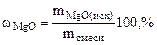 мас. мас. 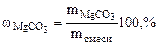 мас. мас. |
ω 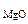 -? ω -? ω 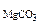 -? -? |
При прокаливании смеси протекает реакция
MgCO3 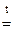 MgO + CO2
MgO + CO2
Тогда по этому уравнению
n 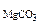 =
= 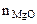 (из MgCO3) или
(из MgCO3) или 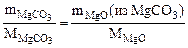
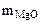 (из MgCO3) =
(из MgCO3) = 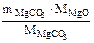 =
= 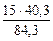 = 7,17 г
= 7,17 г
где 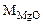 = 24,3 + 16 = 40,3 г/моль
= 24,3 + 16 = 40,3 г/моль
М 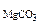 = 24,3 + 12 + 16·3 = 84,3 г/моль
= 24,3 + 12 + 16·3 = 84,3 г/моль
После прокаливания смесь состоит только из MgО
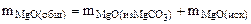
При взаимодействии продукта, полученного после прокаливания с ортофосфорной кислотой, протекает реакция
3MgO(общ.) + 2H3PO4 = Mg3(PO4)2 + 3H2O
Тогда реагирует по уравнению
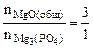 →
→ 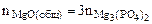
или
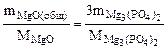
откуда 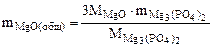
mMgO(общ) = 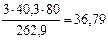 г
г
где М 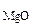 = 40,3 г/моль, М
= 40,3 г/моль, М 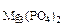 = 262,9 г/моль
= 262,9 г/моль
тогда
mMgO(исх) = mMgO(общ) – mMgO (из MgCO 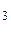 ) = 36,79 г – 7,17 г = 29,62 г
) = 36,79 г – 7,17 г = 29,62 г
Таким образом
mсмеси = mMgO(исх) + 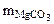 = 29,62 г + 15 г = 44,62 г
= 29,62 г + 15 г = 44,62 г
Состав исходной смеси
ω 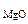 =
= 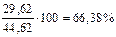 мас.
мас.
ω 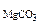 = 100 – 66,38 = 33,62% масс.
= 100 – 66,38 = 33,62% масс.
3. При взаимодействии 1,8 г технического карбоната кальция (мела) с HCl выделилось 400 см3 CO2, собранного над водным раствором NaHCO3 и измеренного при температуре 288 К и давлении 730 мм рт.ст. Давление паров воды при 288 К равно 12,79 мм рт.ст. Определить содержание СаСО3 в техническом карбонате кальция в процентах.
Дано: 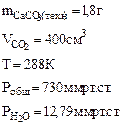  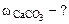 | РЕШЕНИЕ: 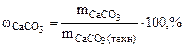 Так как, примеси, содержащиеся в техническом СаСО3 не взаимодействуют с HCl с образованием CO2, то массу чистого карбоната кальция ( Так как, примеси, содержащиеся в техническом СаСО3 не взаимодействуют с HCl с образованием CO2, то массу чистого карбоната кальция (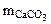 ) определяем по уравнению реакции (1.4): ) определяем по уравнению реакции (1.4): |
СаСО3 +2HCl=CaCl2 + H2O+CO2↑ (1.4)
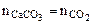
Или 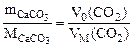 VM(CO2) = 22400 cм3/моль
VM(CO2) = 22400 cм3/моль
тогда 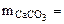
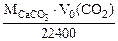 (1.5)
(1.5)
где 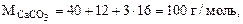
где 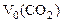 - объем выделившегося СО2, приведенный к нормальным условиям.
- объем выделившегося СО2, приведенный к нормальным условиям.
 Для определения
Для определения 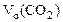 воспользуемся объединенным газовым законом:
воспользуемся объединенным газовым законом:
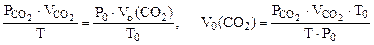
где 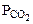 - парциальное давление СО2, так как СО2 собран над водным раствором NaHCO3, то
- парциальное давление СО2, так как СО2 собран над водным раствором NaHCO3, то
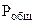 =
= 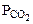 +
+ 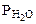 , тогда
, тогда
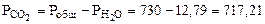 мм рт.ст.
мм рт.ст. 
Тo = 273 К,
Рo = 760 мм рт. ст.,
тогда 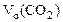 =
= 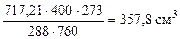
Определяем массу чистого СаСО3 по формуле (1.5):
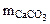 =
= 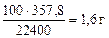 , тогда
, тогда
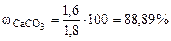
Ответ: содержание СаСО3 в меле 88,89%.
2. ЭКВИВАЛЕНТ. ЗАКОН ЭКВИВАЛЕНТОВ
УРОВЕНЬ А
1. Написать уравнения реакций взаимодействия хлорида железа (III) с гидроксидом натрия с образованием:
а) хлорида гидроксожелеза;
б) гидроксида железа (III).
 2015-06-05
2015-06-05 2654
2654








