В общем виде задача ставится так. Известны неравновесные количества (парциальные давления, концентрации) исходных веществ и их начальное состояние 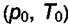 . В системе устанавливается равновесие при
. В системе устанавливается равновесие при
р = const или V= const. Надо определить равновесные концентрации или парциальные давления в системе и её конечную равновесную температуру. Поддержание постоянного объёма или постоянного давления в системе приводит к разным равновесным состояниям, однако методы расчёта в обоих случаях аналогичны. Если рассматривается изолированная система, то речь идёт о расчёте адиабатической температуры реакции.
В качестве наглядного примера рассмотрим задачу о расчёте адиабатической температуры высокотемпературного окисления углеводорода в воздухе и равновесного состава продуктов такого окисления. Процесс окисления и установления равновесия проведём в изолированной системе при р = 1 атм.
В наиболее часто встречающемся случае в исходной смеси содержится 4 элемента С, Н, О, N. В продуктах окисления представляют интерес обычно 11 компонент (веществ). Так как равновесие при высокотемпературном окислении сильно сдвинуто в сторону продуктов, то равновесной концентрацией углеводорода можно пренебречь. Ещё одной неизвестной величиной является адиабатическая температура реакции. Таким образом, имеется 12 неизвестных, для нахождения которых надо составить 12 уравнений.
|
|
|
Запишем брутто реакцию окисления
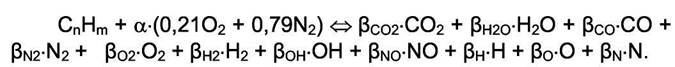
где 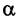 и
и 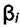 — стехиометрические коэффициенты. Концентрации других веществ, как показывает эксперимент и расчёт, пренебрежимо малы, и их можно не учитывать. Равновесные концентрации указанных веществ в продуктах окисления связаны реакциями между ними. Таких реакций может быть много. Но можно показать, что для системы состоящей из К компонентов и L элементов, количество независимых реакций и соответственно уравнений равновесия равно (К - L). Таким образом, для рассматриваемой системы из 11 компонентов и 4 элементов можно составить 7 независимых реакций, связывающих равновесные концентрации указанных веществ.
— стехиометрические коэффициенты. Концентрации других веществ, как показывает эксперимент и расчёт, пренебрежимо малы, и их можно не учитывать. Равновесные концентрации указанных веществ в продуктах окисления связаны реакциями между ними. Таких реакций может быть много. Но можно показать, что для системы состоящей из К компонентов и L элементов, количество независимых реакций и соответственно уравнений равновесия равно (К - L). Таким образом, для рассматриваемой системы из 11 компонентов и 4 элементов можно составить 7 независимых реакций, связывающих равновесные концентрации указанных веществ.
Вообще безразлично, какие реакции выбрать для расчёта. Важно только, чтобы они были независимы. Это означает, что операции суммирования или вычитания не должны приводить к получению другой
записанной реакции. Обычно расчёт равновесия продуктов высокотемпературного окисления выполняется по следующим реакциям:
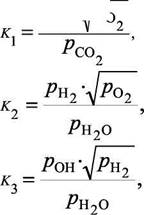 (1) СО2 <=> СО + 0,5О2, K=
(1) СО2 <=> СО + 0,5О2, K=
(2) Н2О «. Н2 + 0,5О2
(3) Н2О «ОН + 0,5Н2
(4)
(5)
(7)
Температурные зависимости констант равновесий (1) - (7) берутся из справочника. Таким образом, имеется 7 уравнений связывающих 11 парциальных давлений компонентов продуктов окисления.
|
|
|

|
Очевидно, что количество атомов элементов С, Н, О, N, содержащихся в 1 кг исходной смеси, должно равняться количеству атомов тех же элементов, содержащихся в 1 кг продуктов окисления. Это условие позволяет составить 4 уравнения баланса вещества.

|

|
Пусть в 1 кг исходной смеси содержится gН кг водорода, gС кг углерода, gО кг кислорода и gN кг азота, тогда балансные уравнения будут выглядеть так:
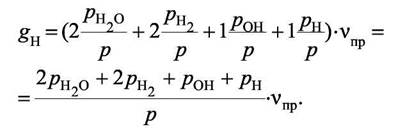
|
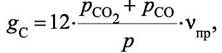
|
(9)
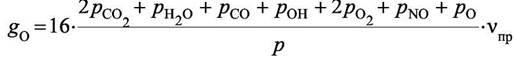
|
(10)
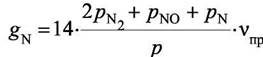
|
(11′)
 2015-07-04
2015-07-04 715
715








