| Метаболіт | Вміст, мкмоль на 1г сирої тканини | Метаболіт | Вміст, мкмоль на 1г сирої тканини |
| Глюкозо-6-фосфат | 0,039-0,049 | 3-Фосфогліцерат | 0,085-0,100 |
| Фруктозо-6-фосфат | 0,017-0,023 | 2-Фосфогліцерат | 0,010-0,016 |
| Фруктозо-1,6-дисфосфат | 0,010-0,017 | Фосфоенолпіруват | 0,035-0,097 |
| Діоксиацетонфосфат | 0,024 | Піруват | 0,120-0,190 |
| Гліцеральдегід-3-фосфат | 0,021-0,046 | Лактат | 1,26-1,70 |
Основним субстратом дихання нервової тканини є глюкоза. Цікаво відзначити, що в перерахунку на загальну масу головного мозку вміст глюкози в ньому становить біля 750 мг. За 1 хв окиснюється 75 мг глюкози. Отже, кількості глюкози, наявної в тканині головного мозку, могло б вистарчити лише на 10 хв життя людини. Тому основним субстратом дихання головного мозку є глюкоза крові, яка, очевидно, легко дифундує в тканину головного мозку.
За 1 хв мозок людини споживає у середньому 0,3 – 0,35 мкмоль глюкози. Її транспорт у клітини мозку здійснюють переносники: GLUT-1 (45 кДа) – в астроцити та олігодендроцити; GLUT-5 (55 кДа) – у клітини мікроглії, у нейронах виявлений специфічний високоактивний транспортер GLUT-3 (55 кДа). Підраховано, що понад 90 % глюкози у мозку окиснюється до СО2 і Н2О за участі циклу трикарбонових кислот. Особливістю цього процесу є той факт, що найповільніше відбувається цитратсинтазна реакція, навіть незначне зниження активності цитратсинтази призводить до порушення синтезу нейромедіатора ацетилхоліну та блокує холінергічну передачу (рис. 18.2)
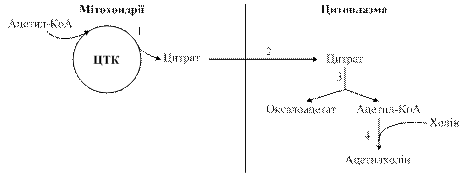
Рис. 18.2. Участь цитратсинтазної реакції в біосинтезі ацетилхоліну: 1 – цитратсинтаза, 2 – переносник трикарбонових кислот, 3 – цитратліаза, 4 – холінацетилтрансфераза.
За фізіологічних умов роль пентозофосфатного шляху окиснення глюкози в нервовій тканині невелика, цей шлях відбувається в усіх клітинах головного мозку. Утворена відновлена форма НАДФ (НАДФН2) використовується для синтезу жирних кислот і стероїдів.
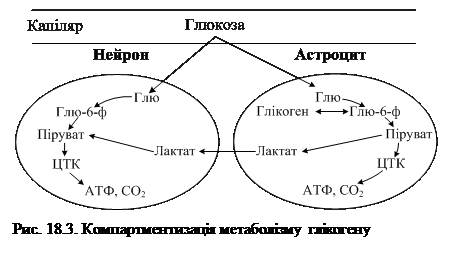
Між глюкозою і глікогеном нервової тканини є тісний зв’язок, який виражається в тому, що при недостатньому надходженні глюкози з крові глікоген головного мозку є джерелом глюкози, а глюкоза при її надлишку – вихідним матеріалом для синтезу глікогену. Шляхи утилізації глюкози дещо різняться в нейронах і астроцитах: у нейронах глюкоза швидко окиснюється в реакціях аеробного гліколізу та ЦТК, а в астроцитах частина цього моносахарида витрачається на синтез глікогену (рис. 18.3). Швидкість процесу залежить від концентрації вихідного субстрату – глюкозо-6-фосфату.
За умов посилення енергозатрат, при гіпоглікемії утворення глікогену сповільнюється, проте посилюється при глибокому наркозі.
 Розпад глікогену в нервовій тканині відбувається шляхом фосфоролізу за участі цАМФ. Кінетичні та регуляторні властивості ензимів метаболізму глікогену в мозку відрізняються від їх властивостей у інших тканинах. У мозку дорослої людини гранули глікогену, а також глікогенфосфорилаза виявлені лише в астроцитах.
Розпад глікогену в нервовій тканині відбувається шляхом фосфоролізу за участі цАМФ. Кінетичні та регуляторні властивості ензимів метаболізму глікогену в мозку відрізняються від їх властивостей у інших тканинах. У мозку дорослої людини гранули глікогену, а також глікогенфосфорилаза виявлені лише в астроцитах.
Поряд з аеробним метаболізмом вуглеводів мозкова тканина здатна до інтенсивного анаеробного гліколізу. Значення цього явища поки що недостатньо зрозуміле, тому що гліколіз, як джерело енергії у головному мозку, ні в якому разі не може зрівнятися за ефективністю з тканинним диханням.
Мінеральні речовини. Натрій, калій, мідь, залізо, кальцій, марганець і магнійрівномірно розподілені в сірій і білій речовинах головного мозку. Вміст фосфатів у білій речовині вищий, ніж у сірій.
Кількісне співвідношення неорганічних аніонів і катіонів у нервовій тканині свідчить про дефіцит аніонів. Розрахунок показує, що для покриття дефіциту аніонів потрібно було б у 2 рази більше мембран, ніж їх є в нервовій тканині. Прийнято вважати, що дефіцит аніонів покривається за рахунок ліпідів. Цілком можливо, що участь ліпідів в іонному балансі – одна з функцій головного мозку.
18.1.1. Особливості енергозабезпечення нервової тканини. На частку головного мозку припадає 2 – 3 % усієї маси тіла людини. У цей же час споживання кисню головним мозком у стані фізичного спокою досягає 20 – 25 % від загального споживання його всім організмом, а в дітей у віці до 4 років мозок споживає 50 % кисню, який утилізується всім організмом.
Встановлено, що 100 г тканини за 1 хв споживає 3,7 мл кисню, тоді як головний мозок (1 500 г) – 55,5 мл.
Після дисоціації оксигемоглобіну кисень дифундує під впливом концентраційного градієнта з плазми крові в міжклітинну рідину, а потім потрапляє в нейрони та гліальні клітини. Найінтенсивніше окиснювальні процеси перебігають у корі головного мозку, таламусі, хвостатому ядрі, тоді як у корі мозочка, чорній субстанції, а також у білій речовині використання кисню значно менше. В цілому газообмін нервової тканини значно вищий, ніж газообмін інших тканин, зокрема він перевищує газообмін м’язової тканини майже в 20 разів.
Постійне і безперервне надходження кисню та глюкози з кровоносного русла в нервову тканину – необхідна умова енергетичного забезпечення нейронів, адже основний шлях отримання енергії – лише аеробний розпад глюкози, вона є майже єдиним енергетичним субстратом, який надходить у нервову тканину і може використовуватися її клітинами для утворення АТФ. Проникнення глюкози в тканину мозку не залежить від впливу інсуліну, котрий не проникає через ГЕБ (вплив інсуліну проявляється лише на периферійних нервах).
Енергія АТФ у нервовій тканині використовується нерівномірно в часі. Так само, як і скелетні м’язи, нервова тканина характеризується різкими перепадами в використанні енергії: зростання енергозатрат відбувається при дуже швидкому переході від сну до стану бадьорості. Тому існує ще одна особливість енергозабезпечення нервової тканини – синтез креатинфосфату:
Креатинфосфат + АДФ ↔ Креатин + АТФ
Напрям цієї реакції залежить від співвідношення АТФ/АДФ у нервовій тканині. Під час сну накопичується креатинфосфат, тоді як перехід до стану бадьорості призводить до різкого зменшення концентрації АТФ і рівновага реакції зміщується вліво, тобто утворюється АТФ.
на забезпечення базових процесів життєдіяльності, які відбуваються в будь-якій тканині, мозок витрачає приблизно 25 % макроергічних сполук, а решта – 75 % макроергів витрачається на виконання специфічних, властивих тільки нервовій тканині функцій (табл. 18.3).
Таблиця.18.3. Основні енергозалежні процеси, що лежать в основі специфічних функцій мозку
| Функції | Біохімічні реакції | Енерго-затрати, % |
| Проведення нервових імпульсів із подальшим відновленням іонної асиметрії | К+, Na+-АТФазна реакція | До 40 |
| Функціонування синаптичних структур | Синтез специфічних білків, ліпо- і глікопротеїдних комплексів синаптичних структур, синтез і метаболізм медіаторів, збереження, транспорт, виведення медіаторів, функціонування рецепторів | 30 – 35 |
| Зберігання та перетворення інформації (нейрологічна пам'ять) | Синтез специфічних білків, нейропептидів, нуклеїнових кислот, ліпо- і глікопротеїдних комплексів | Біля 20 |
| Аксональний і ретроградний потік | Гідроліз АТФ при функціонуванні скоротливих білків сімейств нейроміозинів, кінезинів, динеїнів | 2 – 3 |
| Підтримання просторової орієнтації | Фосфорилування структурних і скоротливих білків | 1 – 2 |
Наведені дані пояснюють, наскільки велика залежність функціональної активності нервової тканини від інтенсивності енергетичного обміну та чому всі структури нервової системи, перш за все, головний мозок, дуже чутливі до недостатності кисню.
Фатальною виявляється ситуація, коли в результаті порушення кровопостачання одночасно знижується або припиняється надходження в мозок не лише кисню, а й глюкози. Ушкоджувальну дію гіпоксії на клітини мозку умовно можна поділити на два етапи. перший пов'язаний із енергетичним дефіцитом внаслідок порушення окиснювальних процесів у мітохондріях та активуванням глутаматергічних нейронів. У результаті знижується рівень АТФ і інших макроергічних сполук, накопичується глутамат у міжклітинному просторі, деполяризуються клітинні мембрани, виникає ацидоз. Для другого етапу характерне різке порушення гомеостазу іонів кальцію, що спричинює активування низки біохімічних механізмів, пов’язаних із деструкцією клітинних елементів.
 2015-07-21
2015-07-21 620
620







