ЭНТРОПИЯ, показатель случайности или неупорядоченностистроения физической системы. В ТЕРМОДИНАМИКЕ энтропия выражает количество тепловой энергии,пригодной для совершения работы: чем энергии меньше, тем выше энтропия. В масштабах Вселеннойэнтропия возрастает. Извлечь энергию из системы можно только путем перевода ее в менее упорядоченноесостояние.
S = k lnW, где k – коэффициент пропорциональности, k = 1,38 ⋅10−23 Дж/ кг – постоянная Больцмана.
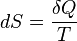 ,
,
где 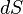 — приращение энтропии;
— приращение энтропии; 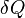 — минимальная теплота, подведённая к системе;
— минимальная теплота, подведённая к системе; 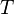 — абсолютная температура процесса.
— абсолютная температура процесса.
Энтропия есть величина аддитивная, т. е. энтропия термодинамической системы равна сумме энтропий всех её частей.
Энтропия - функция состояния. Если процесс проводят вдоль адиабат, то энтропия системы не меняется. Значит адиабаты -это одновременно и изоэнтропы.
Одно из важнейших свойств энтропии заключается в том, что энтропия замкнутой (т.е. теплоизолированной) макросистемы не уменьшается - она либо возрастает, либо остается постоянной. Если же система не замкнута, то ее энтропия может как увеличиваться, так и уменьшаться.
|
|
|
Для любой термодинамической системы состояния с наименьшей энтропией и наименьшей температурой совпадают. С приближением температуры к абсолютному нулю энтропия перестаёт зависеть от температуры и приближается к определённому постоянному значению, которое можно положить равным нулю.
Энтропия изолированной системы в состоянии термодинамического равновесия имеет максимальное значение, т. е. для равновесия изолированной системы необходимо и достаточно, чтобы при всех возможных изменениях её состояния вариация энтропии дS системы не была положительной.
В замкнутой и адиабатически изолированной макроскопической системе наиболее вероятным является процесс, сопровождающийся возрастанием энтропии
 2015-07-14
2015-07-14 6216
6216








