Решение: В исследуемом растворе №1 находится катион 5 аналитической группы, так как осадок бурого цвета, который не растворился в избытке NaOH. Это Fe3+.
В исследуемом растворе №2 находится катион 6 аналитической группы, так как осадок голубого цвета, который не растворился в избытке NaOH. Это Cu2+.
В исследуемом растворе №3 находится катион 4 аналитической группы, так как осадок серо-зеленого цвета, который растворился в избытке NaOH. Это Сr3+.
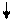 Проба 1: FeCI3 + 3NaOH = FeOH)3 + 3NaCI
Проба 1: FeCI3 + 3NaOH = FeOH)3 + 3NaCI
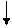 Fe3+ + 3CI- + 3Na+ + 3OH- = Fe(OH)3 + 3 Na+ + 3CI-
Fe3+ + 3CI- + 3Na+ + 3OH- = Fe(OH)3 + 3 Na+ + 3CI-
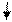 Fe3+ + 3OH- = Fe(OH)3
Fe3+ + 3OH- = Fe(OH)3
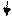 Проба 2: CuSO4 + 2NaOH → Cu(OH)2 + Na2SO4
Проба 2: CuSO4 + 2NaOH → Cu(OH)2 + Na2SO4
 Cu2+ + SO42- + 2Na+ + 2OH- → Cu(OH)2 + 2Na+ SO42-
Cu2+ + SO42- + 2Na+ + 2OH- → Cu(OH)2 + 2Na+ SO42-
 Cu2+ + 2OH- → Cu(OH)2
Cu2+ + 2OH- → Cu(OH)2
 Проба 3: CrCI3 + 3NaOH = Cr(OH)3 + 3 NaCI
Проба 3: CrCI3 + 3NaOH = Cr(OH)3 + 3 NaCI
 Cr3+ + 3 CI- + 3Na+ + 3OH- = Cr(OH)3 + 3 Na+ + 3CI-
Cr3+ + 3 CI- + 3Na+ + 3OH- = Cr(OH)3 + 3 Na+ + 3CI-
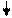 Cr3+ + 3OH- = Cr(OH)3
Cr3+ + 3OH- = Cr(OH)3
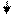 Cr(OH)3 + 3NaOH = Na3[Cr(OH)6]
Cr(OH)3 + 3NaOH = Na3[Cr(OH)6]
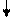
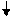 Cr(OH)3 + 3Na + + 3OH- = 3Na+ + [Cr(OH)6] 3-
Cr(OH)3 + 3Na + + 3OH- = 3Na+ + [Cr(OH)6] 3-
Cr(OH)3 + 3OH- = [Cr(OH)6] 3-
 2015-08-12
2015-08-12 869
869








