Окислительно-восстановительные взаимодействия связаны с переносом электронов между реагирующими частицами – молекулами, ионами или комплексами. Окислением называется реакция, связанная с потерей электрона реагирующей частицей, восстановлением – реакция, связанная
с приобретением электронов. Частицу, отдающую электрон, называют восстановителем, а принимающую электроны – окислителем. Молярное отношение между окисляющимся веществом и восстанавливающимся веществом должно быть таково, что число электронов, отданных одним веществом, равно числу электронов, принятых другим. Это следует учитывать при составлении окислительно-восстановительных реакций. Любую реакцию можно представить, как сумму полуреакций.
5Fe2+ + MnO4- + 8H+ → 5Fe3+ + Mn2+ + 4H2O
5 Fe2+ - e → Fe3+ 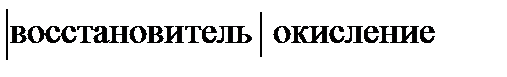
1 MnO4- + 5 e + 8H+ → Mn2+ + 4H2O 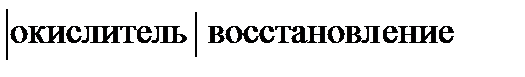
Мерой движущей силы полуреакции является электродный потенциал окислительно-восстановительной системы, который определяется как ЭДС гальванического элемента, составленного из исследуемой ОВ – системы в паре со стандартным водородным электродом, потенциал которого принят за 0,00 В при любой температуре.
Например:
(+) Cu | Cu2+ || H+ | H2 (Pt) (–) Cu2+ + 2 е «Cu0 H2 – 2 е «2H+
(–) Zn | Zn 2+ || H+ | H2 (Pt) (+) Zn 0– 2 е «Zn 2+
2H+ + 2 е «H2
Под равновесным электродным потенциалом понимают потенциал, устанавливающийся на металлическом электроде в растворе своей соли (на инертном электроде, погруженном в раствор, содержащий ОВ – систему)
в отсутствие электрического тока.
Стандартный электродный потенциал Е0 – это равновесный потенциал, который данная окислительно-восстановительная система имеет в том случае, когда все компоненты, участвующие в полуреакции, находятся в стандартном состоянии, т.е. их активности равны единице (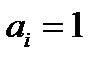 ). Мы будем считать, что состояние иона близко к стандартному, если его концентрация составляет 1 моль/дм3. (Потенциалы, измеренные в паре со стандартным водородным электродом при активности ионов равной 1 и температуре 25°С, называются стандартными электродными потенциалами и обозначаются
). Мы будем считать, что состояние иона близко к стандартному, если его концентрация составляет 1 моль/дм3. (Потенциалы, измеренные в паре со стандартным водородным электродом при активности ионов равной 1 и температуре 25°С, называются стандартными электродными потенциалами и обозначаются 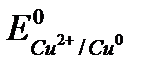 ,
, 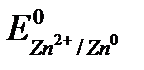 (прил. 6).
(прил. 6).
По соглашению Международного союза по теоретической и прикладной химии (IUPAC) термин «электродный потенциал» относится исключительно
к полуреакциям, записанным в форме реакции восстановления.
Например:
Cu2+ + 2 е «Cu0 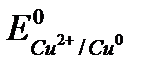 = + 0,337 В.
= + 0,337 В.
Zn 2+ + 2 е «Zn0 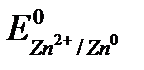 = – 0,76 В.
= – 0,76 В.
За знак электродного потенциала принимают действительный знак изучаемого электрода относительно стандартного водородного электрода, который указывает направление самопроизвольного протекания процесса.
Так, положительный знак медного электрода означает, что реакция
Cu2+ + Н2 «Cu0 + 2Н+
при обычных условиях протекает в сторону выделения металлической меди (слева направо). С другой стороны, отрицательный знак электродного потенциала цинка означает, что аналогичная реакция
Zn 2+ + Н2 «Zn0 + 2Н+
самопроизвольно протекает в сторону растворения металлического цинка (справа налево).
Зависимость между величиной электродного потенциала полуреакции
и концентрацией потенциалопределяющих ионов (компонентов ОВ – системы) выражается уравнением Нернста.
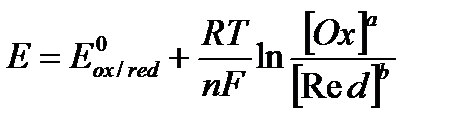 (24)
(24)
где Е – потенциал, В;
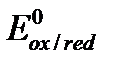 – стандартный электродный потенциал, В;
– стандартный электродный потенциал, В;
R – газовая постоянная, 8,314 Дж/(моль·К);
Т – абсолютная температура, К (273 + t °С);
n – число электронов, участвующих в реакции;
F – число Фарадея, 96485,3399 ± 0,0024 Кл/моль;
[ Ox ], [ Red ] – соответственно равновесные концентрации окисленной
и восстановленной форм;
a, b – стехиометрические коэффициенты.
При температуре 25° С и переходе к десятичным логарифмам получаем уравнение в виде
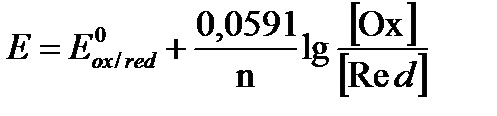 . (25)
. (25)
В процессе титрования происходит изменение потенциала титруемой системы, так как постоянно меняется соотношение 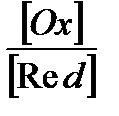 , однако после каждой порции добавленного титранта в растворе устанавливается состояние равновесия (ЕOx = ERed = E сист). Наиболее резкое изменение потенциала происходит вблизи точки эквивалентности.
, однако после каждой порции добавленного титранта в растворе устанавливается состояние равновесия (ЕOx = ERed = E сист). Наиболее резкое изменение потенциала происходит вблизи точки эквивалентности.
 2015-08-13
2015-08-13 776
776








