Термодинамическое равновесие системы характеризуется термодинамическими потенциалами. Все термодинамические параметры системы − давление p, объем V, температура T, и др. − могут быть получены как частные производные термодинамических потенциалов.
Основное уравнение термодинамики для равновесных процессов
| TdS = dU + pdV, | (13.1) |
где U – внутренняя энергия системы, S – ее энтропия.
Основное уравнение термодинамики связывает пять физических величин: температуру, давление, объем, энтропию и внутреннюю энергию (T, p, V, S, U). Для каждой пары из них существует термодинамический потенциал.
Если за независимые переменные в уравнении (13.1) принять энтропию и объем (S и V), то для определения остальных величин необходимо задать зависимость внутренней энергии от энтропии и объема. Перепишем (13.1) как 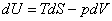 , отсюда dU является полным дифференциалом, и остальные параметры (температура и давление) можно определить как:
, отсюда dU является полным дифференциалом, и остальные параметры (температура и давление) можно определить как:
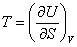 ; ; 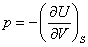 , , | (13.2) |
где индексы V и S означают, что система находится при постоянных объеме и энтропии соответственно.
Рассмотрим другие варианты. Пусть независимыми переменными являются температура (T) и объем (V). Термодинамическим потенциалом в этом случае служит свободная энергия Гельмгольца F:
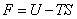 ; ; 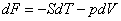 ; ; 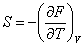 ; ; 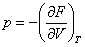 . . | (13.3) |
Для независимых переменных T и p термодинамическим потенциалом является энергия Гиббса G:
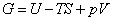 ; ; 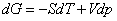 ; ; 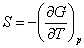 ; ; 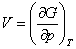 . . | (13.4) |
Энтальпия 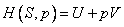 , также один из термодинамических потенциалов.
, также один из термодинамических потенциалов.
Часто в реальных термодинамических системах приходится иметь дело с переменным числом частиц. Внутренняя энергия такой системы может меняться за счет изменения числа частиц какого-либо сорта i на величину 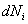 . Тогда основное уравнение термодинамики для таких систем принимает вид
. Тогда основное уравнение термодинамики для таких систем принимает вид
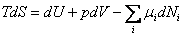 ; ; 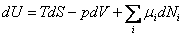 . . | (13.5) |
Величина 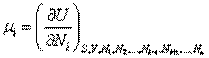 называется химическим потенциалом i-го сорта частиц и имеет смысл энергии, приходящейся на одну частицу. Для систем с переменным числом частиц в выражения для дифференциалов свободной энергии и потенциала Гиббса также будет входить дополнительный член
называется химическим потенциалом i-го сорта частиц и имеет смысл энергии, приходящейся на одну частицу. Для систем с переменным числом частиц в выражения для дифференциалов свободной энергии и потенциала Гиббса также будет входить дополнительный член 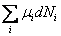 . Следовательно, химический потенциал
. Следовательно, химический потенциал 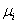 можно получить дифференцированием любого из термодинамических потенциалов по числу частиц
можно получить дифференцированием любого из термодинамических потенциалов по числу частиц
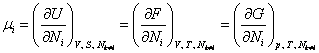 . . | (13.6) |
Все термодинамические потенциалы являются экстенсивными величинами, т. е. они пропорциональны количеству вещества. Величины, не зависящие от количества вещества, называются интенсивными, к ним, например, относятся плотность, концентрация, температура. Экстенсивные величины выражаются математически однородными функциями, и для них справедлива теорема Эйлера об однородных функциях
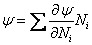 , , | ||
где 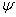 − экстенсивная величина. Применяя эту теорему к термодинамическому потенциалу Гиббса, с учетом (13.6) получим − экстенсивная величина. Применяя эту теорему к термодинамическому потенциалу Гиббса, с учетом (13.6) получим 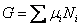 . . | ||
| Термодинамические потенциалы, взятые как функции своих естественных переменных, являются характеристическими функциями системы. Это означает, что любое термодинамич. свойство (сжимаемость, теплоемкость и т. п.) м. б. выражено соотношением, включающим только данный термодинамический потенциал, его естественные переменные и производные термодинамический потенциал разных порядков по естественным переменным. В частности, с помощью термодинамический потенциал можно получить уравнения состояния системы. | ||
Важными свойствами обладают производные термодинамических потенциалов. Первые частные производные по естественным экстенсивным переменным равны интенсивным переменным, например:
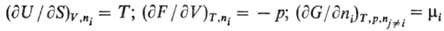
И наоборот, производные по естественным интенсивным переменным равны экстенсивным переменным, например: 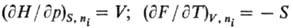
 2015-08-12
2015-08-12 2463
2463
