Залежність між трьома параметрами стану називають рівнянням стану.
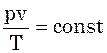
R – питома газова стала, 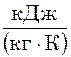 .
.
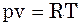 (1) рівняння Клапейрона-Мен-делеєва.
(1) рівняння Клапейрона-Мен-делеєва.
R – це величина, яка має однакове зна-чення для всіх термодинамічних станів да-ного газу. Газова стала має такий фізичний зміст: це потенціальна енергія тиску робо-чого тіла, яка припадає на 1К його темпе-ратури.
Продиференціюємо рівняння (1):
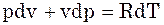 ;
;
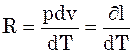 ,
, 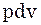 – це робота.
– це робота.
Фізичний зміст питомої газової ста-лої R полягає в тому, що це є робота, яку виконує 1 кілограм газу під час свого розрі-дження в ізобарному процесі під час нагрі-вання на 1 Кельвін.
R=pdv/T
Знайдемо значення газової сталої для нормальних умов (тиск 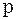
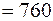
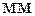
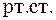 ).
).
1 мм рт. ст.=133,333 Па
р=101325 Па
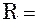
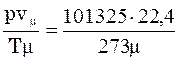 ,
,
де 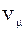 – об’єм 1 кмоля газу за нормаль-них умов.
– об’єм 1 кмоля газу за нормаль-них умов.
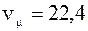
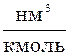 .
.
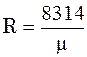
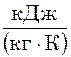 ;
;
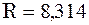
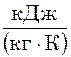 .
.
pvm=mRT,
m – маса робочого тіла.
vm=V;
pV=mRT (2) для m кг газу
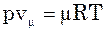 ,
,
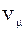 – об‘єм 1 кмоля газу.
– об‘єм 1 кмоля газу.
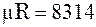
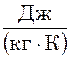 ,
,
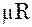 – універсальна газова стала – це величина, яка має однакове значення для всіх газів і усіх станів.
– універсальна газова стала – це величина, яка має однакове значення для всіх газів і усіх станів.
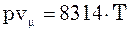 (3) – рівняння Клапейро-на-Менделеєва.
(3) – рівняння Клапейро-на-Менделеєва.
Якщо ми маємо n кмоль газу:
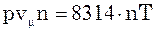
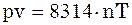 (4) – для n кмолей газу.
(4) – для n кмолей газу.
 2015-09-06
2015-09-06 886
886








