Мольная доля молекулярной и ионной форм органического реагента в растворе зависит от рН раствора.
Оптическая плотность раствора слабой кислоты при заданных значениях рН и длины волны проходящего через раствор излучения может быть выражена уравнением:
 , (166)
, (166)
где 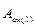 – оптическая плотность раствора, содержащего обе формы органического реагента;
– оптическая плотность раствора, содержащего обе формы органического реагента;
 и
и 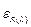 – коэффициенты погашения молекулярной и ионной форм органического реагента при выбранной длине волны излучения,
– коэффициенты погашения молекулярной и ионной форм органического реагента при выбранной длине волны излучения,
дм3×моль-1×см-1;
с – сумма молярных концентраций всех форм органического реагента в растворе, моль/дм3;
х – мольная доля анионной формы органического реагента.
Подставив в выражение (167) величины с и х:
 (167)
(167)
и решая уравнение (169) относительно х, находим:
 (168)
(168)
Комбинируя уравнения (168) и (170), получим:
 . (169)
. (169)
Решаем уравнение (171) относительно K:
 . (170)
. (170)
Графический метод
На кривой зависимости оптической плотности раствора (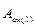 ), измеренной при длине волны, соответствующей максимальному поглощению недиссоциированной формы индикатора, от рН раствора наблюдается резкое измерение значений оптической плотности раствора в области перехода от одной формы кислоты к другой (область перехода окраски индикатора) (рисунок 1). Если измерить оптическую плотность растворов при длине волны, соответствующей максимальному поглощению диссоциированной формы индикатора, то на кривой зависимости
), измеренной при длине волны, соответствующей максимальному поглощению недиссоциированной формы индикатора, от рН раствора наблюдается резкое измерение значений оптической плотности раствора в области перехода от одной формы кислоты к другой (область перехода окраски индикатора) (рисунок 1). Если измерить оптическую плотность растворов при длине волны, соответствующей максимальному поглощению диссоциированной формы индикатора, то на кривой зависимости
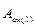 = f (pH) скачок оптической плотности будет в том же диапазоне рН, но в обратную сторону (рисунок 2).
= f (pH) скачок оптической плотности будет в том же диапазоне рН, но в обратную сторону (рисунок 2).
Перпендикуляр, опущенный из точки, соответствующей степени диссоциации реагента a = 50 %, (середина участка крутого подъема или спада оптической плотности) на ось дает значение р K, так как подстановка выражения:
 (171)
(171)
в уравнение (170) приводит к равенству:
lg K = lg[H+] и – lg K = pH. (172)
A
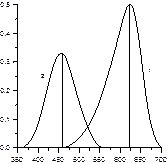 l, нм
l, нм
| A
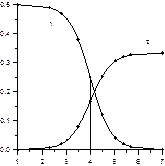 рН
рН
|
| Рисунок 1 – Спектры молекулярной (1) и ионной (2) форм индикатора | Рисунок 2 – Зависимость оптической плотности раствора индикатора от рН при l = 620 нм (1) и l = 460 нм (2) |
 2015-10-22
2015-10-22 792
792








