Курсовая работа
Расчет горения вещества.
1. Уравнение реакции горения.
2. Расчет расхода воздуха на горение.
2.1. 
2.2. 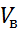
3. Расчет объема продуктов сгорания.
4. Расчет теплоты горения.
5. Расчет температуры горения.
Дано:
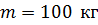

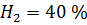

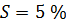
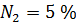
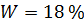
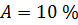
Условия:


Уравнение реакции горения
Для расчетов необходимо составить стехиометрические уравнения реакции горения веществ в воздухе. При этом учитывается, что на один объем кислорода в воздухе приходится 79/21 = 3,76 объема азота, поэтому окислитель, воздух, в записи уравнений представляется как 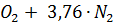 .
.
Составим уравнения химических реакций:
а) 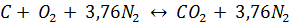
б) 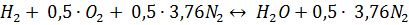
в) 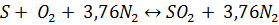
Учитывая то, что расчет производится на 1 моль или 1 м² горючего вещества, в уравнении реакции коэффициент перед символом горючего вещества не ставят. В результате в уравнениях горения перед символами веществ могут быть выствлены дробные стехиометрические коэффициенты.
Расчет расхода воздуха на горение.
2.1. 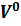
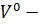 минимальное количество воздуха, необходимое для полного сгорания единицы массы (кг) или объема (м³) горючего вещества, называется теоретически необходимым.
минимальное количество воздуха, необходимое для полного сгорания единицы массы (кг) или объема (м³) горючего вещества, называется теоретически необходимым.
Для того, чтобы провести расчет затрат воздуха на горение сложной смеси химических соединений необходимо методами аналитической химии определить химический состав данной смеси.
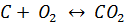
12кг+32кг = 44 кг

4кг + 32кг= 36кг
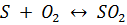
32кг+32кг=64кг
Если для сгорания 12 кг углерода требуется 32 кг кислорода, то для 0,01 кг углерода, т.е. 1% (массовый) его, потребуется кислорода 0,01·32/12=0,01·8/3 кг, для водорода соответственно потребуется 0,01·32/4=0,01·8 кг и для серы - 0,01·32/32=0,01 кг кислорода.
Для полного сгорания 1 кг горючего вещества потребуется кислорода,кг:
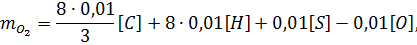
где 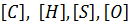 - содержание углерода, водорода, серы и кислорода в горючем веществе, % (мас.).
- содержание углерода, водорода, серы и кислорода в горючем веществе, % (мас.).
На вычисленное количество кислорода в воздухе приходится в 77/23 раза больше азота. Сумма азота и кислорода составляет массу воздуха 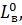 кг, необходимую для горения 1 кг вещества:
кг, необходимую для горения 1 кг вещества:

После преобразования получим:
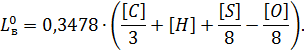
Чтобы выразить количество воздуха в объемных единицах, нужно правую часть выражения разделить на массу 1 м³ воздуха при нормальных условиях, т.е. на 1,293 кг/м³. Получим:
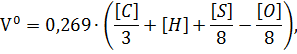
Подставим наши значения:
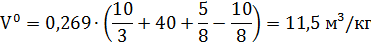
Для сгорания 100 кг заданного вещества потребуется:
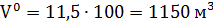
2.2. 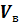
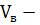 количество воздуха необходимое для сгорания веществ при заданных условиях.
количество воздуха необходимое для сгорания веществ при заданных условиях.

где T - заданная температура газов, К; p - заданное давление, Па.
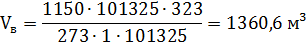
 2018-01-21
2018-01-21 808
808







