Химическая кинетика - раздел химии, изучающий скорости химических реакций.
Фазой называется часть системы, отделенная от других ее частей поверхностью раздела, при переходе через которую свойства изменяются скачком.
Скорость химической реакции – число элементарных актов реакции, происходящий в единицу времени, в единице объема (гомогенная реакция) или на единице поверхности (гетерогенная реакция) раздела фаз.
Мера скорости химической реакции – количество вещества, вступившего в реакцию или образовавшегося при реакции за единицу времени в единице объема системы или на единице поверхности раздела фаз.
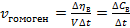 ;
; 
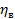 - число молей какого- либо из получающихся при реакции веществ; V – объем системы; t – время; S – площадь поверхности фазы, на которой протекает реакция;
- число молей какого- либо из получающихся при реакции веществ; V – объем системы; t – время; S – площадь поверхности фазы, на которой протекает реакция; 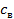 – молярная концентрация данного вещества.
– молярная концентрация данного вещества.
Средняя скорость реакции при определенной температуре равна изменению концентрации одного из реагентов или одного из продуктов за единицу времени.
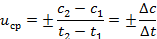
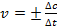 – мгновенная скорость реакций.
– мгновенная скорость реакций.
|
|
|
Скорость химической реакции зависит от природы и концентрации реагентов, давления(для газов), температуры, присутствия катализатора, наличие примесей, степень измельчения, среды.
Закон действующих масс: скорость химических реакций пропорциональна концентрации реагирующих веществ, возведенных в степень их стехиометрических коэффициентов.
Для гомогенных реакций: 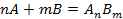
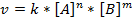
k- константа скорости; [ ] – молярная концентрация.
Величина k зависит от природы реагирующих веществ, от температуры и присутствия катализатора, но не зависит от концентрации реагирующих веществ.
Физический смысл k: если [A]=[B]=1 моль/л, то k=v – это скорость реакции в момент, когда концентрации реагирующих веществ равны единице.
Для гетерогенных реакций в уравнении закона действующих масс входят концентрации только тех веществ, которые находятся в газовой форме или в растворе. Концентрация твердых веществ представляет собой постоянную величину и поэтому входит в константу скорости. Скорость любого гетерогенного процесса возрастает при увеличении поверхности контакта фаз. Для этого используют измельчение твердой фазы.
 2018-01-21
2018-01-21 3264
3264
