СЕВМАШВТУЗ
Кафедра «Инженерной защиты окружающей среды и реновации техники».
МЕТОДИЧЕСКОЕ УКАЗАНИЕ
по выполнению лабораторной работы №1
«Поверхностные явления. Адсорбция»
по дисциплине «Химия»
Индекс: 33.02.00 о.ф.о. 2003г.
2.4.5.
Количество часов,
планируемых на работу – 4 часа.
Северодвинск
2001г.
I. ЦЕЛЬ РАБОТЫ:
Качественно проследить адсорбцию нескольких слабоокрашенных растворов и возможность обратного процесса десорбции; избирательной адсорбции.
II. РАБОЧЕЕ ЗАДАНИЕ:
Проделать опыт и проверить адсорбционную способность угля. Ответить на контрольные вопросы.
III. ОБЩИЕ СВЕДЕНИЯ:
Явление самопроизвольного поглощения вещества на поверхности раздела называется адсорбцией. Вещество, на поверхности которого происходит адсорбция, называется адсорбентом, а вещество, которое поглощается, адсорбируется - адсорбатом.
Адсорбцию обозначают буквой Г, а ее величину принято выражать количеством вещества на единицу поверхности моль/м2 или массы моль/кг адсорбента (когда поверхность адсорбента неизвестна, например пористые твердые тела), тогда величину адсорбции можно представить как:
 или
или  , где
, где
χ-количество адсорбируемого вещества
m- масса адсорбента
S- величина поверхности адсорбента
Адсорбция может проходить на границе раздела жидкость – газ, жидкость – жидкость, твердое тело – раствор, твердое тело – газ.
Адсорбция на границе жидкость – газ.
Поверхностное натяжение в большинстве случаев отличается от поверхностного натяжения чистого растворителя. При растворении в воде неорганических веществ (NaCI, KOH и т.п.) поверхностное натяжение несколько увеличивается, прибавление других веществ (например, сахар) не изменяет поверхностного натяжения воды. Растворение некоторых веществ органического происхождения приводит к значительному уменьшению поверхностного натяжения воды.
Вещества, понижающие поверхностное натяжение растворителя называются поверхностно-активными веществами (ПАВ). Примером ПАВ в водных растворах могут служить органические соединения: жирные кислоты, соли этих кислот, высокомолекулярные спирты, амины и т.д. в их молекулах одновременно содержатся полярные группы (-COOH, -OH, -NH2 и т.д.) и неполярная углеводородная цепь. Такие молекулы называются дифильными, т.е. обладающие двойственным сродством и с полярной (гидрофильной) и неполярной (гидрофобной) фазами. Например, молекула уксусной кислоты состоит из неполярного радикала CH3 и полярной группы COOH. Схематично дифильные группы обозначают в виде «головастика» ─ О, у которого чертой обозначена углеводородная часть (неполярная), а кружком полярная группа. Дифильные молекулы, попадая на границу раздела фаз, определенным образом ориентируются: полярная часть молекулы к полярной фазе, неполярная - к неполярной. Существует уравнение, связывающее величину адсорбции на границе жидкость – газ не только с температурой Т и с концентрацией С, но и с поверхностным натяжением. Это уравнение Гиббса:
 ,
,
где 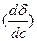 - поверхностная активность, для поверхностно активных веществ с увеличением концентрации
- поверхностная активность, для поверхностно активных веществ с увеличением концентрации 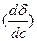 <0, поэтому Г <0.
<0, поэтому Г <0.
 2017-11-01
2017-11-01 268
268







