ЛИПИДЫ
К липидам относятся органические вещества, многие из которых являются сложными эфирами жирных высокомолекулярных кислот и многоатомных спиртов, – это жиры, фосфатиды, воска, стероиды, жирные высокомолекулярные кислоты и др.
Липиды находятся главным образом в семенах растений, ядрах орехов, а в животных организмах – в жировой и нервной тканях, особенно в мозгу животных и человека.
Природные жиры представляют собой смеси сложных эфиров трёхатомного спирта глицерина и высших карбоновых кислот, т.е. смеси глицеридов этих кислот.
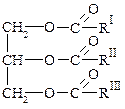
Общая формула жира:
α
β
α1,
где RI RII RIII – углеводородные радикалы высших жирных кислот нормального строения с чётным числом углеродных атомов. В состав жиров могут входить остатки как насыщенных, так и ненасыщенных кислот.
Насыщенные кислоты:
С15H31COOH – пальмитиновая;
С17Н35СООН – стеариновая;
С3Н7СООН – масляная (содержится в сливочном масле) и др.
Ненасыщенные кислоты:
С17Н33СООН – олеиновая;
С17Н31COOH – линолевая;
С17Н29СООН – линоленовая и др.
Получают жиры из природных источников животного и растительного происхождения.
Физические свойства жиров обусловлены кислотным составом. Жиры, содержащие преимущественно остатки насыщенных кислот, – твёрдые или мазеобразные вещества (бараний, говяжий жир и др.) Жиры, в составе которых содержатся главным образом остатки ненасыщенных кислот, имеют жидкую консистенцию при комнатной температуре и называются маслами. Жиры не растворяются в воде, но хорошо растворяются в органических растворителях: эфире, бензоле, хлороформе и др.
Химические свойства. Как все сложные эфиры, жиры подвергаются гидролизу. Гидролиз может протекать в кислой, нейтральной или щелочной среде.
1. Кислотный гидролиз.
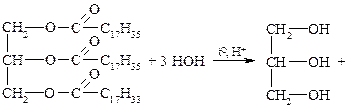
2С17Н35СООН стеариновая
кислота
С17Н33СООН
олеодистеарин глицерин олеиновая кислота
Реакция может быть использована для получения глицерина и высших жирных кислот из жира.
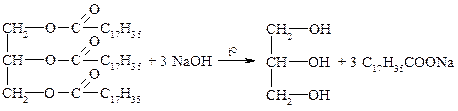
2. Щелочной гидролиз (омыление).
- стеарат натрия (твёрдое мыло).
- тристеарин (глицерин).
Эта реакция лежит в основе процесса получения мыла из жира. В живом организме жиры гидролизуются под действием фермента липазы при t 30–40oС.
3. Гидрогенизация (гидрирование) жидких жиров.
Жидкие жиры могут вступать в реакцию присоединения водорода, в результате чего происходит отвердение жиров.
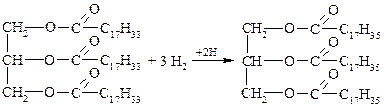
триолеин тристеарин (жидкий жир) (твёрдый жир – саломас)
Подобные твёрдые жиры используются в мыловарении и производстве пищевого маргарина, при этом в полученный твёрдый жир добавляют молоко, яйца, витамин А и другие добавки.
4. Галогенирование жидких жиров.
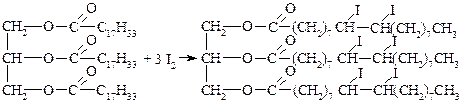
триолеин (жидкий жир)
Реакция используется для определения степени непредельности жиров.
5. Прогоркание жиров.
При хранении жиры под влиянием света, кислорода воздуха, влаги приобретают неприятный вкус и запах, этот процесс называется прогорканием.
При прогоркании происходит несколько химических процессов:
а) Самоокисление жиров. По месту двойной связи происходит присоединение кислорода с образованием перекисных соединений, которые разлагаются в дальнейшем по схеме:
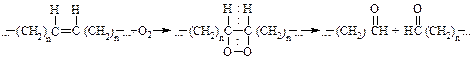
В результате образуются низкомолекулярные альдегиды и кислоты (типа масляной) с неприятным запахом. Этот процесс кроме кислорода окружающей среды, повышенной температуры ускоряют также металлы (Сu, Fe и др.), попадающие в виде следов из оборудования.
Процесс самоокисления жиров можно затормозить с помощью химических веществ – антиоксидантов. Это токоферол (витамин Е), каротиноиды, фосфатиды, полифенольные соединения и др. Добавляют также вещества, которые усиливают действие антиоксидантов. Они называются синергистами. Это аскорбиновая кислота (витамин С), лимонная кислота, сорбит, сахара и их производные и др.
б) Частичная полимеризация (высыхание), что ведёт к накоплению высокомолекулярных полимерных продуктов в жирах. Этот процесс активнее протекает в растительных маслах, отличающихся высоким содержанием непредельных кислот. Различают высыхающие масла (льняное, конопляное), содержащие непредельные кислоты с двумя или тремя двойными связями, линолевую, линоленовую. Такие масла способны на воздухе «высыхать», образуя плёнки. На этом свойстве и основано применение таких масел для получения олифы. Невысыхающие масла (подсолнечное, кукурузное) обладают этим свойством в меньшей степени.
в) Частичный гидролиз, которому подвергаются жиры под действием влаги окружающей среды. В результате накапливаются свободные жирные кислоты, которые оказывают каталитическое действие на процесс самоокисления жиров.
Различные микроорганизмы также способствуют прогорканию жиров, в результате чего биологическая ценность их падает.
Отсюда условия хранения жиров: чистые помещения, низкая температура, отсутствие света, тщательная упаковка (для защиты от кислорода воздуха и влаги).
6. Разложение при нагревании.
При сильном нагревании (250–300°) жиры разлагаются с выделением жирных кислот и различных полимерных смолообразных полимерных продуктов.
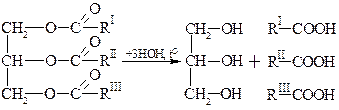
жир глицерин смесь кислот
При этом глицерин расщепляется до акролеина:
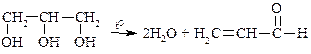
глицерин акролеин
Акролеин преобладает в составе кухонного чада. Это слезоточивая жидкость с резким запахом, при концентрации её 70мг/м3 воздух опасен для жизни, так как является канцерогенным веществом.
Физико-химические показатели жиров.
Качество жира характеризуют такие физико-химические константы:
1. Кислотное число – показывает, сколько миллиграммов КОН требуется для нейтрализации свободных жирных кислот, содержащихся в 1 г жира. Это число характеризует свежесть и доброкачественность жира.
2. Йодное число – показывает, какое количество граммов йода присоединилось к 100 г жира. Чем больше ненасыщенных кислот содержится в молекуле жира, тем больше йодное число.
Так, свиное сало имеет йодное число 50–75
масло подсолнечное – 120–130
масло конопляное – 140–167
масло льняное – 171–200
Чем выше йодное число, тем легче окисляется жир, а значит, менее устойчив при хранении.
3. Перекисное число – показывает количество граммов йода, выделенное из иодида калия перекисями, содержащимися в 100 г жира. Чем выше перекисное число, тем более окисленным является жир, а значит, менее доброкачественным.
Применение жиров:
1. Жиры являются высококалорийной пищей, в процессе усвоения организмом 1 г жира выделяет 9,4 ккал.
2. Жиры являются источником жирорастворимых витаминов А, Д, Е и полиненасыщенных кислот (витамин F).
3. Жиры часто используются в медицине (рыбий жир, оливковое, шиповниковое, персиковое масла), а также как основа для приготовления линиментов, мазей и др.
4. Жиры используются для приготовления косметических средств (кремов, масок и других смесей).
5. Жиры используются для получения мыла, шампуней, а также олифы, которая применяется для приготовления масляных красок, клеёнки, линолеума и т.д.
Фосфатиды – это группа природных сложных эфиров, аналогичная жирам, но в отличие от жиров вместо одного из остатков высшей жирной кислоты содержит остаток фосфорной кислоты, эфирообразно связанный с аминоспиртом.
Общая формула фосфатида:
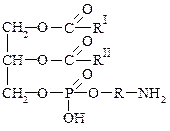
RI, RII – углеводородные радикалы высших жирных кислот
R – (углеводородный) радикал от аминоспирта (остаток амноспирта)
В состав фосфатидов входят аминоспирты – коламин
HOCH2CH2–NH2 и холин 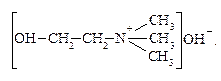
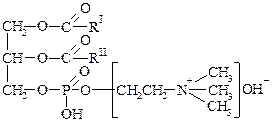
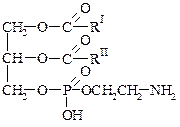
В зависимости от этого фосфатиды делят на кефалины и лецитины. В состав кефалина входит коламин, а в состав лецитина холин.
α
β
α1
кефалин лецитин
Фосфатиды широко распространены в природе. В большом количестве содержатся в нервной ткани (особенно в мозговой части), яичном желтке, в семенах и ростках растений, сое, горохе, молочном жире, печени, сердце и др.
Фосфатиды имеют мягкую консистенцию, плохо растворяются в воде (набухают), растворимы в жирах и органческих растворителях (спирте, эфире и др.). Лецитины нерастворимы в ацетоне.
Химические свойства.
Фосфатиды существуют в виде внутренних солей:
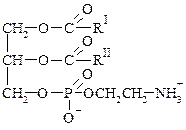
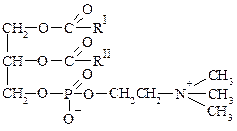
внутренняя соль кефалина внутренняя соль лецитина
Так как фосфатиды содержат кислотную и основную группы, они обладают амфотерными свойствами (образуют соли с кислотами и основаниями).
Фосфатиды могут содержать остатки насыщенных и ненасыщенных кислот, поэтому могут проявлять свойства непредельных соединений. Под действием кислот и щелочей, а также фермента – липазы фосфатиды гидролизуются, распадаясь на жирные кислоты, глицерин, фосфорную кислоту, аминоспирт.
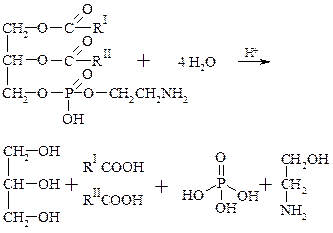
кефалин
глицерин кислоты фосфорная коламин
кислота
В результате этого процесса кислотность при хранении продуктов повышается.
Фосфатиды применяются:
1) в маргариновом и шоколадном производстве в качестве эмульгатора для повышения текучести шоколадной массы, в производстве мороженого;
2) для производства косметических средств (шампуни, кремы и др.);
3) в медицине для введения в организм фосфора в легкоусвояемой форме.
 2014-01-31
2014-01-31 2109
2109








