Тема 5. Основные теории химии и биологии.
Существенный вклад в становление научной химии внесли Бойль, Ломоносов, Лавуазье, Дальтон, Авогадро, Берцелиус.
Благодаря Дальтону в начале XIX века возобладала атомно-молекулярная теория, рассматривающая химический элемент как вид атомов. В 1801 году сформулировал закон парциальных давлений и составил первую таблицу атомных весов химических элементов.

| Джон Да́льтон(1766-1844) — английский химик, физик, создатель химического атомизма. Он стал одним из самых знаменитых и уважаемых учёных своего времени благодаря новаторским работам в разных областях знания |
В 1811 г. Авогадро открыл закон, согласно которому в равных объёмах различных газов при одинаковых температурах и давлениях содержится одинаковое число молекул. Число молекул в одном моле называют числом Авогадро: NA = 6,02252 • 1023 моль.-1
1860 год: симпозиум химиков в Карлсруэ (Германия) – принятие единой системы химических обозначений и написания уравнений.
Периодический закон химических элементов
|
|
|
К моменту открытия Периодического закона было известно 63 элемента. Атомный вес выделен Менделеевым как параметр, определяющий периодические изменения свойств химических элементов →

| Д.И. Менделе́ев(1834 – 1907). Русский учёный-энциклопедист. Среди наиболее известных открытий – периодический закон химических элементов (1869 г.), один из фундаментальных законов мироздания, универсальный для всего естествознания. |
Теория химического строения вещества А.М. Бутлерова
Основы классической теории химического строения были обнародованы А.М. Бутлеровым в сентябре 1861 года в докладе на Съезде естествоиспытателей и врачей в Шпейере (Германия).
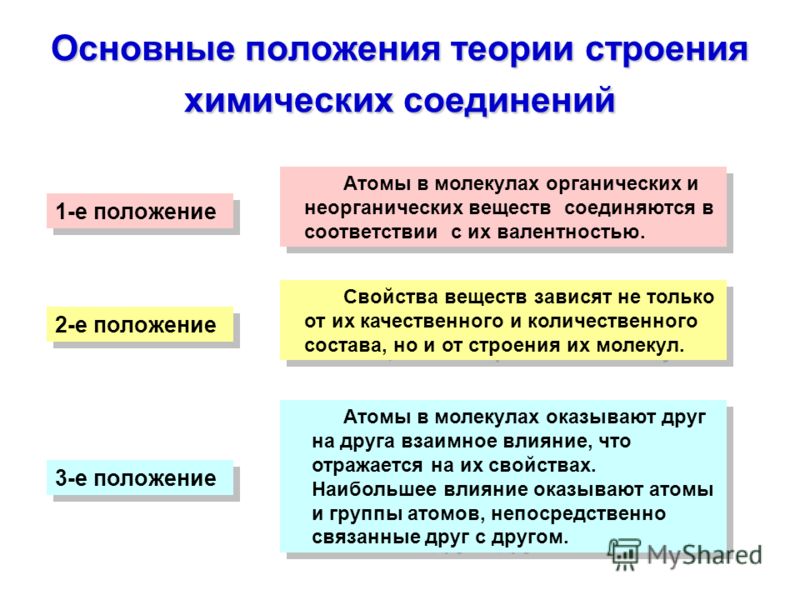
Изомери́я – явление существования соединений, имеющих одинаковый молекулярный состав, но различное строение и разные свойства (малеиновая и фумаровая кислоты, бутан и изобутан и др.).
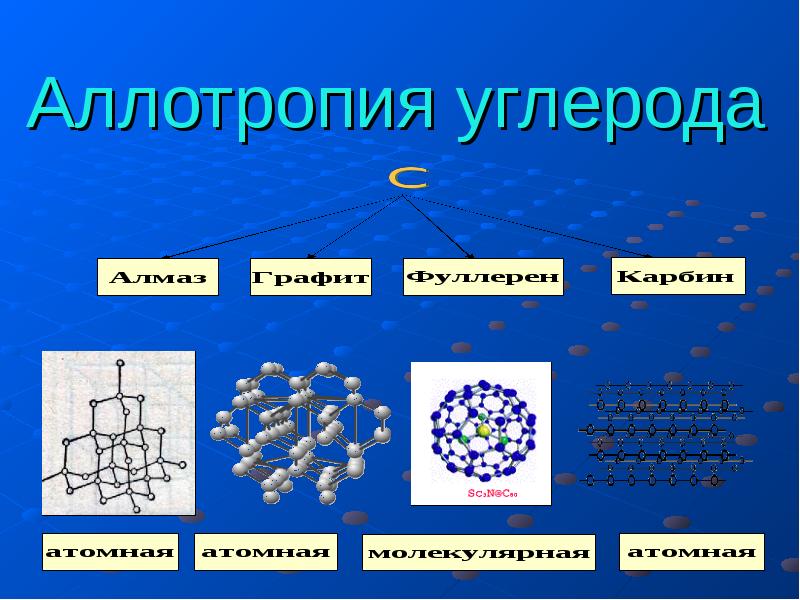
Аллотро́пия – существование двух и более простых веществ одного химического элемента, различных по строению и свойствам.
 2020-09-24
2020-09-24 145
145







