На практике измерение электропроводности растворов электролитов чаще всего используют в двух случаях:
а) для контроля технологических процессов в которых происходит изменение концентрации растворов электролитов, например, процесса обессоливания воды на ХВО ТЭС;
б) для целей химического анализа в сочетании с методами объемного анализа (нейтрализации, комплексообразования). Такой метод получил название кондуктометрического анализа.
Рассмотрим несколько подробнее.
а) Применение электропроводности для контроля технологических процессов на ХВО.
Непременным условием контроля за электропроводностью растворов электролитов в технологических процессах на ТЭС является знание величин удельных электропроводностей этих растворов. В то же время описанный метод дает возможность получать данные лишь о полной электропроводности растворов всегда разной при различных конструкциях датчиков.
Вычисление удельной электропроводности раствора электролита по измеренной полной ее величине G (Ом-1) проводят по уравнению:
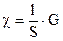 ,
,
где l – расстояние между электродами, см; S – площадь электродов, см2.
В качестве электродов обычно используют две металлические пластины из платины или другого металла, весьма произвольной формы (чтобы увеличить емкость датчика). Во всех случаях отношение l/S остается постоянным и называется постоянной датчика, см-1:
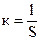 ;
;
тогда 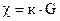 ; Ом-1см-1
; Ом-1см-1
Если электроды выполнены не в виде пластин, а в виде коаксиальных цилиндров, то постоянная такой ячейки, см-1:
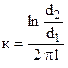 .
.
Электроды обычно закрепляются в корпусе датчика, выполненного из изоляционного материала, часто стекла. Иногда постоянную датчика трудно определить расчетным путем (сложная конфигурация, разные S, l и т.д.). Тогда К определяют экспериментально, путем измерения электропроводности стандартных растворов, т.е. растворов, имеющих точно известное значение удельной электропроводности при заданных t оС и концентрации С. В качестве стандартного раствора используют обычно раствор KCl.
Таблица. Значения удельной электропроводности раствора KCl, Ом-1см-1
| Температура, оС | Концентрация раствора KCl, г-экв/дм3 | ||
| 1,0 н | 0,1 н | 0,01 н | |
| 0,065 | 0,007 | 0,0008 | |
| 0,092 | 0,010 | 0,0011 | |
| 0,112 | 0,013 | 0,0014 |
Измеряя датчиком G раствора KCl при определенной температуре и концентрации рассчитывают к=c/G=const.
 2014-02-04
2014-02-04 873
873








