ГЛАВА 10. ОПРЕДЕЛЕНИЕ ТЕПЛОТЫ СГОРАНИЯ УГЛЕЙ
Теплота сгорания углей является одной из важнейших его энергетических характеристик. Основными горючими веществами в угле являются углерод, водород и отчасти сера (органическая и колчеданная). При горении углерода по реакции
С+О2=СО2
выделяется 8137 ккал/кг тепла[17].
Свободный водород, сгорая, в воду (при 180 С) выделяет 34 180 ккал/кг тепла. Если вода получается в виде пара, то выделяется 28 905 ккал/кг тепла.
Соединения водорода с углеродом дают примерно такие же количества тепла, но водород, связанный с кислородом (Н2О), в тепловом отношении является не только потерянным, но даже вредной составной частью угля (затрачивается тепло на испарение). Процентное содержание связанного водорода в угле упрощено, его представляют равным 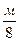 .
.
Сера выделяет при сгорании в SO2 2187 ккал/кг тепла.
Если допустить, что элементы, входящие в состав угольного вещества, дают при сгорании столько же тепла, сколько и в свободном состоянии, то приближенно по составу угля его высшую теплоту сгорания можно выразить так:
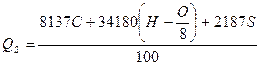 , ккал/кг
, ккал/кг
При учете расхода тепла на испарение гигроскопической влаги (600 W/100) выражение низшей теплоты сгорания по составу угля принимает вид:
, ккал/кг
где W - содержание в угле гигроскопической влаги, %.
Д. И. Менделеев дает упрощенную формулу (округление коэффициентов, уменьшение числа составных частей) для определения теплоты сгорания угля:
Q=81C+300H-26(O-S), ккал/кг,
где C, H, O, S - содержание в угле соответственно углерода, водорода, кислорода и серы, %.
При определении теплоты сгорания надо учитывать фазовое состояние, как сжигаемого вещества, так и продуктов реакции. Если в результате реакции получается газ, то определенная опытом теплота сгорания при постоянном объеме QV отличается от теплоты сгорания при постоянном давлении QP на величину работы, которую могут совершить образующиеся газы:
QP=QV+RT(n¢-n),
где n¢ - число молей газа до реакции;
n - число молей газа после реакции;
R - универсальная газовая постоянная;
Т - температура, 0К.
Экспериментально теплоту сгорания угля определяют (по ГОСТ 147 - 74) путем сжигания навески аналитической пробы угля в калориметрической бомбе (при постоянном объеме) в среде сжатого кислорода, насыщенного водяным паром, и в определении количества теплоты, выделившейся при сгорании угля, а также при образовании и растворении в воде серной и азотной кислот в условиях испытания угля.
Навеску угля помещают в чашечку, располагаемую внутри калориметрической бомбы, заполненной кислородом под давлением 25 - 30 кг/см2 и соединенной с запалом тонкой (диаметр 0,1 - 0,2 мм) проволокой, с помощью которой, пропуская электрический ток, поджигают навеску.
Зная вес сожженного угля и количество воды в калориметрическом сосуде, наблюдая повышение ее температуры, вычисляют теплоту сгорания  угля. Следует учитывать, что при сжигании угля в топках содержащаяся в нем вода переходит в пар, удаляющийся вместе с топочными газами, унося с собой скрытую теплоту парообразования, в бомбе же пар конденсируется.
угля. Следует учитывать, что при сжигании угля в топках содержащаяся в нем вода переходит в пар, удаляющийся вместе с топочными газами, унося с собой скрытую теплоту парообразования, в бомбе же пар конденсируется.
Содержащиеся в угле сера и азот в бомбе окисляются и образуют серную и азотную кислоты с выделением некоторого количества тепла. В топках этого не происходит - горючие соединения серы в угле образуют сернистый газ, уходящий вместе с продуктами сгорания угля. Азот же не окисляется и удаляется из топки в виде инертного газа. Поэтому в полученные результаты анализа вносят поправки на скрытую теплоту парообразования в топках и теплоту образования кислот в бомбе.
 2014-02-05
2014-02-05 1771
1771
