1. В промышленности – основной источник получения алканов – продукты перегонки нефти и сопутствующие газы.
2. Получение из синтез-газа и двуокиси углерода

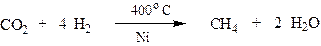
3. Каталитическое гидрирование алкенов.
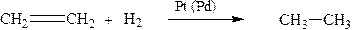
4. Реакция Вюрца (лабораторный метод):
СН3Br + 2Na → CH3Na + NaBr
CH3Na + CH3Br → CH3-CH3 + NaBr
Суммарно: 2 CH3Br + 2Na → CH3-CH3 + 2NaBr
Алканы достаточно инертные соединения, однако в определенных условиях они способны вступать в реакции.
1. реакции замещения протекают по радикальному механизму SR:
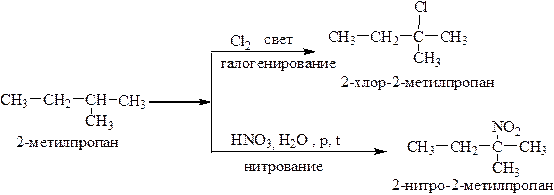
Реакция галогенирования протекает на свету (условное обозначение – һν), с помощью этой реакции можно ввести в молекулу алкана хлор, бром.
Монозамещение атома водорода протекает, преимущественно у третичного углерода, если такового в структуре алкана нет, тогда у вторичного углерода; так как в этом случае образуются наиболее устойчивые промежуточные частицы (радикалы).
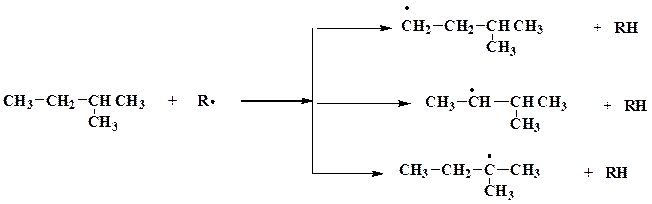
2. Реакции окисления.
Насыщенные углеводороды при нормальных условиях не окисляются даже сильными окислителями. При высоких температурах, под действием кислорода воздуха они воспламеняются и сгорают с выделением большого количества тепла, окисляясь при этом до СО2 и Н2О. Каталитическое окисление алканов даёт возможность получать кислородсодержащие соединения различных классов:
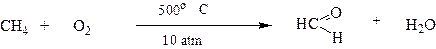
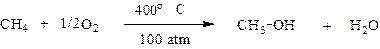

Применение
Алканы – основные компоненты топлив.
Метан СН4 используется для получения ацетилена, синильной кислоты, хлороформа, четыреххлористого углерода, сажи (технический углерод), формальдегида.
Этан С2Н6 – исходный материал в синтезе этилена.
Пропан С3Н8 применяют в синтезе этилена (пиролиз) и пропилена, нитрометана, сажи. Это компонент бытового топлива.
Бутаны С4Н10 дегидрируют в изобутилен и бутадиен-1,3.
Пентаны С5Н12 дегидрируют с целью получения изопрена и синтетического каучука, применяют в качестве растворителя. Кроме того, они являются ценными компонентами бензинов.
Гептан С7Н16 нормального строения
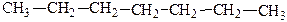
и 2,2,4-триметилпентан, называемый изооктаном,
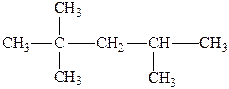
применяют в качестве стандартных веществ при определении октанового числа бензинов.
 2014-02-02
2014-02-02 1552
1552








