**алифатические (α-, β-,γ)
**ароматические
 - COOH исполь-ся в пр-ве красителей и лек.ср-в
- COOH исполь-ся в пр-ве красителей и лек.ср-в
_ NH2
Онтрониловая к-та.

 - COOH
- COOH
 ПАБК
ПАБК
NH2
Способы получения: **действие аммиака на Hal– карб.к-ты.


 R-CH-COOH +NH3 R-CHCOONH4 +HCl R-CH-COOH
R-CH-COOH +NH3 R-CHCOONH4 +HCl R-CH-COOH
CH -NH4Cl NH4 NH2
**Восстановительное аминирование оксо к-т.


 R-C-COOH NH3,H2 R-C-COOH R-C-COOH
R-C-COOH NH3,H2 R-C-COOH R-C-COOH



 O NH NH2
O NH NH2
Иминокислота
**Присоед. NH3к α,β-ненасыщ.к-ам.
β
 R–CH=CH–COOH+NH3®R-CH-CH2COOH
R–CH=CH–COOH+NH3®R-CH-CH2COOH
NH2
**Ароматические получают восстановлением по Зинину соотв. нитробензойных к-т.

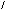 COOH COOH
COOH COOH

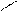



 [H] +H2O
[H] +H2O
 | |||||
 |  | ||||

 NO2 NH2
NO2 NH2
Химические свойства: *Все реакции по –COOH
*Реакции по NH2гр.
Аминокисл –это амф.соед.об-ют соли как с щелочами, так и с к-ми.
*Отнош. к нагрев.позволяют различить α,β,γ-алиф.аминок-ты.
а) α –АК при t-ре межмолек.дегидратируются с образованием дикетопиперазина.
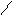
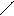 O
O
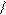
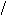
 R-CH-C O
R-CH-C O
 HNH OH R-CH-C
HNH OH R-CH-C
 + to HN NH
+ to HN NH

 HNH -2H2O C-CH-R
HNH -2H2O C-CH-R
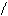
 HO O
HO O
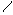 C-CH-R
C-CH-R
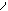 O
O
б) β-АК подвергаются дезаминированию
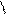
 R-CH-CH-COOH to R-CH=CH-COOH
R-CH-CH-COOH to R-CH=CH-COOH
 NH2 H -NH3 непред.карб.кислота
NH2 H -NH3 непред.карб.кислота
в) γ-АК дегитратируются внутримолек с об-ем лактама.


 СН2-CH2 CH2-CH
СН2-CH2 CH2-CH
R-CH C=O to R-CH C=O
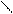

 HNH OH -H2O NH лактам.
HNH OH -H2O NH лактам.
γ-аминомаслян.к-та(ГАМК)
α-аминомаслян.к-та.(аминолон)
ПАБК входит в состав фолиевой к-ты.
Ее эфиры:этиловый эфир ПАБК(анестезин)

 O
O

 H2N- -C
H2N- -C
 OC2H5
OC2H5
 O
O
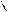 H2N- -C
H2N- -C
 OCH2CH2N(C2H5)2 новокаин
OCH2CH2N(C2H5)2 новокаин

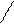
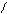
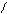
 O
O
H2N- -C

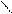 NHCH2CH2N(C2H5)2 новокаинамид
NHCH2CH2N(C2H5)2 новокаинамид
Природные α-аминокислоты
Большое зн.имеет 20 α-аминок-т, входящих в состав пептидов и белков,т.е.
α
 H2N-CH-COOH - общая формула.
H2N-CH-COOH - общая формула.
R
Стереоизомерия. Все кроме глицина имеют хиральный атом С и сущ-ют в виде пары энантиомеров.
(природные отн-ся к 4-ряду)


 COOH COOH
COOH COOH


 H NH2 NH2 H
H NH2 NH2 H
 R R
R R
Д-α-АК 4-α-АК
Изолицин и трионин имеют по 2 хиральных центра из 4-х изомеров, в пр-де встр-ся следующие:
COOH COOH



 H2N H H2N H
H2N H H2N H

 H3C H H OH
H3C H H OH
CH2CH3 CH3
4-изолейцин 4-треонин
Классификация: 1. Моноаминомонокарбоновые (1 NH2, 1-COOH, нейтр.)
** H2N-CH2COOH глицин (гли)
 ** H2N-CH-COOH аланин (ала)
** H2N-CH-COOH аланин (ала)
CH3
 **H2N-CH-COOH валин(вал)
**H2N-CH-COOH валин(вал)
 CH-CH3
CH-CH3
CH3
 ** H2N-CH-COOH лейцин(лей)
** H2N-CH-COOH лейцин(лей)
 CH2
CH2
 CH-CH3
CH-CH3
CH3
 ** H2N-CH-COOH изолейцин(илей)
** H2N-CH-COOH изолейцин(илей)
 CH-CH3
CH-CH3
 CH2
CH2
CH3
Оксоаминокислот
 ** H2N-CH-COOH серин(сер)
** H2N-CH-COOH серин(сер)
CH2OH
 **H2N-CH-COOH треонин(тре)
**H2N-CH-COOH треонин(тре)
 CHOH
CHOH
CH3
Серусодержащиеаминокислоты
 **H2N-CH-COOH цистеин(цис)
**H2N-CH-COOH цистеин(цис)
CH2-SH
 H2N
H2N

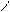 **H2N-CH-COOH CH-COOH
**H2N-CH-COOH CH-COOH
CH2SH – SCH2 цистин(цис– S-S-цис)
 ** H2N-CH-COOH метионин(мет)
** H2N-CH-COOH метионин(мет)
 CH2
CH2
CH2SCH3
Ароматические
 ** H2N-CH-COOH фенилаланин(фен)
** H2N-CH-COOH фенилаланин(фен)
 CH2
CH2
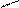

 | |||
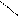 | |||
 ** H2N-CH-COOH тирозин(тир)
** H2N-CH-COOH тирозин(тир)
 CH2
CH2


OH
Гетероциклические


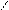
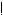

 ** СH2-CH-COOH
** СH2-CH-COOH
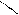 NH2 триптофан (три)
NH2 триптофан (три)
 N
N
H
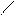
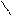

 ** N
** N
 - CH2-CH-COOH гистидин (гис)
- CH2-CH-COOH гистидин (гис)
 N NH2
N NH2
H
2. Моноаминодикарбон-ые к-ты (1-NH2, 2-COOH, кислые)
 H2N-CH-COOH
H2N-CH-COOH
CH2-COOH аспарагиновая к-та (АСП)
 ** H2N-CH-COOH
** H2N-CH-COOH

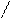 O
O
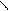 CH2C аспарагин (асн)
CH2C аспарагин (асн)
NH2
 **H2N-CH-COOH глутаминовая к-та (глу)
**H2N-CH-COOH глутаминовая к-та (глу)
 CH2
CH2
CH2COOH
 **H2N-CH-COOH
**H2N-CH-COOH
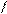

 CH2 O глутамин(глн)
CH2 O глутамин(глн)
 CH2C
CH2C
NH2
3. Диаминомонокарбон. к-ты. (2-NH2, 1-COOH)
 **H2N-CH-COOH
**H2N-CH-COOH
 (CH2)3 орнитин (орн)
(CH2)3 орнитин (орн)
NH2
 ** H2N-CH-COOH
** H2N-CH-COOH
 (CH2)4 лизин(лиз)
(CH2)4 лизин(лиз)
NH2
 ** H2N-CH-COOH
** H2N-CH-COOH
 (CH2)3 аргинин(арг)
(CH2)3 аргинин(арг)
 NH
NH
 C=NH
C=NH
NH2
4.Иминокислота
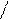
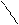
 **
**
 COOH пролин (про)
COOH пролин (про)
 N
N
H

 ** HO
** HO

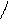
 COOH оксипролин (про-н)
COOH оксипролин (про-н)

 N
N
H
Незаменимые АМК (не синтезир-ся в орг-ме, должны поступ.в орг)
-вал
-лей
-илей
-тре
-мет
-лиз
-фен
-три
Остальные синтез-ся в орг-ме в процессе след.реак:
1. Трансамнирование (переом-ие)


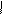
 COOH COOH COOH COOH
COOH COOH COOH COOH



 C=O + CH-NH2 F C=O + CH-NH2
C=O + CH-NH2 F C=O + CH-NH2
R1 кето R2 амино R2 нов.кето R1 нов.амино

 2. COOH COOH
2. COOH COOH


 C=O +NH3, +H2 CHNH2
C=O +NH3, +H2 CHNH2
R R
Химические свойства: 1. Получение произ-ых по карбоксильн.группе
- соли (со щелоч)
- амиды (с NH3)
- сл.эфиры (со спиртами)
- ангидриды (с карб.к-ми)
- хлорангидриды (с PCl5, PCl3, SOCl2)
- декарбоксилирование


 In Vitro Ba(OH)2 to
In Vitro Ba(OH)2 to

 H2N-CH-COOH - H2N-CH2-R
H2N-CH-COOH - H2N-CH2-R
R inVivo биогенные амины (коламин, гистамин)

2. Реакции по аминогруппе
-об-ие солей (с мин.к-ми)
-алкилирование (с алкилгалоген.)
 O
O
 -ацилир-ие (с R-C / (CH3CO)2O)
-ацилир-ие (с R-C / (CH3CO)2O)
Cl
-дезаминирование:
In Vitro;


 H2N-CH-COOH+HONO®HO–CH–COOH+N2+H2O
H2N-CH-COOH+HONO®HO–CH–COOH+N2+H2O
R R
Метод Ван-Слайка (исп-ся для комп.опред.АМК)
In Vivo; окиси-ое:





 H2N-CH-COOH HAД+ R-CHCOOH®R-C-COOH
H2N-CH-COOH HAД+ R-CHCOOH®R-C-COOH
R HAДН NH O
Неокислит:

 R-CH-CH-COOH ® R-CH=CH-COOH
R-CH-CH-COOH ® R-CH=CH-COOH
H Nh2 -NH3
3. Реак. с формальдегидом (для опред.колич.АМК)


 R-CH-COOH O
R-CH-COOH O

 NH2 + H-C ®R-CH-COOH
NH2 + H-C ®R-CH-COOH
H NHCH2OH
Реак.сфенилизатиоцианатом


 C6Hб-5N=Cб+ =Sб-+ H2N-CH-COOH ®C6H5NH–C–NH–CH–COOH®
C6Hб-5N=Cб+ =Sб-+ H2N-CH-COOH ®C6H5NH–C–NH–CH–COOH®
R R
HCl


 -H2O S
-H2O S
 C
C
 C6H5-NH NH фенилтиогидантаиновоепроиз-ое.
C6H5-NH NH фенилтиогидантаиновоепроиз-ое.
 C-CH-R
C-CH-R
O
 2014-02-02
2014-02-02 2678
2678








