Лекция № 18
· Реакция ароматического электрофильного замещения (SEAr). Механизм, понятие о p- и s-комплексах. Энергетические характеристики реакций SEAr. Экспериментальные доказательства механизма. Примеры SE реакций: нитрование, галогенирование, алкилирование и ацилирование по Фриделю-Крафтсу, сульфирование. Особенности этих реакций.
Для бензола характерны реакции замещения. Поскольку над и под плоскостью бензольного цикла есть две тороидальные области повышенной электронной плосности, бензольное кольцо может быть атаковано частицей, имеющей недостаток электронов - электрофилом. Это реакции SEAr – ароматического электрофильного замещения (сокращение читается справа налево).
Реакция SEAr состоит из следующих стадий:
· образование p-комплекса - диполь-дипольное взаимодействие электрофила с ароматической системой;
· образование s-комплекса - электрофил вытягивает из ароматической системы пару электронов, образуя сигма-связь с атомом углерода;
· реароматизация – отщепление протона с образованием замещенной ароматической молекулы.
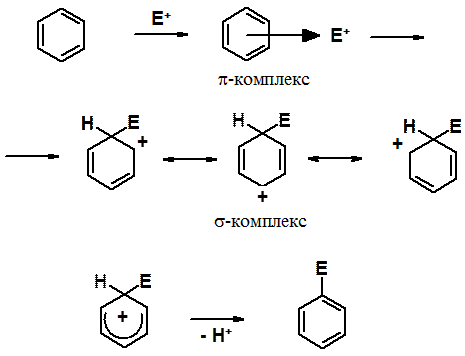
Строение s-комплекса может быть показано тремя граничными структурами с различным расположением p-электронов и карбокатионного центра. Реальный s-комплекс – суперпозиция граничных структур, в котором атом углерода, участвующий в реакции, находится в sp 3-гибридизованном состоянии, а остальные - в sp 2. Положительный заряд делокализован (распределен) по пяти sp 2-углеродным атомам. Положительный заряд – недостаток электронов, а не наличие частицы с плюсом. Следовательно, делокализованный положительный заряд – делокализация четырех электронов по пяти углеродным атомам. Формально можно рассчитать так: 5 (углеродов) минус 4 (электрона) = +1 (заряд s-комплекса). В показанных выше граничных структурах на трех углеродных атомах есть плюс. Это означает, что в s-комплексе нет идеальной выровненности p-электронной плотности, как в молекуле бензола. На тех атомах, у которых в граничных структурах положительный заряд, электронная плотность ниже, чем у двух других.
Последняя стадия реакции – реароматизация. Как уже отмечалось, ароматические системы характеризуются высокой устойчивостью (низким содержанием энергии), благодаря делокализации p-электронов (см. энергию сопряжения). Нарушение ароматической системы ведет к увеличению энергии, возврат к ароматическому циклу – к уменьшению. Именно поэтому происходит отщепление протона, а не присоединение к s-комплексу какой-либо нуклеофильной частицы.
Из энергетического профиля реакции SEAr (рис. 18.1) можно сделать вывод, что первая стадия реакции (образование s-комплекса) является определяющей. Её энергия активации (Еа1) значительно большее энергии активации второй стадии (Еа2).
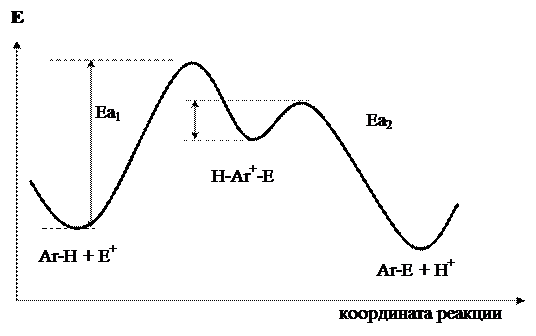
Рис. 18.1. Энергетическая диаграмма реакции
ароматического электрофильного замещения
Доказательством правильности изложенного механизма является отсутствие первичного кинетического изотопного эффекта в реакциях SEAr дейтерированного бензола.
Рассмотрение рис. 18.1 позволяет сделать важный вывод. Высшая точка реакции – переходное состояние (не регистрируется), образующееся на первой стадии, по энергии ближе к промежуточному продукту (s-комплексу). Все факторы, стабилизирующие s-комплекс, будут стабилизировать (уменьшать энергию, облегчать реакцию) и переходное состояние. Рассмотрим конкретные реакции замещения, обращая внимание на природу атакующего агента.
 2014-02-02
2014-02-02 1202
1202
