Теплоемкостью тела будем называть отношение элементарного количества тепла dQ, сообщенного телу в каком-либо процессе, к произошедшему в результате этого изменению температуры тела dT
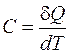 .
.
В том случае, если теплоемкость не сильно зависит от температуры, ее можно определить также как физическую величину численно равную количеству теплоты, которое нужно сообщить телу, чтобы увеличить его температуру на 1 градус.
Теплоемкость зависит от массы тела, его термодинамического состояния и вида процесса сообщения тепла.
Удельной теплоемкостью называется теплоемкость единицы массы однородного вещества
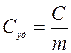 .
.
Единица удельной теплоемкости — Дж/(кг К)
Молярной теплоемкостью называют теплоемкость одного моля вещества
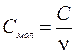 , где
, где 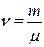 - число молей вещества.
- число молей вещества.
Единица молярной теплоемкости — Дж/(моль К).
Пусть нагревание тепа происходит при неизменном объеме (V =const). Соответствующая молярная теплоемкость называется изохорической теплоемкостью и обозначается CV
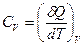 .
.
Так как в этом случае dQ = dU, то можно записать, что
|
|
|
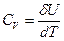 .
.
Аналогично определяется теплоемкость при постоянном давлении Сp (изобарическая теплоемкость)
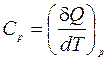 .
.
Идеальный газ представляет физическую модель, согласно которой:
1) собственный объем молекул газа пренебрежимо мал по сравнению с объемом сосуда;
2) между молекулами газа отсутствуют силы взаимодействия;
3) столкновения молекул газа между собой и со стенками сосуда абсолютно упругие.
Теплоемкость Сp идеального газа при постоянном давлении больше теплоемкости при постоянном объеме СV
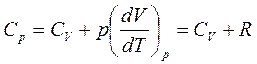 , уравнение Майера
, уравнение Майера
поскольку для одного моля газа
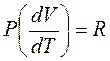 .
.
как следует из дифференцирования уравнения уравнение Клапейрона - Менделеева по dT при условии p =const.
Так как 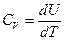 , то при постоянной молярной теплоемкости CV внутреннюю энергию можно записать
, то при постоянной молярной теплоемкости CV внутреннюю энергию можно записать
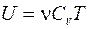 . (14)
. (14)
Идеальный газ можно рассматривать как совокупность беспорядочно движущихся молекул-шариков, имеющих пренебрежимо малый собственный объем и не взаимодействующих друг с другом на расстоянии.
 2014-02-02
2014-02-02 2388
2388








