В водных растворах пероксид водорода – слабая кислота ( ):
):
I. 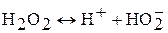
II. 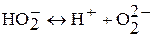
Пероксида металлов (Na2O2, BaO2, Li2O2 и аммония), которые получены при действии концентрированного раствора пероксида водорода на гидроксиды, рассматривают как соли этой слабой кислоты.
2. Окислительно-восстановительные свойства.
Оба атома кислорода в Н2О2 находятся в промежуточной степени окисления –1, поэтому пероксид водорода может проявлять окислительные и восстановительные свойства:
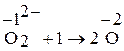 (окислитель)
(окислитель)
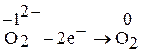 (восстановитель)
(восстановитель)
Пероксид водорода – сильный окислитель, при его восстановлении образуется вода или ОН–. Окислительные свойства пероксидов выражены сильнее, чем восстановительные.
Например:
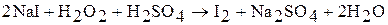
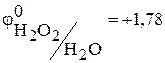 В
В
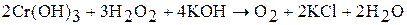
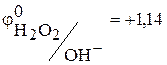 В
В
Окислительные свойства наиболее ярко выражены в кислой и нейтральных средах.
Пероксид водорода – слабый восстановитель, реагирует с сильными окислителями. В этих реакциях выделяется свободный кислород. Например:
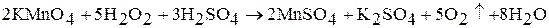
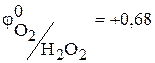 В
В
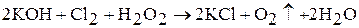
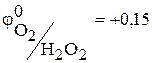 В
В
Восстановительные свойства наиболее ярко выражены в щелочной среде.
3. Пероксид водорода – гетерогенный окислитель. Например:
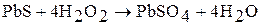
4. Так как связи в молекуле пероксида водорода неравноценны, то вещество крайне неустойчиво. Пероксид водорода самопроизвольно диспропорционирует даже в разбавленных растворах с образованием Н2О и кислорода:

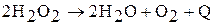
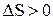 ,
, 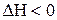 ;
; 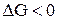
Пероксид с высокой концентрацией разлагается со взрывом, поэтому в него добавляют ингибитор (Na4P2O7), разбавленный пероксид сравнительно устойчив и разлагается под действием катализатора (MnO2, ионы d-элементов Cu2+, Fe3+, Mn2+, платина, серебро, хлорид ионы, некоторые белки).
Пероксид водорода используют для отбеливания бумаги, кожи, текстильных материалов, как окислитель ракетного топлива. Растворы пероксида водорода применяются в качестве дезинфицирующего средства.
Кислоты, содержащие пероксидную группу, называют пероксокислотами. Например, пероксосерная кислота H2SO5, пероксодисерная кислота H2S2O8.
Так же как пероксид водорода пероксокислоты неустойчивы и проявляют сильные окислительные свойства. При гидролизе пероксокислот образуется пероксид водорода:
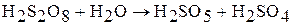
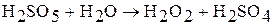
 2014-02-03
2014-02-03 4798
4798
