Активная реакция и окислительно-восстановительный
Активная реакция среды. Обусловлена присутствием в воде ионов Н+ и ОН-. Как известно, часть молекул воды диссоциирует на эти
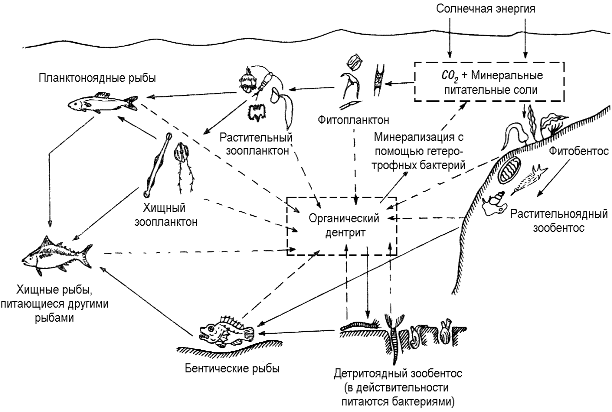
Рисунок 4.6 – Схема круговорота вещества в океане (по [9])
ионы, причем произведение их концентраций есть величина постоянная, численно равная при 25 °С 10-14 г-ионов в 1 дм3воды.
В случае, когда концентрации ионов Н+ и ОН- равны (каждый из них содержится в количестве 10-7 г-ионов/дм3)вода нейтральная. С увеличением содержания ионов Н+ и ОН- более 10-7 г-ионов/дм3 вода будет соответственно кислой или щелочной.
Обычно в качестве показателя активной реакции берется не концентрация Н+, а ее десятичный логарифм с обратным знаком. Эта величина называется водородным показателем иобозначается символом рН. Если рН меньше 7 – вода кислая, больше 7 – щелочная, для нейтральной воды рН равен 7.
Активная реакция природных вод довольно устойчива, т.к. они благодаря присутствию карбонатов представляют собой сильно забуфференную систему. В случае отсутствия карбонатов рН воды может снижаться. Во время интенсивного фотосинтеза рН может подниматься до 10 и более вследствие почти полного исчезновения из воды углекислоты.
В морских водах рН обычно равен 8,1-8,4. Природные воды с рН от 3,4 до 6,5 называются кислыми,с рН от 6,5 до 7,5 – нейтральными, с рН от 7,5 до 10 и выше – щелочными.
В одном и том же водоеме рН в течение суток может колебаться на 2 единицы и более: ночью рН понижается в результате подкисления воды выделяющимся в процессе дыхания углекислым газом, днем повышается за счет потребления углекислого газа фотосинтезирующими растениями. В грунтах озер и болот рН обычно несколько ниже 7, в океанических осадках он часто бывает несколько сдвинут в щелочную сторону.
По отношению к различным концентрациям водородных и гидроксильных ионов гидробионты подразделяются на:
– эвриионных, выдерживающих большие изменения рН;
– стеноионных, обитающих в водах с колебанием рН в незначительных пределах. Среди стеноионных выделяются ацидофильные (предпочитают кислые воды), алкалифильные (обитают в щелочных водах).
Экологическое действие рН связано с изменением проницаемости наружных мембран клеток, влиянием на водно-солевой обмен, границы распространения и характер жизнедеятельности гидробионтов.
Окислительно-восстановительный потенциал. Характеризует условия протекания в среде окислительных и восстановительных процессов.
В результате взаимодействия двух веществ может происходить окислительно-восстановительная реакция, приводящая к возникновению между ними разности электрических потенциалов – Еh, или редоксипотенциала. Величина Еh измеряется обычно милливольтами (мВ). Он тем выше, чем больше отношение концентрации компонентов, способных к окислению, к концентрации компонентов, могущих восстанавливаться.
Концентрация окисленной формы водорода (Н+) характеризуется величиной рН, концентрация восстановленной формы водорода выражается показателем rH (или rH2), представляющим собой логарифм величины давления молекулярного водорода, взятый с обратным знаком. Чем меньше величина rH, тем выше восстановительная способность среды. Таким образом, окислительно-восстановительные свойства среды могут характеризоваться как величиной редоксипотенциала Eh, так и условными единицами rH, указывающими концентрацию молекулярного водорода, способную создать данные окислительно-восстановительные условия. Чем выше редоксипотенциал, тем выше окислительная способность среды и тем выше величина r, т.е. ниже концентрация молекулярного водорода, необходимая для создания окислительно-восстановительных условий.
Связь между Eh, rH и рН выражается зависимостью:
Eh=0,029(rH-2pH).
Вода морских и пресных водоемов, содержащая значительное количество кислорода, имеет положительный Eh=300-350 мВ, т.е. является средой окисленной, и в ней величина rH=35-40. В придонных слоях воды содержание кислорода снижается, Eh становится отрицательным, rH падает до 15-12.
Величина редоксипотенциала влияет на скорость окисления сероводорода серными бактериями, на поведение гидробионтов.
Те или иные свойства воды в разных участках водоемов, водотоков проявляются в неодинаковой степени. Проникновение света, движение воды, температурный режим, кислородный баланс и др. показывают, что в различных участках водоемов свойства воды проявляются не в равной мере.
 2014-02-09
2014-02-09 3007
3007
