КИСЛОРОД – газ без цвета, запаха и вкуса. Атмосферный кислород
состоит из трех изотопов 168О; 128О; 188О. Атомная масса атмосферного кислорода 15,9994 а.е.м. Кислород соединяется с большинством элементов с образованием окислов, проявляя при этом валентность равную –2, кроме соединений со фтором). Сжижается в бледносинюю жидкость, с температурой кипения –182,98 С. Твердый кислород – также бледносинего цвета – притягивается магнитом.
Кислород в воздухе может существовать в атомарном и молекулярном виде. В молекулярном виде кислород может существовать в виде собственно кислорода О2 и озона О3. Озон – газ голубого цвета в тонком слое и синего в толстом слое. В сжиженом состоянии представляет собой синефиолетовую жидкость, а в твердом состоянии имеет почти черный цвет. Обладает своеобразным едким запахом, напоминающем запах хлора при высоких концентрациях. В небольших концентрациях имеет «запах свежести».
Кислород слабо растворим в воде и других растворителях. В одном объеме воды при 20ОС растворяется 3 объема кислорода.
Кислород обладает высокой магнитной восприимчивостью по сравнению с другими газами (магнитная восприимчивость окиси азота в два раза меньше, а остальные газы имеют значительно меньшие значения магнитной восприимчивости). Его удельная магнитная восприимчивость значительно зависит от температуры и с повышением температуры резко снижается. Именно это свойство кислорода используется в основе большинства применяемых в ГА.
Повышение в воздушной среде концентрации кислорода приводит повышению пожароопасности. С повышением температуры смеси большинства веществ с кислородом самовоспламеняются и взрываются. При снижении концентрации кислорода до 12-15 % горение прекращается. При понижении концентрации кислорода до 8-9% прекращается тление.
ВОДОРОД – газ без цвета, запаха, вкуса. Обладает наибольшей среди газов скоростью диффузии. Диффундирует через пористые перегородки (резина, фарфор), нагретые до 10000С тонкие металлические перегородки. Хорошо абсорбируется многими металлами, особенно платиновой группы. (Один объем палладия поглощает 850 объемов водорода.) Очень легко воспламеняется и взрывается в смеси с любыми окислителями. В смеси с воздухом имеет нижний предел самовоспламенения около 4%. Водород имеет высокую теплопроводность, соизмеримую лишь с гелием. Но поскольку гелий в атмосфере содержится лишь в небольших количествах, то именно это свойство используется в основе принципа действия большинства ГА на водород.
ОКИСЬ УГЛЕРОДА – газ без цвета и запаха. Чрезвычайно ядовит. В процессе пожаров образуется в воздушной среде отсеков в больших количествах (Достаточно одного вдоха для смертельного отравления). Является продуктом неполного сгорания углерода, поэтому поддерживает горение. В смеси с воздухом горит синеватым пламенем и взрывается. Сгущается в бесцветную прозрачную жидкость при –192оС. Имеет характерную полосу поглощения в ИК спектре и именно на этом свойстве основана работа автоматических ГА на окись углерода. Средством защиты от окиси углерода в процессе пожара являются только изолирующие средства защиты.
На катализаторах платиновой группы легко окисляется в углекислый газ при комнатной температуре.
УГЛЕКИСЛЫЙ ГАЗ – бесцветный газ с кисловатым вкусом и запахом. В воздухе присутствуют следующие изотопы углекислого газа:
q С12 О16 О16 - 98,42%;
q С13О16 О16 – 1,1%;
q С12 О16О18 – 0,4%.
Сгущается в бесцветную жидкость при –56,6С. Имеет характерные полосы поглощения в ИК спектре: 618 – 667 см-1; 1932 см-1; 2037 – 2129 см-1; 3613 – 3714 см-1. На этом его свойстве основаны газоанализаторы непрерывного типа. В гермообъектах накапливается в значительных количествах в процессе жизнедеятельности людей и работы механизмов. Поэтому может быть определен по изменению оптической плотности воздушной среды.
ОКИСЛЫ АЗОТА: ОКИСЬ АЗОТА, ДВУОКИСЬ АЗОТА, АЗОТНЫЙ ТЕТРАОКСИД.
ОКИСЬ АЗОТА – бесцветный газ, сгущающийся при атмосферном давлении при-151,4С в бесцветную жидкость. В помещениях без вентиляции образуется в достаточно больших количествах при эксплуатации электрического оборудования. На поверхности электрического разряда, сопровождающего любое переключение в электрических цепях азот воздуха окисляется до окиси азота. Окись азота очень быстро окисляется кислородом воздуха до двуокиси азота. С повышением температуры реакция окисления замедляется.
ДВУОКИСЬ АЗОТА – красно-бурый газ, обладающий в малых концентрациях «свежим» запахом, в больших концентрациях запахом напоминающим запах хлора. Легко сгущается в бурую жидкость кипящую при +21С. Двуокись азота является чрезвычайно сильным окислителем. При взаимодействии с водой образует смесь азотистой и азотной кислот. С увеличением концентрации двуокись азота превращается в азотный тетраоксид и находится с ним с состоянии равновесия. При нормальном давлении и температуре 40С доля двуокиси азота составляет 31%, при 100С – 88% при 140С – 100%. В больших концентрациях вызывает поражение кожных покровов человека (пожелтение и омертвение кожи) и отек легких.
АЗОТНЫЙ ТЕТРАОКСИД (АТ или «Амил» – компонент ракетного топлива баллистических ракет (окислитель горючего – несимметричного диметилгидразина). Агрессивная темнобурая жидкость хранящаяся на пла в ампулизированном виде. Для исключения разъедания АТ сплава бака, где хранится АТ его поверхности пассивируют йодом. Но даже в этом случае возможна разгерметизация бака окислителя с течением времени. Разгерметизация бака с окислителем является крайне тяжелой аварией. Азотный тетраоксид попадая в воздушную среду диссоциирует с образованием двуокиси азота. Для защиты от азотного тетраоксида используются изолирующие противогазы ПРВ, ИП-6Р и специальная одежда. Облив азотным тетраоксидом приводит к разгерметизации переговорной мембраны изолирующего противогаза, разрушением маски и спецодежды в течение нескольких минут. Поэтому в случае облива работающий персонал должен немедленно покинуть, если это возможно, загазованное помещение. Человеческая кожа при кратковременном контакте с парами АТ приобретает ярко желтый цвет.
Определяется по реакции вытеснения йода из некоторых соединений с реакцией последнего с крахмалом. Окись азота предварительно окисляется до двуокиси азота на стекловолокне, смоченном марганцовокислым калием.
АММИАК – бесцветный газ с характерным резким запахом. Температура кипения –33,4С, температура плавления –77,7С.Легко растворяется в воде. Водный раствор аммиака обладает сильными основными свойствами. При 0С предел растворимости – 42,8%, при20С – 33,1%, при 40С – 23,4% при 60С – 14%. Воздух, содержащий 16,5 -26,8 % аммиака, взрывоопасен. Аммиак используется для создания щелочного режима в 1 контуре водо-водяных реакторов. Имелись случаи тяжелого отравления аммиаком при взрывах на хранилищах аммиака в различных городах. Средство защиты – фильтрующий противогаз, любое изолирующее СИЗОД. Наиболее частое средство определения аммиака – реактив Несслера.
СЕРОВОДОРОД – бесцветный газ с характерным запахом тухлых яиц. Температура кипения –61,8С Горит в кислороде. Смеси с воздухом взрывоопасны..
СЕРНИСТЫЙ АНГИДРИД – бесцветный газ с характерным резким запахом. Температура кипения –10С. Легко сжижается. Растворим в воде, спиртах.
МЫШЬЯКОВИСТЫЙ ВОДОРОД – образуется в процессе работы аккумуляторных батарей в которых мышьяк является антикоррозионным модификатором, улучшает механические свойства пластин, повышает срок службы батареи. Бесцветный тяжелый газ без запаха с температурой кипения – 55С. (Чесночный запах обусловлен присутствием продуктов неполного окисления). Растворим в воде. С повышением температуры разлагается с осаждением мышьяка на горячей поверхности в виде зеркала. Легко воспламеняется. Разлагается кислородом воздуха на воду и окись мышьяка. Ядовит. В воздушной среде аккумуляторных ям сжигается печами дожига совместно с водородом. Образующаяся при этом пыль окиси мышьяка улавливается противоаэрозольными или совмещенными фильтрами очистки воздушной среды.
СУРЬМЯНИСТЫЙ ВОДОРОД – бесцветный газ с удушливым запахом, напоминающим запах сероводорода. Температура кипения –17С. Растворим в воде, этиловом спирте. Ядовит. Горит зеленоватым пламенем, выделяя пары окиси сурьмы. С повышением температуры разлагается на горячих поверхностях, образуя «зеркало». Образуется при работе АБ. В состав пластин аккумуляторов сурьма добавляется в количестве до 4,5% для понижения потенциала выделения кислорода.
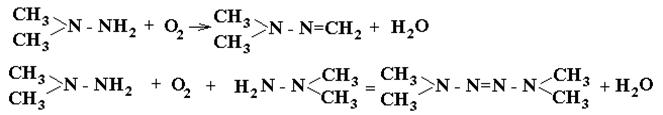
НЕСИММЕТРИЧНЫЙ ДИМЕТИЛГИДРАЗИН – компонент ракетного топлива – горючее. Температура кипения - 63С. Температура плавления –57С. Сильный восстановитель. Крайне ядовитое соединение, обладающее выраженными канцерогенными свойствами. Легко окисляется в воздухе с образованием ряда продуктов превращения: диметилгидразона формальдегида, тетраметилтетразена, диметиламина, диметилнитрозоамина и др.
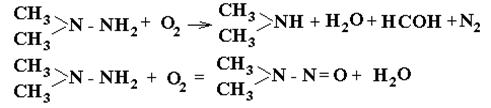 |
Легкая бесцветная жидкость с удушливым аммиачным запахом. Разлив НДМГ на поверхности сопровождается его самовозгоранием. При использовании в качестве средств защиты фильтрующих противогазов возможно возгорание шихты противогаза.
Совместное появление в ракетной шахте паров горючего и окислителя сопровождается мгновенным взрывом. Пролив горючего во внешнюю среду является тяжелой экологической аварией. При однокомпонентном проливе интенсивно разлагается, вступает в многочисленные взаимодействия с образованием свыше 20 различных веществ. Основная масса НДМГ (до 70%) при контакте с воздухом за сутки окисления превращается в диметилгидразон формальдегида.
РТУТЬ – блестящий жидкий металл в диапазоне 357 - -38С. Температура кипения - 356,9С. Испаряется при любых даже отрицательных температурах. Замороженная ртуть по своим свойствам напоминает свинец. Природная ртуть состоит из 7 стабильных изотопов с массами 196, 198, 199, 200, 202, 204. С металлами образует амальгамы. Достаточно легко испаряется. С увеличением температуры давление поров ртути сильно возрастает. Пары ртути очень токсичны. Легко распространяются по кораблю при проливе. Легко сорбируются любыми строительными материалами, которые становятся источниками паров ртути. Удаление ртутного загрязнения с поверхностей крайне трудоемкий процесс. Имелись случаи загрязнения пла ртутью, которые сопровождались тяжелыми последствиями и очень длительным процессом ее удаления - демеркуризации. Ртуть обладает огромной адсорбционной емкостью и хорошо адсорбирует газы и пары. Обычная ртуть по этой причине крайне грязная. При работах ртуть очищают от механических загрязнений, органических веществ, растворенных металлов. Определяется методом Полежаева.
УГЛЕВОДОРОДЫ: БЕНЗИНОВОЙ, КЕРОСИНОВОЙ ФРАКЦИЙ, АРОМАТИЧЕСКИЕ.
УГЛЕВОДОРОДЫ БЕНЗИНОВОЙ ФРАКЦИИ – преимущественно предельные углеводороды выделяющиеся из различных пластиков, смазочных масел и др в процессе их деструкции, разложения, испарения, пиролиза. Обладают опьяняющим действием. Ядовиты. Крайне пожароопасны. Способны к самовоспламенению. Определяются совместно. Наличие в воздушной среде углеводородов говорит об имеющихся протечках различных топлив, смазок. Из воздушной среды удаляются шихтовыми и совмещенными фильтрами. Определяются совместно различными методами (ИК, ГХ, ХМС, ИТ)
УГЛЕВОДОРОДЫ КЕРОСИНОВОЙ ФРАКЦИИ – представляют собой смесь парафиновых, нафтеновых, ароматических и непредельных углеводородов с температурой кипения 180 - 320С. Свойства их аналогичны углеводородам бензиновой фракции. Определяются совместно различными методами (ИК, ГХ, ХМС, ИТ)
АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ –бензол, толуол, ксилолы и др. Преимущественным образом выделяются из окрашенных поверхностей и смазочных масел. Ядовиты, взрывоопасны в смесях с воздухом. Способны вытеснять адсорбированные предельные и непредельные углеводороды из шихты фильтров очистки воздуха. Определяются совместно.
 2014-02-09
2014-02-09 650
650







