При изохорном процессе выполняется условие dv = 0 или v = const. Из уравнения состояния идеального газа (1.3) следует, что
p/T = R/ v =const,
т.е. давление газа прямо пропорционально его абсолютной температуре:
р2/ р1 = T2/ T1. (4.1)
Работа расширения в этом процессе равна нулю, т.к. dv = 0.
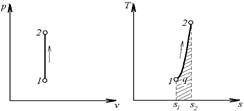
Изображение изохорного процесса в р,v – и Т, s – координатах.
Количество теплоты, подведенной к рабочему телу в процессе 12 при c v = const, определяется
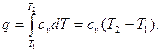 (4.2)
(4.2)
При переменной теплоемкости
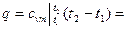
 (4.3)
(4.3)
где 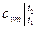 – средняя массовая изохорная теплоемкость в интервале температур от t1 до t2.
– средняя массовая изохорная теплоемкость в интервале температур от t1 до t2.
Так как l = 0, то в соответствии с первым законом термодинамики Du = q и
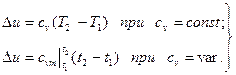 (4.4)
(4.4)
Поскольку внутренняя энергия является функцией состояния тела, то формулы (4.4) справедливы для любого термодинамического процесса идеального газа.
Изменение энтропии в изохорном процессе определяется по формуле
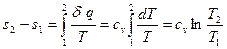 , (4.5)
, (4.5)
т.е. зависимость энтропии от температуры в изохорном процессе при cv = const имеет логарифмический характер.
4.2 Изобарный процесс.
Изобарным называется процесс, происходящий при постоянном давлении. Из уравнения состояния идеального газа (1.3) при p = const находим:
v/ T = R/ p = const,
или v2/ v1 = T2/ T1, (4.6)
т.е. в изобарном процессе объем газа пропорционален его абсолютной температуре (закон Гей-Люссака).
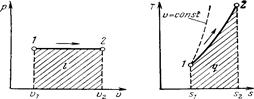
Изображение изобарного процесса в р,v –и Т, s – координатах.
Работа при р = const, будет
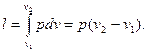 (4.7)
(4.7)
Т.к. pv1 = R T1 и pv2 =R T2, то одновременно
l = R (T2 – T1). (4.8)
Количество теплоты, сообщаемое газу при нагревании (или отдаваемое им при охлаждении), находим:
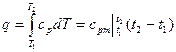 , (4.9)
, (4.9)
где 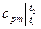 – средняя массовая изобарная теплоемкость в интервале температур от t 1 до t 2; при ср = const.
– средняя массовая изобарная теплоемкость в интервале температур от t 1 до t 2; при ср = const.
q = cp (t 2 –t 1).(4.10)
Изменение энтропии при ср = сonst равно:
s 2 – s 1 = cp ln (T 2/ T 1), (4.11)
т.е. температурная зависимость энтропии при изобарном процессе тоже имеет логарифмический характер, но поскольку cp > cv, то изобара в Т, s – диаграмме идет более полого, чем изохора.
 2014-02-09
2014-02-09 1269
1269