Основные состояния вещества.
В отличие от механики, которая изучает движение отдельных частиц или тел под действием различных сил, молекулярная физика имеет дело со свойствами вещества.
Можно выделить три наиболее характерных состояния, в которых может находиться вещество, — твердое, жидкое и газообразное.
Определение 1.
Как проявление макроскопических свойств рассмотрим существование твердого, жидкого и газообразного состояний.
Из механики известно, что
· минимум потенциальной энергии частицы U(r) отвечает положению её устойчивого равновесия;
· величина кинетической энергии T служит мерой движения частицы.
Таким образом, в зависимости от соотношения между величинами потенциальной и кинетической энергий частица будет или «привязана» к определенной области пространства, или совершать свободное движение.
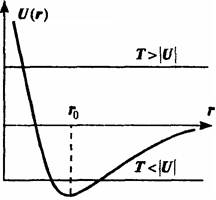 На графике изображена характерная кривая потенциальной энергии частицы во внешнем поле центра притяжения, имеющая глубокий минимум в точке r0.
На графике изображена характерная кривая потенциальной энергии частицы во внешнем поле центра притяжения, имеющая глубокий минимум в точке r0.
Эта кривая отвечает взаимодействию частицы с полем, которое приводит к притяжению частицы на больших расстояниях (r > r0) и к отталкиванию на малых (r < r0).
|
|
|
Двумя прямыми изображены возможные значения полной энергии частицы E = T + U.
В первом случае T >> |U| и частица не может покинуть «потенциальную яму» — эта ситуация отвечает случаю твердого тела.
Во втором случае, когда T >> |U|, частица свободно покидает яму — имеет место случай газа частиц.
Промежуточный случай отвечает жидкости.
Макроскопические свойства тела определяются суммарными и усредненными по большому числу частиц величинами. Такой способ описания является статистическим.
Определение 2.
Макроскопические характеристикисистемы, вычисляемые методами математической статистики, называются термодинамическими переменными.
Пользуясь термодинамическими переменными, можно изучать процессы передачи и преобразования энергии в физических объектах, не обращаясь к микроскопической картине.
 2014-02-09
2014-02-09 2421
2421







