Природные фосфаты (апатиты, фосфориты) используют в основном для получения минеральных удобрений. Качество полученных фосфорных соединений оценивают по содержанию в них Р2О5 — общего, растворимого в воде, аммиачном растворе цитрата аммония (цитратнорастворимого).
Существует ряд методов переработки природных фосфатов: механические, термические и методы кислотного разложения.
Одним из методов механической обработки является измельчение фосфатов. Полученная фосфоритная мука при использовании в кислых почвах очень медленно растворяется в почвенных водах и таким образом становится долговременно действующим удобрением.
Фосфорные удобрения могут быть получены термическим разложением фосфатов при температурах 1200—1800ºС. Так. получают термофосфаты, обесфторенные фосфаты, плавленые магниевые и термощелочные фосфаты.
Однако основным методом получения фосфорных удобрений является химическое разложение фосфатного сырья минеральными кислотами, чаще всего серной. В результате сернокислотной переработки получают простой суперфосфат и фосфорную кислоту, которую, в свою очередь, перерабатывают в двойной суперфосфат, преципитат и сложные удобрения.
|
|
|
Производство простого суперфосфата. Сущность производства простого суперфосфата состоит в превращении природного фторапатита, нерастворимого в воде и почвенных растворах, в растворимые соединения, преимущественно в монокалыдийфос-фатСа(Н2Р04)2.
Процесс разложения может быть представлен следующим суммарным уравнением:
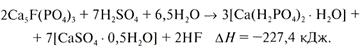 (IV)
(IV)
В процессе производства простого суперфосфата разложение протекает в две стадии. На первой стадии примерно 70% апатита реагирует с серной кислотой. Образуются фосфорная кислота и полугидрат сульфата кальция:
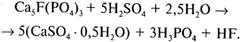 (V)
(V)
Эта стадия представляет собой химическое растворение, осложненное осаждением на зернах фосфата плотных или сравнительно рыхлых пористых корок сульфата кальция. Плотные корки сильно затрудняют диффузию жидкой фазы к поверхности фосфата и реакция замедляется; рыхлые корки замедляют реакцию в меньшей степени. Структура образующейся корки обусловлена скоростью кристаллизации твердой фазы, зависящей главным образом от пересыщения раствора сульфатом кальция, которое определяется, в свою очередь, концентрацией серной кислоты, температурой и другими факторами.
Выкристаллизовавшиеся микрокристаллы сульфата кальция образуют структурную сетку, удерживающую большое количество жидкой фазы, и суперфосфатная масса затвердевает (схватывается). Первая стадия процесса разложения начинается сразу после смешения реагентов и заканчивается в течение 20—40 мин в суперфосфатных камерах.
|
|
|
После полного израсходования серной кислоты начинается вторая стадия разложения, в которой оставшийся апатит (30%) разлагается фосфорной кислотой:
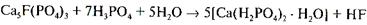 . (VI)
. (VI)
Образующийся монокальцийфосфат в отличие от сульфата кальция не сразу выпадает в осадок. Он постепенно насыщает раствор фосфорной кислоты, после чего начинает выкристаллизовываться в виде Са(Н3РО4)2 • Н2О. Реакция (VI) протекает значительно медленнее, чем реакция (V), что объясняется низкой активностью фосфорной кислоты и кристаллизацией твердых фаз. Она начинается в суперфосфатных камерах и длится еще в течение 5—20 сут. хранения суперфосфата на складе. После дозревания на складе разложение фторапатита считают законченным.
Производство двойного суперфосфата. Двойной суперфосфат — концентрированное фосфорное удобрение, получаемое разложением природных фосфатов фосфорной кислотой. Он содержит 42—50% усвояемого Р2О5, в том числе в водорастворимой форме 27—42% Р2О5 т. е. в 2—3 раза больше, чем простой.
По внешнему виду и фазовому составу двойной суперфосфат похож на простой суперфосфат. Однако он почти не содержит балласта — сульфата кальция.
При разложении природных фосфатов фосфорной кислотой протекает реакция (VI), совпадающая со второй стадией производства простого суперфосфата. Фосфорную кислоту для проведения этой реакции предварительно получают также из фосфатного сырья, например его разложением концентрированной серной кислотой (экстракционная фосфорная кислота), либо высокотемпературным восстановлением элементного фосфора с последующим его окислением и гидратацией (термическая фосфорная кислота).
Двойной суперфосфат можно получать по схеме, аналогичной схеме производства простого суперфосфата. Такой метод называется камерным. Его недостатками являются длительное складское дозревание продукта, сопровождающееся неорганизованными выделениями вредных соединений фтора в атмосферу, и необходимость применения концентрированной фосфорной кислоты.
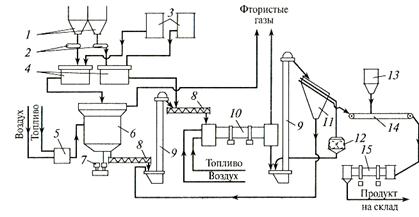
Рис. 3. Схема производства гранулированного двойного суперфосфата из фосфоритной муки и неупаренной экстракционной фосфорной кислоты:
/ — бункер для фосфоритной муки; 2 — весовой дозатор; 3 — напорный бак для фосфорной кислоты; 4 — реактор; 5— топка; 6— распылительная сушилка; 7 — привод гребка; 8 — шнек; 9 — элеватор; 10 — барабанная сушилка; 11 — грохот; 12 — дробилка; 13 — бункер молотого мела; 14 — ленточный транспортер; /5 — барабанный нейтрализатор
Более прогрессивным и экологичным является поточный метод производства двойного суперфосфата. В нем используют для разложения сырья более дешевую неупаренную фосфорную кислоту (рис.3). Метод является полностью непрерывным (отсутствует стадия длительного складского дозревания продукта).
В реакторы 4 подают фосфоритную муку и фосфорную кислоту. В течение примерно 1 ч при 70—90 °С происходит разложение фосфоритов на 55—60%. Вытекающую из реакторов пульпу разделяют на два потока. Часть ее (около половины) высушивают топочными газами в распылительной сушилке. Высушенный мелкозернистый материал подвергают гранулированию. Для этого его смешивают в шнековом смесителе-грануляторе 8 со второй частью пульпы. Сюда же подают небольшое количество ретура. Затем гранулы, содержащие 20—22% влаги, высушивают в прямоточной барабанной сушилке 10 до влажности 3—4%.
В процессе сушки разложение исходного сырья продолжается и общая степень разложения сырья увеличивается до 80—90%.
 2014-02-09
2014-02-09 6141
6141








