Ø Ненасыщенный пар.
Мы много раз употребляли слова газ и пар. Никакой принципиальной разницы между газом и паром нет. Но если при неизменной температуре газ простым сжатием можно превратить в жидкость, то мы называем его паром, точнее, ненасыщенным паром.
Ø Зависимость давления насыщенного пара от температуры.
Состояние насыщенного пара, как говорит опыт, приближенно описывается уравнением состояния идеального газа, а его давление определяется формулой
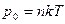
С ростом температуры давление растет. Так как давление насыщенного пара не зависит от объема, оно зависит только от температуры.
| Однако эта зависимость ро(Т), найденная экспериментально, не является прямо пропорциональной, как у идеального газа при постоянном объеме. С увеличением температуры давление насыщенного пара растет быстрее, чем давление идеального газа (рис. 30, участок кривой АВ). Это становится особенно очевидным, если провести изохору через точку А (пунктирная прямая) Почему это происходит? |
Однако эта зависимость р(Т), найденная экспериментально, не является прямо пропорциональной, как у идеального газа при постоянном объеме. С увеличением температуры давление насыщенного пара быстрее, чем давление идеального газа (рис. 30). Почему это происходит?
|
|
|
При нагревании жидкости в закрытом сосуде часть жидкости превращается в пар. В результате согласно формуле 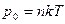 давление насыщенного пара растет не только вследствие повышения температуры жидкости, но и вследствие увеличения концентрации молекул (плотности) пара. В основном увеличение давления при повышении температуры определяется именно увеличением концентрации. Главное различие в поведении идеального газа и насыщенного пара состоит в том, что при изменении температуры пара в закрытом сосуде (или при изменении объема при постоянной температуре) меняется масса пара. Жидкость частично превращается в пар или, напротив, пар частично конденсируется. Когда вся жидкость испарится, пар при дальнейшем нагревании перестанет быть насыщенным и его давление при постоянном объеме будет возрастать прямо пропорционально абсолютной температуре (см. рис. 30, участок ВС).
давление насыщенного пара растет не только вследствие повышения температуры жидкости, но и вследствие увеличения концентрации молекул (плотности) пара. В основном увеличение давления при повышении температуры определяется именно увеличением концентрации. Главное различие в поведении идеального газа и насыщенного пара состоит в том, что при изменении температуры пара в закрытом сосуде (или при изменении объема при постоянной температуре) меняется масса пара. Жидкость частично превращается в пар или, напротив, пар частично конденсируется. Когда вся жидкость испарится, пар при дальнейшем нагревании перестанет быть насыщенным и его давление при постоянном объеме будет возрастать прямо пропорционально абсолютной температуре (см. рис. 30, участок ВС).
Ø Кипение.
По мере увеличения температуры жидкости интенсивность испарения увеличивается. Наконец, жидкость начинает кипеть. При кипении по всему объему жидкости образуются быстро растущие пузырьки пара, которые всплывают на поверхность. Температура кипения жидкости остается постоянной. В жидкости всегда присутствуют растворенные газы, которые выделяются на дне и стенках сосуда, а также на взвешенных в жидкости пылинках. Пары жидкости, которые находятся внутри пузырьков, являются насыщенными. С увеличением температуры давление насыщенных паров возрастает, и пузырьки увеличиваются в размерах. Под действием выталкивающей силы они всплывают вверх. Если верхние слои жидкости имеют более низкую температуру, то в этих слоях происходит конденсация пара в пузырьках. Давление стремительно падает, и пузырьки захлопываются. Захлопывание происходит настолько быстро, что стенки пузырька, сталкиваясь, производят нечто вроде взрыва. Множество таких микровзрывов создает характерный шум. Когда жидкость достаточно прогреется, пузырьки перестанут захлопываться
|
|
|
и всплывут на поверхность. Жидкость закипит. Пузырек пара может расти, когда давление насыщенного пара внутри его немного превосходит давление в жидкости, которое складывается из давления воздуха на поверхность жидкости (внешнее давление) и гидростатического давления столба жидкости.
 2014-02-09
2014-02-09 2695
2695
