В особую группу выделяют несколько видов отравлений, вызываемых токсинами, содержащимися в различных частях некоторых видов рыб. Различают ихтиотоксины, ихтиокринотоксины и ихтиохемотоксины.
Ихтиотоксины — это токсины, содержащиеся в органах воспроизводства рыб (икре и молоках). Таких рыб известно более 50 видов. Симптомы отравления ихтиотоксинами — боли в желудке и диарея. Ярким примером такого отравления является «барбусовая холера», вспышки которой наблюдались в Европе. Яд ципридин, содержащийся в икре рыб (маринок, усачей и османов), вызывает падеие артериального давления, снижение температуры тела и паралич дыхательной системы. При токсичных дозах яда возможна остановка сердца.
Ихтиокринотоксины — это токсины, вырабатываемые кожными железам или отдельными клетками некоторых видов рыб (каменных окуней, мурен и др.). Как правило, эти токсины имеют горький вкус, токсичны для других рыб и обладают гемолитическим действием.
Ихтиохемотоксины — это токсины, содержащиеся в сыворотке крови большеголова атлантического, сельдевых рыб, анчоусов, тунцов, морского и пресноводного угря. Как правило, отравление наступает при приеме с пищей большого количества свежей крови этих рыб. Симптомы отравления выражаются в возникновении рвоты, нерегулярном пульсе, параличе мышц и дыхательной системы; в тяжелых случаях наступает смерть.
5. Интоксикация сигуатера. Сигуатера — название обычно нелетального пищевого отравления, вызываемого рифовыми рыбами в тропических и субтропических странах. Однако этот термин неточен. Ранние испанские поселенцы на Кубе знали, что пресноводная улитка сигуа при употреблении в пищу часто вызывает нарушения пищеварения и нервной системы. Термин «сигуатера» появился внаучной литературе в 1787 г. В настоящее время известно более 400 видов сигуатоксичных рыб.
Действительное число таких отравлений неизвестно, так как сигуатера не подлежит учету и, кроме того, многие врачи неправильно диагностируют это заболевание. По симптомам оно сходно с отравлением фосфорорганическими веществами. На Виргинских островах, например, регистрируется только 10-15 % случаев отравления. Между тем органы здравоохранения считают, что происходит как минимум 30 случаев отравления еженедельно, из них более 20 зарегистрированных смертельных случаев являются результатом употребления в пищу мяса барракуды.
Типичные симптомы данного отравления включают начальный период желудочно-кишечного расстройства (боли в животе, тошнота, рвота и понос), затем наступает растянутый период неврологических нарушений (покалывание и онемение губ, языка и конечностей, головная боль, судороги). В большинстве случаев эти симптомы продолжаются от нескольких часов до нескольких недель и затем проходят. В случаях тяжелой интоксикации симптомы могут длиться 20-25 лет.
Заболевание вызывается токсином, происхождение которого до настоящего времени точно не известно. Предполагают, что его вырабатывают придонные синезеленые водоросли. Косвенным подтверждением этого предположения является то, что большинство сигуатоксичных рыб обитают вблизи дна или, если они хищные, питаются придонной рыбой. Установлено, что сигуатера вызывается не одним соединением. Выделено несколько токсичных веществ, включая растворимый в липидах токсин (сигуатерин), водорастворимый токсин (сигуа-токсин) и токсин с высокой молекулярной массой (мейтотоксин). Структура этих токсинов не установлена. Разработаны методы идентификации сигуатоксичной рыбы, такие как биологическая проба на мышах или на жаброногих ракообразных. Однако эти методы не могут быть использованы для контроля качества, поскольку не всегда дают удовлетворительные результаты. В связи с тем, что токсины стабильны при замораживании и кипячении, разработаны правила для предупреждения отравления: рекомендуется не употреблять те виды рыб, которые опасны в определенной местности; не употреблять их внутренние органы, особенно печень; не употреблять крупную и старую рыбу, которая с возрастом становится сигуатоксичной.
6. Скомброидное отравление. Наибольшее количество отравлений продуктами моря вызывают токсины, образующиеся при бактериальном разложении из-за неправильного хранения рыбы. Такое отравление называется скомброидным. Симптомы скомброидного отравления напоминают аллергическую реакцию на гистамин: покраснение лица, сильная головная боль, рвота, боли в животе. Эта болезнь редко приводит к смертельному исходу.
Бактериальное разложение тканей тунца, макрели, сардин, анчоусов и других рыб вызывает значительное увеличение концентрации гистамина (2000-5000 кг/г) еще до появления первых внешних признаков ее порчи. Однако причину возникновения скомброидного отравления нельзя объяснить только избыточной концентрацией гистамина. Некоторые люди выдерживают большие количества чистого гистамина (около 180 нг) без вредных последствий. По-видимому, существует другая причина скомброидного отравления, до настоящего времени неизвестная.
7. Отравление альготоксинами. Альготоксины — это токсины синезеленых водорослей Cyanophyta, обитающих во внутренних пресноводных водоемах. Массовое размножение синезеленых водорослей, известное как «цветение» воды, - явление экологическое, однако оно имеет важное биологическое и медицинское значение. Развитие синезеленых водорослей приводит к накоплению в теле многих гидробионтов и окружающей водной среде сильнодействующих токсичных веществ, продуцируемых водорослями. Альготоксины аккумулируются в водной экосистеме, иногда подвергаясь трансформации и сохраняя при этом токсичность. Следующим звеном в цепи аккумуляции и передачи альготоксинов являются моллюски и рыбы и далее — теплокровные наземные животные и человек. Известны также отравления травоядных (домашнего скота) на водопое при попадании в пищеварительный тракт как фитопланктона, так и самой воды. Определенную опасность представляет загрязнение альготоксинами водоснабжения и водозаборов. Отравление человека может произойти при купании во время цветения воды. Масштабы этих явлений могут быть достаточно большими, так как во время цветения воды развивается значительная биомасса (более 100-200 г/л) и численность (миллионы клеток на 1 л) синезеленых водорослей.
Токсичные свойства синезеленые водоросли приобретают из-за присутствия в них таких токсичных соединений, как анатоксин, неосакситоксин, сакситоксин, микроцистин, L-лейцин и R-аргинин (так называемый токсин LR). Последние токсины особенно опасны, в литературе их иногда называют фактором быстрой смерти.
Отравление синезелеными водорослями может протекать в нескольких клинических формах, в том числе желудочно-кишечной, кожно-аллергической, мышечной и смешанной.
При попадании токсинов синезеленых водорослей в водопроводную сеть возможны вспышки эпидемического токсического гастроэнтерита, протекающего по типу дизентерие- или холероподобного заболевания. Основные симптомы: тошнота, боли в желудке, спазмы кишечника, рвота, диарея, головная боль, боли мышцах и суставах. При кожно-аллергической форме характерны дерматит, зуд, набухание и гиперемия слизистой глаз (конъюнктивиты), реакции со стороны дыхательных путей по типу бронхиальной астмы.
В особую форму выделяют «юксовско-сартланскую болезнь», обычно развивающуюся после употребления в пищу инфицированной синезелеными водорослями рыбы (щуки, судака, налима, окуня и др.). К факторам, провоцирующим начало заболевания, относят физическое напряжение и охлаждение. Интоксикация развивается через 10-72 ч после употребления в пищу рыбы, причем термическая обработка не снижает токсичности. Возникают очень резкие боли в мышцах ног, рук, поясницы, грудной клетки, усиливающиеся при малейшем движении. Наблюдаются цианоз кожи, сухость во рту, иногда рвота. Опасность представляет асфиксия вследствие паралича дыхательной мускулатуры. Болевой приступ длится от 3 до 4 суток возможны рецидивы.
Для профилактики отравлений рекомендуется длительное кипячение воды, фильтрация ее через активированный уголь, на водопроводных станциях — озонирование. Следует отметить, что основной показатель загрязнения воды альготоксинами — сильный рыбный запах. Следовательно, употреблять рыбу из такого водоема небезопасно. В системе профилактических мероприятий ведущее место занимает также постоянный гидробиологический контроль качества воды.
ЛЕКЦИЯ 3
ТЕМА: БЕЗОПАСНОСТЬ ГЕНЕТИЧЕСКИ МОДИФИЦИРОВАННЫХ ИСТОЧНИКОВ ПИЩИ
Цели: Дать понятие генетически модифицированных источников. Рассмотреть методы определения генетически модифицированных источников в продуктах питания.
В настоящее время с целью увеличения мировых продовольственных ресурсов широко применяются достижения биотехнологии и генной инженерии. Растения, животные и микроорганизмы, полученные с помощью генно-инженерной биотехнологии, называются генетически измененными, а продукты их переработки — трансгенными пищевыми продуктами, или генетически модифицированными источниками (ГМИ).
Генетическая модификация традиционных сельскохозяйственных растений, животных и птицы придает им новые, заданные человеком свойства. В то же время широкое внедрение ГМИ требует решения определенных проблем, связанных с оценкой возможных незаданных эффектов, таких как изменение пищевой ценности отдельных видов продовольствия, аллергические и токсические реакции, отдаленные последствия и т. д.
Методы генной инженерии основаны на переносе генов одних организмов в клетки других организмов — реципиентов, а также на получении рекомбинантных рибонуклеиновых или дезоксирибонуклеиновых кислот, т. е. нуклеиновых кислот с частично измененной последовательностью нуклеотидов.
В результате трансгенной модификации растения становятся устойчивыми к гербицидам, инсектицидам, вирусам, приобретают новые потребительские достоинства. При этом уменьшается количество применяемых гербицидов и инсектицидов, снижается их остаточное содержание в продукции, сокращается количество технологических операций при переработке, уменьшаются потери, повышается качество продукции, экономятся средства и материальные ресурсы.
Большое значение приобретают новые технолог ни получения трансгенных сельскохозяйственных животных и птицы, направленные на повышение продуктивности и оптимизацию выхода отдельных частей и тканей туши (тушек), что оказывает положительное влияние на качество и физико-химические свойства мяса, его функционально-технологические свойства, промышленную пригодность, особенно в условиях дефицита отечественного мясного сырья.
Специфичность и направленность интегрированных генов позволяют менять структуру и цвет мышечной ткани, рН, жесткость, влагоудерживающую способность, степень и характер жирности, мраморность, а также консистенцию, вкусовые и ароматические свойства мяса после технологической обработки. С помощью генной инженерии можно не только добиться желаемых показателей, но и повысить приспосабливаемость животных и птицы к окружающей среде, получить устойчивость к заболеваниям, направленно изменить наследственные признаки.
В области генной инженерии микроорганизмов большая часть исследований направлена на отбор продуцентов ферментов, витаминов, антибиотиков, органических кислот и др. Полученные с помощью генетически измененных бактерий ферменты применяют с целью модификации свойств продовольственного сырья, например, протеолитические ферментные препараты могут использоваться в технологии производства мясных продуктов для умягчения мяса, при изготовлении сыров; амилолитические и липолитические ферменты широко применяются в технологии хлебобулочных изделий и т. д. В настоящее время во многих странах мира продукты, полученные с помощью таких «нетрадиционных» ферментов, должны быть зарегистрированы в установленном порядке.
Основные принципы санитарно-гигиенического нормирования, регистрации, маркировки пищевых продуктов из генетически модифицированных источников.
В связи с необходимостью проведения оценки качества и безопасности продуктов, полученных из генетически модифицированных источников, в Институте питания РАМН разработаны методы и медико-биологические критерии оценки их качества и безопасности.
Ключевым моментом является детальное изучение химического состава новой пищевой продукции, которое должно включать как показатели пищевой ценности, так и санитарно-химические показатели безопасности. Поскольку продукты, полученные из новых нетрадиционных источников или с использованием новых технологий, могут содержать неизвестные компоненты, необходимо проведение токсикологических исследований на лабораторных животных — с включением в их рацион нового продукта, с изучением интегральных показателей состояния животных, биохимических показателей крови, мочи и внутренних органов, гематологических показателей периферической крови, морфологических исследований органов, а также с изучением иммунного статуса организма.
При необходимости проводят специальные исследования: изучают аллергенные свойства, выявляют возможные мутагенные и канцерогенные эффекты, проводят оценку возможных отдаленных последствий для будущих поколений.
На основании результатов проведенных исследований рассматривается вопрос о государственной регистрации и разрешении широкого применения нового продукта или компонента пищи.
Причиной нежелательных последствий могут быть рекомбинантная дезоксирибонуклеиновая кислота (ДНК) и возможность экспрессии на ее основе новых белков, не характерных для данного вида продукции. Именно новые белки могут самостоятельно проявлять или индуцировать аллергенные свойства и токсичность ГМИ. Однако большинство новых ГМИ не обладают аллергенностью и токсичностью.
Согласно СанПиН 2.3.2.1078-01 для пищевых продуктов из генетически модифицированных источников обязательна следующая информация; «генетически модифицированная продукция», или «продукция, полученная из генетически модифицированных источников», или «продукция содержит компоненты из генетически модифицированных источников» (для пищевых продуктов, содержащих более 0,9 % компонентов ГМИ), — а также информация о государственной регистрации. Пищевые продукты, полученные из ГМИ и не содержащие ДНК и белок, в дополнительном этикетировании не нуждаются в случае полной эквивалентности пищевой ценности продукта традиционному аналогу.
Эксперты предлагают проводить исследования безопасности в первую очередь продуктов, содержащих рекомбинантную ДНК и (или) кодируемые ею белки. При отсутствии ДНК или протеина в продукте предлагается не подвергать ГМИ оценке на безопасность. К таким продуктам, не содержащим белок и ДНК, относятся пищевые и ароматические добавки, рафинированные масла, модифицированные крахмалы, мальтодекстрин, сиропы глюкозы, декстрозы и др.
Статья 5 Федерального закона «О государственном регулировании в области генно-инженерной деятельности» от 5 июля 1996 г. № 86-ФЗ обязывает предоставлять полную информацию о методах получения и свойствах продукта, содержащего результаты генно-инженерной деятельности. С учетом действующего законодательства в области защиты прав потребителей данная статья впервые ввела требования об обязательности информирования потребителя о методах получения и свойствах пищевых продуктов из ГМИ.
В Российской Федерации постановлением Главного государственного санитарного врача «О нанесении информации на потребительскую упаковку пищевых продуктов, полученных из генетически модифицированных источников» от 8 ноября 2000 г. № 13 создана система проверки безопасности и установлен порядок государственной регистрации пищевой продукции из ГМИ, предусматривающий проведение комплексных исследований с медико-генетической, медико-биологической и технологической оценкой. При ввозе из-за рубежа пищевой продукции, полученной из ГМЙ, проводится проверка товарно-сопроводительной документации включая наличие свидетельства о государственной регистрации, выданного в установленном порядке Минздравсоцразвития РФ. При отсутствии этого документа принимается решение о запрещении ввоза продукции, а при его наличии изучается санитарное состояние партии продукта и отбираются образцы для лабораторных исследований.
Методы определения генетически модифицированных источников в продуктах питания
В настоящее время основными нормативными документами, включающими описание методов контроля за содержанием в продуктах компонентов из ГМИ, являются следующие:
6. ГОСТ Р 52173-2003 «Сырье и продукты пищевые. Метод идентификации генетически модифицированных источников (ГМИ) растительного происхождения»;
7. ГОСТ Р 52174-2003 «Биологическая безопасность. Сырье и продукты пищевые. Метод идентификации генетически модифицированных источников (ГМИ) растительного происхождения с применением биологического микрочипа»;
Методические указания МУК 4.2.1913-04 «Методы количественного определения генетически модифицированных источников (ГМИ) растительного происхождения в продуктах питания».
Методы, приведенные в указанных ГОСТах, позволяют проводить качественный анализ, т. е. выявлять присутствие или отсутствие в анализируемых продуктах компонентов из ГМИ.
Методы, описанные в МУК 4.2.1913-04, позволяют не только проводить качественное определение ГМИ, но и при получении положительного результата проводить количественное определение конкретного ГМИ (в процентах), который был использован при производстве исследуемого продукта.
Все указанные методы базируются на идентификации рекомбинантной ДНК с использованием различных модификаций метода полимеразной цепной реакции (ПЦР).
Основы метода полимеразной цепной реакции. Метод полимеразной цепной реакции (ПЦР), за разработку которого в 1993 г. была вручена Нобелевская премия, предложен Кэри Мюллисом (фирма «Cetus», США) в 1983 г. В настоящее время ПЦР-технологии широко используются как в научных исследованиях, так и при проведении лабораторной диагностики в здравоохранении, системах санитарно-эпидемиологического и ветеринарного надзора (генотипирование, диагностика инфекционных заболеваний, определение генетически модифицированных организмов, идентификация видовой принадлежности мяса И ингредиентов мясных продуктов и т. д.).
В основе метода ПЦР как инструмента лабораторной диагностики лежит обнаружение небольшого фрагмента ДНК, специфичного для определяемого организма, с использованием полимеразной цепной реакции для накопления искомого фрагмента Методика проведения анализа с использованием метода ПЦР включает три этапа:
ü выделение ДНК из материала пробы;
ü амплификация специфических фрагментов ДИК:
ü детектирование продуктов амплификация.
Выделение ДНК. На данной стадии проведения анализа исследуемый образец подвергается специальной обработке, в результате которой происходит:
3. лизис клеточного материала;
4. очистка от веществ, ингибирующих полимеразную цепную реакцию (полисахариды, липиды. жирные кислоты, белки и т. д.);
5. выделение чистого препарата ДНК. свободного ОТ ингибиторов ПЦР и готового для дальнейшей амплификации.
Амплификации специфических фрагментов ДНК. На дайной стадии происходит накопление коротких специфических фрагментов ДИК в количестве, необходимом для их дальнейшего обнаружения.
В основе амплификации лежит естественный процесс многократного увеличения числа копий специфического участка ДНК, катализируемый ферментом ДНК-полимеразой. Этот процесс комплементарного достраивания ДНК матрицы также называется репликацией ДНК.
Амплификация ДНК включает несколько стадий:
1. денатурация ДНК (рас плетение двойной спирали, расхождение нитей ДНК);
2. образование коротких двухцепочечных участков ДНК («затравок», необходимых для инициации синтеза ДНК);
3. синтез новой цепи ДНК (комплеметарное достраивание обеих нитей).
Данный процесс можно использовать для получения копий коротких участков ДНК, специфичных для конкретных организмов, другими словами, осуществлять направленный синтез таких специфических участков с целью их последующего определения.
Открытие термостабильной ДНK-полимеразы (Таq-полимеразы) позволило сделать процесс репликации ДНК циклическим и использовать его для работы in vitro. При многократном повторении циклов синтеза происходит экспоненциальное увеличение числа копий специфического фрагмента ДНК, что позволяет из небольшого количества анализируемою материала, который может содержать единичные клетки определяемых организмов, получить достаточное количеств ДНК-копий для их идентификации тем или иным методом (электрофорез, иммуноферментный анализ (ИФА) и др.).
Комплементарное достраивание цепи начинается не на любой точке последовательности ДНК, а только в определенных стартовых блоках коротких двунитевых участках. При присоединении таких блоков к специфическим участкам ДНК можно направить процесс синтеза повой цепи только в том участке, а не но всей длине ДНК-цепи.
Для создания стартовых блоков в заданных участках ДНК используют две олигонуклеотидные «затравки», называемые праймерами, которые комплементарны последовательностям ДНK на границах специфического фрагмента и ориентированы таким образом, что достраивание новой цени ДНК происходит только между ними.
дНТФ
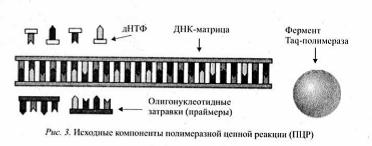
Рис. 3. Исходные компоненты полимеразной цепной реакции (ПЦР)
Таким образом, для проведения амплификации необходимы следующие основные компоненты (рис. 3):
5) ДНК-матрица — ДНК или ее часть, содержащая искомый специфический фрагмент;
6) праймеры — синтетические олнгонуклеотиды (16-30 нуклеотидных нар), комплементарные участкам матричной ДНК, между которыми находится носледовательность-мишень (специфический фрагмент ДНК);
7) специфический фрагмент ДНК и праймеры, выбор которых играет важнейшую роль при проведении амплификации и оказывает влияние на качество проведения анализа;
8) смесь дезоксинуклеотндтрнфосфатов (дНТФ) — смесь четырех дНТФ. являющихся материалом для синтеза новых комплементарных цепей ДНК;
9) фермент Taq-полимсраза — термостабильная ДНК-иолимераза, катализирующая удлинение цепей праймеров путем последовательного присоединения нуклеотидных оснований к растущей цепи, синтезируемой ДНК;
10) буфер-раствор, содержащий катионы и анионы в концентрации, обеспечивающей оптимальные условия ПЦР и стабильное значение рН.
Каждый цикл амплификации включает три этапа, протекающих в различных температурных режимах (рис. 4):
Этап I. Денатурация ДНК (расплетение двойной спирали). Происходит при температуре 93-95 °С в течение 20-40 с.
Этап 2. Присоединение праймеров (отжиг). Происходит комплементарно к соответствующим последовательностям на противоположных цепях ДНК на границах специфического участка. Для каждой пары праймеров существует своя температура отжига, значения которой обычно находятся в интервале 50-65 °С. Время отжига — 20-60 с.
Этап 3. Достраивание цепей ДНК. Комплементарное достраивание цепей ДНК происходит от 5 '-конца к 3 '-концу цепи в противоположных направлениях начиная с участков присоединения праймеров.
Материалом для синтеза новых цепей ДНК служат добавляемые в раствор дезоксинуклеотндтрифосфаты (дНТФ). Процесс синтеза катализируется ферментом — термостабильной ДНК-полимеразой (Taq-полимеразой) и проходит при температуре 70-72 °С (см. рис. 4). Время протекания синтеза — 20-40 с.

Для получения достаточного количества копий искомого характеристического фрагмента ДНК проводят 20-40 циклов амплификации. Образовавшиеся в первом цикле амплификации новые цепи ДНК служат матрицами для второго цикла, в котором также происходит образование искомого специфического фрагмента ДНК, так называемого ампликона. В последующих циклах амплификации ампликоны служат матрицей для синтеза новых цепей (рис. 5).
Таким образом, происходит накопление ампликонов в растворе по формуле 2n, где п — количество циклов амлификации. Поэтому, даже если в исходном растворе находилась только одна двухцепочечная молекула ДНК, за 35 циклов в растворе теоретически должно накапливаться более 30 млрд молекул ампликона. Такого количества достаточно для достоверного визуального определения фрагмента методом электрофореза в агарозном геле.

Фактически же эффективность отдельных циклов амплификации составляет, по некоторым данным, 78-97 %. В случае присутствия в пробе ингибиторов реакции это значение может быть значительно меньше, фактическое количество специфических продуктов амплификации более точно можно определить по уравнению:
А = M(1+E)n
где М— начальное количество ДНК-мишеней; п — количество циклов амплификации; Е — эффективность реакции.
Следует отметить, что в процессе амплификации на исходной цепи синтезируются и длинные фрагменты, однако их накопление происходит лишь в арифметической прогрессии по формуле
К=Мп,
где К— количество длинных продуктов амплификации; п — число циклов.
Таким образом, специфические фрагменты, ограниченные на концах праймерами, впервые появляются в конце второго цикла, накапливаются в геометрической прогрессии и вскоре начинают доминировать среди продуктов амплификации.
Детектирование продуктов амплификации. На данном этапе проводится анализ смеси продуктов ПЦР с целью их идентификации. Используются различные методы, в том числе:
• классический метод горизонтального электрофорезав агарозном геле;
• метод вертикального электрофореза в полиакриламидном геле;
• метод гибридизационных зондов;
• ПЦР «в реальном времени».
 |  |  | |||||
 | |||||||
Метод горизонтального электрофореза в агарозном геле. На сегодняшний день наиболее
распространенным является метод электрофореза. основанный на разделении молекул ДНК по размеру. Для этого готовят пластину агарозного геля, представляющего собой застывшеую после расплавления в электрофорезном буфере агарозу с добавлением специального красителя ДНК, например бромистого этидия, образующего с двухцепочечными фрагментами ДНК прочные соединения внедрения.
При заливке в геле формируют с помощью гребенок специальные лунки, в которые в дальнейшем внося! продукты амплификации. Пластину геля помещают в аппарат для горизонтального гель-электрофореза и подключают источник постоянного напряжения. Отрицательно заряженная ДНК начинает двигаться в геле от «минуса» к «плюсу». При этом более короткие молекулы ДНК движутся быстрее, чем длинные, а молекулы одною размера движутся с одинаковой скоростью. На скорость движения ДНК в геле влияют также концентрация агарозы, напряженность электрического поля, температура, состав электрофорезного буфера и, в меньшей степени,состав ДНК.
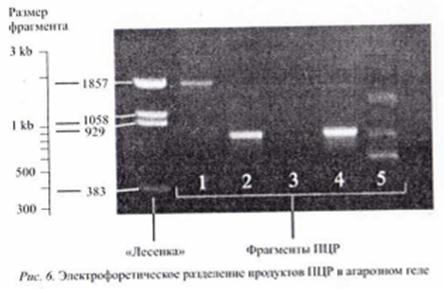
По окончании электрофореза, продолжающеюся от 10 мин до 1 ч, гель помещают на фильтр трансиллюминатopa, излучающего свет в ультрафиолетовом диапазоне (254-310 им). Энергня ультрафиолета, поглощаемая ДНК в области 260 нм, передается на молекулы красителя, заставляя их флуоресцировать в оранжево-красной области видимого спектра, что позволяет peгистрировать их в виде светящихся полос после электрофоретического разделения амплификационной смеси в агарозном геле (рис. 6).
Метод вертикального электрофореза. Отличается от метода горизонтального электрофореза тем, что в данном случае вместо агарозы используют полиакриламидные гели, а разделение продуктов амплификации проводят в специальной камере для вертикального электрофореза.
Электрофорез в полиакриламидном геле имеет большую разрешающую способность по сравнению с агарозным электрофорезом и позволяет различать молекулы ДНК разных размеров с точностью до одного нуклеотида.
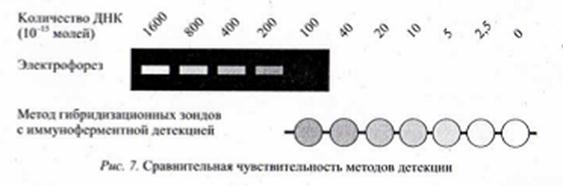
Метод гибридизационных зондов. Электрофоретический метод детектирования имеет ряд недостатков, в частности, низкую чувствительность, субъективность считывания результатов и ограничения по определению различных ДНК в одном амликоне. В качестве альтернативы предложены гнбридизационные схемы детекции. В этих схемах образующиеся в результате амплификации фрагменты ДНК гибридизируются (образуют двухцепочечные комплексы «гибриды») со специфическими олигонуклеотидными зондами. Регистрация таких комплексов может быть проведена колориметрически или флуориметрически. На практике чаще всего используют микропланшетный формат и систему детекции, сходную с используемой при иммуноферментном анализе. Чувствительность метода гнбридизационных зондов с иммуноферментной системой детекции примерно в 100 раз превышает чувствительность метода горизонтального электрофореза (рис. 7).
Гибридизационные методы представляют большой интерес с точки зрения массового скрининга, так как при наличии соответствующего оборудования могут быть легко автоматизированы.
В последнее время для оценки количества детектируемой ДНК в продуктах амплификации применяется метод, известный как ПЦР «в реальном времени». Суть данного метода детекции состоит в использовании специальных реагентов и приборного обеспечения, позволяющего следить за кинетикой накопления продуктов амплификации.
Существует несколько вариантов реализации ПЦР «в реальном времени», один из которых заключается в следующем. В реакционную смесь вводят гибридизационные зонды, имеющие в своем составе меченные особыми реактивами нуклеотиды, способные флуоресцировать лишь в свободном состоянии. На стадии отжига происходит гибридизация зондов с внутренними участками ампликонов. В процессе синтеза ДНК Taq-полимераза разрушает зонды в силу своей экзонуклеазной активности, что приводит к попаданию меченых нуклеотидов в раствор, где они начинают флуоресцировать. Интенсивность флуоресценции, фиксирующаяся в режиме on-line специальным детектором, соответствует количеству продуктов амплификации. Напротив, если гибридизация не происходит, то зонд остается целым и нуклеотиды, входящие в его состав, не флуоресцируют.
При исследовании образцов каждая серия экспериментов сопровождается постановкой амплификации с контролями (несколько 10-кратных разведений ДНК). Сравнение кинетики образования свободных нуклеотидов в реакционных смесях в исследуемом образце и контрольных пробирках позволяет полуколичественно оценить концентрацию ДНК в образце в диапазоне разведений контрольных препаратов ДНК.
Организация ПЦР-лаборатории
Беспрецедентно высокая чувствительность ПЦР-технологий диагностики обусловливает необходимость особенно тщательного устройства ПЦР-лаборатории. Это связано с наиболее острой проблемой метода — возможностью контаминации реакционной смеси специфическими ДНК из внешней среды, в результате чего возникают ложноположительные результаты.
Специфические молекулы ДНК, способные служить мишенями в реакции амплификации, могут попадать во внешнюю среду либо непосредственно из образцов на этапе пробоподготовки, либо из пробирок, в которых была завершена амплификация. При недостаточно продуманной организации ПЦР-лаборатории вероятность загрязнения внешней среды ДНК-мишенями, а затем и постоянной контаминации реакционной смеси очень высока.
Существует несколько способов борьбы с контаминацией, лучшим из которых является правильная организация ПЦР-лаборатории и режима ее работы.
ПЦР-лаборатория должна быть разделена на три зоны — по числу технологических операций (рис. 8). Все три зоны должны представлять собой изолированные комнаты, снабженные предбоксниками.

Рис.8 Схема маршрутов в ПЦР-лаборатории
Желательно наличие устройствафильтрации воздуха. Если первую и вторую зоны в крайнем случае допускается объединить (при наличии специальных боксов), то комната для детекции должна размещаться как можно дальше от двух других зон (другой этаж, другое здание) и иметь не связанную с ними систему вентиляции. Это одно из наиболее строгих требований при организации ПЦР-лаборатории желательно предусмотреть в ПЦР-лаборатории отдельные помещения для переодевания и хранения верхней одежды, приема пищи, складское помещение для лабораторных материалов. Все производственные комнаты должны быть снабжены коротковолновыми ультрафиолетовыми лампами.
Перемещение пробирок, штативов и пр. должно производиться только в од-ком направлении, при этом потоки не должны пересекаться. Исследуемый материал, поступивший в лабораторию, должен быть как можно быстрее обработан в комнате пробоподготовки. В эту же комнату должны поступать пробирки с реакционной смесью из «чистой зоны» для внесения в них препаратов ДНК. Затем пробирки помещают в амплификатор и по окончании термоциклирования, не открывая крышек, переносят в комнату для детекции.
Все операции (подготовка реакционной смеси, пробоподготовка, детекция) должны выполнять разные люди.
Подготовку реакционной смеси следует проводить в ПЦР-боксе, снабженном электрическими розетками, лампами дневного и ультрафиолетового света. Для обработки клинических образцов должны быть установлены ламинарные шкафы, обеспечивающие вертикальный поток воздуха для безопасности персонала при работе с инфекционным материалом, а также предусматривающие возможность работы без ламинарного потока и длительную экспозицию облучения внутренних поверхностей ультрафиолетовым светом.
Инактивацию биологического материала проводят в автоклаве в течение 1 ч при давлении 1,5 атм. Допускается использование настольных автоклавов.
Запрещается внесение пробирок с положительными контролями или клиническими образцами как до, так и после обработки в комнату подготовки реакционной смеси («чистую зону»).
Если все же, несмотря на принятые меры, следы контаминации обнаружены, все поверхности помещения, оборудования, пипеток, посуды и т. д. необходимо обработать 0,1-молярным раствором соляной кислоты, а все используемые порции реагентов заменить новыми.
ЛЕКЦИЯ 4
ТЕМА: МЕТОДОЛОГИЯ ОЦЕНКИ БЕЗОПАСНОСТИ ПИЩЕВЫХ ПРОДУКТОВ И ПРИНЦИПЫ ГИГИЕНИЧЕСКОГО НОРМИРОВАНИЯ
Цель: Рассмотреть методологию оценки безопасности пищевых продуктов и принципы гигиенического нормирования. Сформировать понятия ПДК, ПДУ, ДСД. Изучить методы определения токсичных элементов в пищевых продуктах.
В науке о безопасности питания базисным регламентом являются предельно допустимая концентрация (ПДК), предельно допустимый уровень (ПДУ), допустимое суточное потребление (ДСП) и допустимая суточная доза (ДСД).
Предельно допустимая концентрация (ПДК) — концентрация химических, биологических веществ, не оказывающая в течение всей жизни прямого или косвенного неблагоприятного действия на настоящее или будущие поколения, не снижающая работоспособности человека, не ухудшающая его самочувствия и санитарно-бытовых условий жизни.
Предельный допустимый уровень (ПДУ) — максимальное количество вредного вещества или воздействия физического фактора, которое при ежедневном воздействии не должно вызывать заболеваний или отклонений в состоянии здоровья населения, обнаруживаемых современными методами исследований.
Допустимая суточная доза (ДСД) загрязнителей — максимальная доза (в милиграммах на 1 кг массы), ежедневное пероральное поступление которой на протяжении всей жизни безвредно, т. е. не оказывает неблагоприятного влияния на жизнедеятельность, здоровье настоящего и будущих поколений. Умножая ДСД на массу человека (60 кг), определяют допустимое суточное потребление (ДСП) в милиграммах в сутки в составе пищевого рациона. Зная ДСД, ПДК и средний набор пищевых продуктов в суточном рационе, рассчитывают ПДК ксенобиотика в тех продуктах, в которых он может находиться.
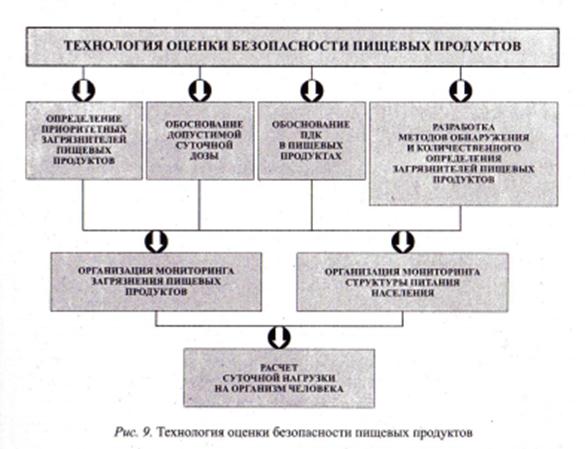
На рис. 9 показаны основные направления работы, определяющие технологию оценки безопасности пищевых продуктов. Присутствие в пищевых продуктах одновременно нескольких загрязнителей может сказываться на общем токсическом эффекте. Теоретически возможны четыре варианта токсического действия:
суммирование эффектов;
сверхсуммирование или потенцирование, когда токсический эффект превышает суммирование;
ингиляция, когда эффект меньше, чем при суммировании;
изменение характера токсического воздействия.
Российскими учеными установлено, что в большинстве случаев, особенно при воздействии малых доз загрязнителей, наблюдается суммирование токсического эффекта. Это позволяет рассчитать аддитивный эффект двух и более факторов, выражая каждый из них в долях предельно допустимой концентрации. Например, если в воздухе концентрация фтора составляет 0,001 мг/м3 (ПДК = 0,005), бензола — 0,16 мг/м3 (ПДК = 0,8), то в сумме их концентрация меньше 1 ПДК (фтора — 1/5 ПДК, бензола — 1/5 ПДК), т. е. суммарное воздействие этих химических веществ в такой концентрации безопасно.
Принцип суммирования часто используют при расчете комплексного влияния различных загрязнителей. Например, если вещество поступает в организм человека с атмосферным воздухом, водой и пищей, то расчет проводят по формуле
Сатм /ПДКатм+Свод /ПДКвод +Спрод/ПДКпрод <1, (1)
где Сатм,Свод,Спрод - концентрация данного вещества в атмосфере, воде, продуктах питания; ПДК — ПДК ксенобиотика в атмосфере, воде, продуктах питания.
Безопасность пищевых продуктов в микробиологическом и радиационном отношении, а также по содержанию химических загрязнителей определяется их соответствием гигиеническим нормативам, установленным в санитарно-эпидемиологических правилах и нормативах СанПиН 2.3.2.1078-01 «Гигиенические требования безопасности и пищевой ценности пищевых продуктов». Указанный документ, устанавливает перечень обязательных к определению приоритетных загрязнителей, их предельно допустимые концентрации и рекомендует методы анализа остаточных количеств контаминантов в пищевых продуктах.

ЗАГРЯЗНЕНИЯ ТОКСИЧНЫМИ ЭЛЕМЕНТАМИ
Существует несколько точек зрения по проблеме загрязнений токсичными элементами.
Согласно одной из них все химические элементы периодической системы делят на три группы: 1) элементы как незаменимые факторы питания (эссенциальные макро- и микроэлементы); 2) неэссснциальныс, или необязательные для жизнедеятельности, элементы; 3) токсичные элементы. Согласно другой точке зрения все элементы необходимы для жизнедеятельности, но в определенных количествах.
Разработана классификация микроэлементов по воздействию на организм человека:
микроэлементы, имеющие значение в питании человека и животных (Со, Сг, Се, F, Fе, I, Mn, Mo, Ni, Se, Si, V, Zn);
микроэлементы, имеющие токсикологическое значение (As, Be, Cd, Со, Cr, F, Hg, Mn, Mo, Ni, Pb, Pd, Se, Sn, Ti, V, Zn).
Следует отметить, что девять из перечисленных элементов отнесены в обе группы. Биологически эссенциальные микроэлементы имеют пределы доз, определяющих их дефицит, оптимальный уровень и уровень токсического действия. Токсичные элементы на этой же шкале в низких дозах не оказывают вредного действия и не выполняют биологических функций, однако в высоких дозах они оказывают токсическое действие. Таким образом, не всегда можно установить различие между жизненно необходимыми и токсичными элементами. Все элементы могут проявить токсичность, если они потребляются в избыточном количестве. Кроме того, токсичность химических элементов обнаруживается при их взаимодействии друг с другом. Например, физиологическое воздействие кадмия на организм, в частности его токсичность, зависит от количества присутствующего цинка, а функции железа в клетках определяются присутствием меди, кобальта и в некоторой степени молибдена и цинка. Тем не менее существуют химические элементы, которые проявляют сильно выраженные токсикологические свойства при самых низких концентрациях и не выполняют какой-либо полезной функции. К таким токсичным элементам относятся ртуть, кадмий, свинец, мышьяк. Они не являются ни жизненно необходимыми, ни благотворными, но даже в малых дозах приводят к нарушению нормальных метаболических функций организма.
Объединенная комиссия ФАО и ВОЗ по пищевому кодексу (Codex Alimentarius) включила ртуть, кадмий, свинец, мышьяк, медь, олово, цинк и железо в число компонентов, содержание которых контролируется при международной торговле продуктами питания. В России согласно действующим санитарным нормам СанПиН 2.3.2.1078-01 подлежат контролю шесть токсичных элементов: ртуть, свинец, кадмий, мышьяк, олово и хром.
Ртуть: источники загрязнения пищевых продуктов. Токсическая опасность ртути и ее соединений
Ртуть достаточно легко извлекается из руд и, несмотря на ограниченное применение, широко известна в течение многих веков. В природе ртуть находится в трех окисленных состояниях: металлическая или атомарная (Hg°), окисленная со степенью окисления +1 (Hg22+) и окисленная со степенью окисления +2 (Hg2+). Свойства ртути с различной степенью окисления (+1, +2) определяются окислительно-восстановительным потенциалом раствора и присутствием комплексных соединений. Ион Hg2+ может образовывать стабильные комплексы с биологическими соединениями, особенно через сульфгидрильные группы. В водном растворе образуются четыре соединения с хлором: HgCl+, HgCl2, HgCI3-, и HgCl42-.
Ртутные соединения относятся к наиболее опасным глобальным загрязнителям биосферы. В большом количестве они содержатся в стоках химических предприятий, бумажных и целлюлозных производств. Ежегодно в результате сжигания каменного угля в атмосферу планеты выбрасывается около 3 000 т ртути. Соединения ртути являются действующей основой многих пестицидов, используемых для протравливания семян растений.
В почве ртутные соединения находятся преимущественно в виде менее токсичной сернистой ртути или могут попадать в нее с протравленными семенами в виде очень ядовитых ртутьорганических соединений, используемых в растениеводстве как фунгициды.
В пищевых продуктах ртуть может присутствовать в трех видах: атомарная ртуть, окисленная ртуть Hg22+ и алкилртуть — соединения ртути с алкилирующими агентами.
Ртуть аккумулируют планктонные организмы (например, водоросли), которыми питаются ракообразные. Ракообразных поедают рыбы, а рыб — птицы. Концевыми звеньями пищевых цепей нередко становятся чайки и орланы. Человек может включаться в цепь на любом этапе и в свою очередь также становиться концевым звеном; в основном это происходит в результате потребления рыбы. Цепочку передачи ртутных соединений можно представить следующим образом:
промышленные выбросы, смывы с полей → водоемы → зоопланктон, ракообразные, моллюски, рыбы, морские животные (кормовая мука из рыб, морских животных) → домашние животные → человек.
С токсикологической точки зрения ртуть наиболее опасна, когда она присоединена к углеродному атому метиловой, этиловой или пропиловой группы (алкильные соединения с короткой цепью). Процесс метилирования ртути является ключевым звеном в ее биокумуляции по пищевым цепям водных экосистем. Если в основных пищевых продуктах содержание ртути составляет менее 60 мкг/кг продукта, то в пресноводной рыбе из незагрязненных рек и водохранилищ оно составляет 100-200 мкг/кг, а из загрязненных — 500-700 мкг/кг. Среднее количество ртути в морских рыбах — 150 мкг/кг.
За естественный уровень содержания ртути в рыбе принимают величину 0,1-0,2 мг/кг. ВОЗ предложила считать предельно допустимой концентрацией значение 0,5 мг/кг. Это значение, вероятно, завышено, поэтому рекомендуется есть рыбу только 1-2 раза в неделю, а беременным женщинам — вовсе не употреблять ее в пищу.
Избыточное потребление рыбы человеком даже при достаточно низкой концентрации в ней метилртути (например, порядка 0,8 мг/кг) приводит к отложению ртути в волосах человека и сопровождается появлением первых признаков отравления. Концентрация ртути в волосах до 10 мг/кг считается безопасной, она возможна даже при потреблении воды и рыбы, практически не содержащих ртути. Содержание ртути в волосах в количестве около 300 мг/кг уже опасно для жизни.
Органические соединения ртути - стойкие вещества, очень медленно разрушающиеся и выводящиеся из организма. Метилртуть выводится из организма частично через почки, а в основном - через печень и желчь, а также с фекалиями. Продолжительность выведения соединений ртути из организма (полупериод их биологического распада) составляет около 70 дней. Токсическая опасность ртути выражается во взаимодействии с SH-группами белков. Блокируя их, ртуть изменяет биологические свойства тканевых белков и инактивирует ряд гидролитических и окислительных ферментов. Ртуть, проникнув в клетку, может включиться в структуру ДНК, что оказывает влияние на наследственность человека. Мозг проявляет особое сродство к метилртути и способен аккумулировать почти в шесть раз больше ртути, чем остальные органы. Более 95 % ртути в тканях мозга находится в органической форме. В других тканях органические соединения деметилируются и превращаются в неорганическую ртуть. В эмбрионах ртуть накапливается так же, как и в организме матери, но содержание ртути в мозге плода может быть выше.
В продуктах животноводства повышенное содержание ртути может наблюдаться в результате скармливания животным рыбы, рыбной муки, а также после употребления в корм зерна, обработанного ртутными препаратами. Скармливание животным зерна, обработанного ртутьорганическими пестицидами, сопровождается длительным выделением ртути с молоком, а также может вызвать ее накопление в большом количестве в органах и тканях животных, употребляемых в пищу.
Допустимое недельное поступление соединений ртути не должно превышать 0,3 мг на человека, в том числе метилртути не более 0,2 мг.
Кадмий, его токсичность и источники загрязнения
Кадмий представляет собой один из наиболее опасных токсикантов внешней среды. В природной среде кадмий встречается в очень малых количествах. Наибольшие количества содержатся в почве (в среднем 0,1 мг/т). В более высокой концентрации кадмий имеется в минеральных удобрениях, особенно фосфорсодержащих, и некоторых фунгицидах.
Значительным источником загрязнения являются кадмированная арматура, окрашенные кадмиевыми соединениями пластмассы, используемые в пищевой промышленности для машин и оборудования. Например, кадмиевые пигменты необходимы для производства лаков, эмалей и керамики, соединения кадмия применяются в качестве стабилизатора пластмасс (поливинилхлорида), в электрических батареях. В результате промышленных выбросов, а также при сжигании кадмийсодержащих пластмассовых отходов кадмий может попадать в воздух.
Кадмий опасен в любой форме: принятая внутрь доза 30-40 мг уже может оказаться смертельной. Поэтому даже потребление напитков из пластмассовой тары, материал которой содержит кадмий, является чрезвычайно опасным. Может происходить хроническое отравление, ранними симптомами которого являются поражение почек и нервной системы с последующим возникновением острых костных болей. Типично также нарушение функции легких.
Токсичность кадмия проявляется весьма сильно, в связи с чем этот металл рассматривается в числе приоритетных загрязнителей. Кадмий способен замещать цинк в энзиматических системах, необходимых для формирования костных тканей, что сопровождается тяжелыми заболеваниями. Имеются данные об эмбриотропном и канцерогенном действии кадмия.
В организме кадмий накапливается в первую очередь в почках. После достижения пороговой концентрации (около 0,2 мг кадмия на 1 г массы почек) появляются симптомы тяжелого отравления и почти неизлечимого заболевания.
Кадмий почти невозможно изъять из природной среды, поэтому он все больше накапливается в ней и попадает различными путями в пищевые цепи человека и животных. Поглощенное количество кадмия выводится из организма очень медленно (0,1 % в сутки). Кадмий имеет высокий коэффициент биологической кумуляции, полупериод биологического распада кадмия — время, необходимое для снижения накопившегося в органе или организме металла в два раза по сравнению с исходным содержанием — составляет 19-40 лет. Поэтому возникает реальная угроза неблагоприятного воздействия на человеческий организм потребления кадмия даже в низких дозах.
Больше всего кадмия мы получаем с растительной пищей. Кадмий легко переходит из почвы в растения, которые поглощают до 70 % кадмия из почвы и лишь 30 % - из воздуха.
Всемирная организация здравоохранения считает максимально допустимой дозой кадмия для взрослых людей 500 мкг в неделю, т. е. ДСП составляет 70 мкг/сут., а ДСД - 1 мкг на 1 кг массы тела.
Свинец, его токсичность и источники загрязнения
Свинец относится к наиболее известным ксенобиотикам и среди современных токсикантов играет весьма заметную роль. Свинец находится почти повсеместно. В почвах обычно содержится от 2 до 200 мг/кг свинца. Свинец, как правило, сопутствует другим металлам, чаше всего цинку, железу, кадмию и серебру. Традиционно его используют для изготовления пуль и снарядов, для пайки швов жестяных банок, при производстве двигателей, в полиграфии.
Повышенное содержание свинца в окружающей среде обусловлено главным образом техногенным загрязнением воздуха, почвы и воды. Источниками загрязнения являются энергетические установки, работающие на угле, жидком топливе, двигатели внутреннего сгорания. В настоящее время в роли токсикантов окружающей среды выступают прежде всего алкильные соединения свинца, такие как тетраэтилсвинец, которые примешивают к автомобильному бензину в качестве антидетонаторов.
Отмечается увеличенная загрязненность свинцом промышленных районов и городов. Выбросы промышленных производств, выхлопные газы автотранспорта попадают в почву, и концентрация свинца в растениях из зон, прилегающих к автотрассам, может увеличиваться в десятки раз. Скармливание травоядным животным травы или сена из придорожных или пригородных зон приводит к накоплению свинца в организме животных. Часть свинца может выводиться из организма с молоком (в этом случае молоко становится опасным для употребления в пищу), а часть накапливается в органах и тканях сельскохозяйственных животных.
При обработке продуктов основным источником поступления свинца является жестяная банка, которая используется для упаковки 10-15 % пищевых изделий. Свинец попадает в продукт из свинцового припоя в швах банки. Установлено, что около 20 % свинца в ежедневном рационе людей (кроме детей до 1 года) поступает из консервированной продукции, в том числе 13-14 % из припоя, а остальные 6-7 % — из самого продукта. В последнее время с внедрением новых методов пайки и закатки банок содержание свинца в консервированной продукции уменьшается.
Около 10 % поглощенного с пищей, водой и из воздуха свинца абсорбируется в желудочно-кишечном тракте. На степень абсорбции могут влиять различные факторы. Например, снижение содержания кальция приводит к усилению абсорбции свинца. Витамин D увеличивает поглощение как кальция, так и свинца. Недостаток железа также способствует абсорбции свинца, что наблюдается при голодании. К такому же эффекту приводит диета с повышенным содержанием углеводов, но дефицитом белков.
При попадании в кровеносную систему свинец разносится по всему телу, включаясь в клетки крови и плазму. В крови свинец в основном включается в эритроциты, где его концентрация почти в 16 раз выше, чем в плазме. Полупериод биологического распада свинца в человеческом организме составляет 5 лет, в костях - 10 лет.
Метаболизм свинца имеет много общего с метаболизмом кальция. Оба металла содержатся в кристаллической структуре костей, которые в основном состоят из фосфата кальция. Свинец токсически воздействует на четыре системы органов: кроветворную, нервную, желудочно-кишечную и почечную. Острое отравление свинцом обычно проявляется в виде желудочно-кишечных расстройств. Вслед за потерей аппетита, диспепсией, запорами могут последовать приступы колик с интенсивными болями в животе. Заболевания головного мозга в результате воздействия свинца у взрослых встречаются редко, но у детей бывают довольно часто. Сокращение периода жизнедеятельности эритроцитов при отравлении свинцом может стать причиной анемии.
Хорошо изучено воздействие свинца на нервную систему, как центральную, так и периферическую. Кроме острой энцефалопатии, существуют и более мягкие симптомы реагирования нервной системы на поступление свинца, в частности, снижение умственных способностей и агрессивное поведение. Поражение периферической нервной системы выражается в так называемых свинцовых параличах мышц рук и ног.
Установлено, что даже небольшое регулярное поступление свинца в организм, если оно продолжительное, приводит к хроническому заболеванию. Согласно докладу ВОЗ продолжительное воздействие свинца при его концентрации и крови свыше 70 мкг/мл может вызвать хроническую необратимую нефропатию.
Экспертами ФАО и ВОЗ установлена величина максимально допустимой доза свинца для взрослого человека - 3 мг в неделю, т. е. ДСД составляет около 0,007 мг на 1 кг массы тела, ПДК в питьевой воде - 0,05 мг/л.
Мышьяк, его токсичность и источники загрязнения
Мышьяк широко распространен в окружающей среде. Он встречается почти во всех почвах. Степени окисления мышьяка: -3, 0, +3, +5. Наиболее распространенными неорганическими соединениями мышьяка являются оксид мышьяка (III) As2О3 и оксид мышьяка (V) As2O5. Другими важными соединениями мышьяка являются хлорид мышьяка (III) и различные соли, такие как арсенат свинца, ацетарсенат меди, а также газообразное водородное соединение арсин (AsH3). По степени токсичности соединения мышьяка располагаются в следующий ряд: AsH3 > As3+ > As5+ > RAsX.
В результате широкого распространения в окружающей среде и использования в сельском хозяйстве мышьяк присутствует в большинстве пищевых продуктов. Обычно его содержание в пищевых продуктах достаточно мало (менее 0,5 мг/кг) и редко превышает 1 мг/кг, за исключением некоторых морских организмов, которые аккумулируют этот элемент. При отсутствии значительных загрязнений содержание мышьяка в хлебных изделиях составляет до 2,4 мг/кг, фруктах - до 0,17, напитках - до 1,3, мясе - до 1,4, молочных продуктах - до 0,23 мг/кг. В морских продуктах содержится больше мышьяка - обычно 1,5-15,3 мг/кг.
Мышьяк присутствует почти во всех пресных водах. В питьевой воде из различных источников содержание мышьяка определяется природой залегающих пород. В некоторых геологических формациях залегает арсенопирит, который является источником мышьяка в пресных водах и приводит к увеличению его концентрации до 0,5-1,3 мг/л.
Основную опасность представляет техногенное загрязнение окружающей среды соединениями мышьяка вокруг медеплавильных заводов, предприятий, перерабатывающих цветные металлы, сжигающих бурые угли. В зоне действия таких предприятий создается высокая концентрация мышьяковистого ангидрида и других соединений мышьяка в воздухе, происходит их накопление в воде, почве, растениях с последующим перераспределением в организм животных, потребляющих загрязненные корм, воду, а также в молоко и мясо, получаемые от этих животных.
Медики установили, что в малых количествах мышьяк оказывает благотворное действие на организм человека: улучшает кроветворение, повышает усвоение азота и фосфора, ограничивает распад белков и ослабляет окислительные процессы. Эти свойства мышьяка используются при назначении с лечебной целью мышьяковистых препаратов. Неорганические препараты (раствор арсената(Ш) натрия, мышьяковистый ангидрид и др.) назначают при истощении, малокровии, некоторых кожных заболеваниях. В зубоврачебной практике применяют пасту с мышьяковистым ангидридом («белый мышьяк»). Органические препараты мышьяка используются при лечении возвратного тифа, малярии и ряда других инфекционных заболеваний.
Однако применение лечебных мышьяковистых препаратов в животноводстве в течение длительного времени или в высоких дозах может привести к накоплению мышьяка в получаемых от животных мясе, молоке, а при противочесоточных обработках — в шерсти.
По данным экспертов ФАО и ВОЗ, суточная доза мышьяка для взрослого человека составляет в среднем 0,05-0,42 мг. При потреблении продуктов с повышенной концентрацией мышьяка возникает опасность интоксикации и других отрицательных последствий.
Трех- и пятивалентные формы мышьяка легко поглощаются в желудочно-кишечном тракте. Количество реально поглощенного мышьяка зависит от вида химического соединения мышьяка и состава пищи. Поглощенный мышьяк быстро распространяется по всем органам и тканям в виде протеинового комплекса с α-глобулином. Примерно через 24 ч после поступления в организм его концентрация в большинстве органов начинает уменьшаться. Однако в коже количество мышьяка может увеличиться через несколько дней после его поступления в организм. Обнаружено, что мышьяк аккумулируется в коже, ногтях, волосах, а также в костях и мышцах.
Мышьяк связывается с сульфгидрильными группами белков и таким образом ингибирует действие многих ферментов, участвующих в процессах клеточного метаболизма и дыхания.
Хроническое отравление мышьяком приводит к потере аппетита и снижению веса, кишечным расстройствам, периферийным неврозам, конъюнктивиту, гиперкератозу и меланоме кожи. Меланома возникает при длительном воздействии мышьяка и может привести к развитию рака кожи.
Экспертами ФАО и ВОЗ установлена ДСД мышьяка 0,05 мг на 1 кг массы тела, что для взрослого человека составляет около 3 мг/сут.
Токсические свойства меди, стронция, цинка, железа, сурьмы, олова, никеля, хрома, алюминия
Медь является одним из первых металлов, которые человечество начало
использовать в чистом виде.
Значительное количество меди применяется в электротехнической промышленности, для изготовления водопроводных и отопительных систем, в сельском хозяйстве и фармакологии.
Медь присутствует почти во всех пищевых продуктах. Суточная потребность в меди взрослого человека - 2,0-2,5 мг, т.е. 35-40 мкг/кг, детей - 80 мкг/кг. Однако при нормальном содержании в пище молибдена и цинка - физиологических антагонистов меди - суточное потребление меди, по оценке экспертов ФАО, может составлять не более 0,5 мг/кг (до 30 мг в рационе).
Стронций — достаточно широко распространенный в литосфере металл. Концентрация стронция в плодах, растущих на нормальной почве, колеблется от 1 до 169 мг/кг. В животных тканях его содержится 0,06-0,50 мг/кг. Взрослый человек обычно поглощает с пищей 0,4-2,0 мг стронция в сутки.
Стронций плохо абсорбируется в кишечном тракте, поэтому большая часть металла, попадающего в организм, из него выделяется. Оставшийся в организме стронций замещает кальций и в небольших количествах накапливается в костях.
Цинк. Цинковые руды широко распространены. Цинк присутствует во
многих пищевых продуктах и напитках, особенно в продуктах растительного
происхождения.
В настоящее время установлено, что человеку необходимо получать цинк с пищей. Во многих странах существуют рекомендации по суточной норме потребления металла. Цинк участвует в ряде важных биологических процессов, особенно ферментативных. Однако избыток цинка вызывает токсическое воздействие на организм.
Токсичные дозы солей цинка действуют на желудочно-кишечный тракт, что приводит к острому, но излечимому заболеванию, сопровождающемуся тошнотой, рвотой, болями в желудке, коликами и диареей.
Железо является вторым наиболее распространенным металлом после алюминия и пятым по распространенности химическим элементом в земной коре. Почти все пищевые продукты содержат железо в разных количествах.
Железо является необходимым микроэлементом. Однако, несмотря на го что содержание железа тщательно регулируется в организме, иногда может поглощаться его избыточное количество. Это приводит к накапливанию металл в организме, в результате чего развивается болезнь сидероз.
Сурьма. В природе сурьма обычно встречается в виде сульфидных минералов - сурьмяного блеска (антимонита).
По механизму токсического действия и клинической картине отравления сурьма аналогична мышьяку. Токсичная доза для взрослого человека составляет 100 мг/сут., летальная - 500-1000 мг/сут.
Профилактические мероприятия заключаются в строгой регламентации содержания и характера соединений сурьмы в эмали, полуде и припое. В России для полуды посуды допустимая концентрация сурьмы в олове составляет не более 0,05 %.
Олово известно еще с древности. Более половины добываемого олова идет на производство покрытий. При производстве консервных банок используются мягкие стали с гальваническим покрытием. Однако при длительном хранении консервов олово может переходить в продукты и при накоплении в больших количествах отрицательно действует на организм. Поэтому жестяные банки после лужения дополнительно покрывают лаками, а количество олова в консервах контролируют. Срок хранения консервов, вырабатываемых в жестяной банке, устанавливают с учетом предупреждения накопления больших количеств олова (на 1 кг продукта - не более 200 мг олова для взрослых и 100 мг для детей).
Высокая концентрация олова в пище может привести к острому отравлению. Для человека токсичная доза олова составляет 5-7 мг/кг.
Никель. В природе никель обычно встречается совместно с мышьяком, сурьмой и серой. В небольших количествах никель присутствует почти во всех почвах. Растения могут содержать его от 0,5 до 3,5 мг/кг. В значительных количествах он содержится в большинстве тканей животных. Суточная норма поступления никеля в организм человека с пищей составляет 0,3-0,6 мг.
Источниками загрязнения никелем пищевых продуктов могут являться почва и применяемое в пищевой промышленности оборудование. В частности, существует опасность поступления избыточного количества никеля с маргаринами и спредами, так как никель входит в состав катализатора, используемого для гидрирования растительных масел.
Никель плохо абсорбируется из пищевых продуктов и напитков. В тканях организма остается около 3-6 % ежедневно поглощаемого металла. Распределяется никель в организме почти однородно, без преимущественного накопления в каких-либо органах.
Хром широко распространен в земной коре, его количество составляет 0,04% твердой породы. В основном хром применяется в металлургической промышленности для получения нержавеющих сталей и для покрытия металлических изделий с целью коррозионной защиты. В небольших количествах хром содержится в большинстве пищевых продуктов и напитков. Среднее суточное потребление хрома с пищей составляет 50-80 мкг. Потенциальным источником повышенной концентрации хрома в пищевых продуктах является загрязнение окружающей среды сточными водами.
С точки зрения биологического действия на организм хром является необходимым элементом. Основная его роль заключается в поддерж
 2014-02-12
2014-02-12 3497
3497
