Прежде, чем рассматривать природу гидрофобного взаимодействия, необходимо ввести понятие «гидрофильных» и «гидрофобных» функциональных групп.
Группы, которые могут образовывать водородные связи с молекулами воды, называются гидрофильными.
К этим группам относятся полярные группы: аминогруппа (-NH2), карбоксильная (-COOH), карбонильная группы (-CHO) и сульфгидрильная группа (-SH).
Как правило, гидрофильные соединения хорошо растворимы в воде. !!! Это обусловлено тем, что полярные группы способны образовывать водородные связи с молекулами воды.
Появление таких связей сопровождается выделением энергии, поэтому и возникает тенденция к максимальному увеличению поверхности контакта заряженных групп и воды (Рис. 2.3):

Рис. 2.3. Механизм образования гидрофобных и гидрофильных взаимодействий
Молекулы или части молекул, неспособные образовывать водородные связи с водой называются гидрофобными группами.
К этим группам относятся алкильные и ароматические радикалы, которые неполярны и не несут электрического заряда.
Гидрофобные группы – плохо или вовсе не растворимы в воде.
Это объясняется тем, что атомы и группы атомов, входящие в состав гидрофобных групп, являются электронейтральными и (поэтому) не могут образовывать водородных связей с водой.
!!! Гидрофобные взаимодействия возникают в результате контакта между неполярными радикалами, неспособными разорвать водородные связи между молекулами воды.
В результате этого молекулы воды вытесняются на поверхность гидрофильных молекул (Рис. 2.3).
2.1.5. Ван-дер-ваальсовы взаимодействия.
В молекулах существуют также весьма слабые и короткодействующие силы притяжения между электрически нейтральными атомами и функциональными группами.
Это так называемые ван-дер-ваальсовые взаимодействия.
Они обусловлены электростатическим взаимодействием между отрицательно заряженными электронами одного атома и положительно заряженным ядром другого атома.
Так как ядра атомов экранированы окружающими их собственными электронами от ядер соседних атомов, то возникающие между различными атомами ван-дер-ваальсовы взаимодействия весьма невелики.
Все эти типы взаимодействий принимают участие в формировании, поддержании и стабилизации пространственной структуры (конформации) белковых молекул (Рис. 2.4):
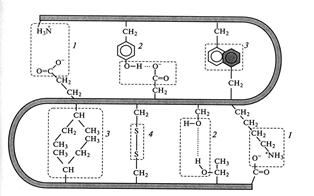
Рис. 2.4. Механизм образования ковалентных связей и слабых нековалентных взаимодействий: 1 - электро-статические взаимодействия; 2 – водородные связи;
3 – гидрофобные взаимодействия, 4 – дисульфидные связи
Силы, которые способствуют формированию пространственной структуры белков и удерживающие её в стабильном состоянии, являются очень слабыми силами. Энергия этих сил на 2-3 порядка меньше энергии ковалентных связей. Они действуют между отдельными атомами и группами атомов.
Однако, огромное число атомов в молекулах биополимеров (белков), приводит к тому, что суммарная энергия этих слабых взаимодействий становится сравнима с энергией ковалентных связей.
Белки
В предыдущей лекции мы с вами говорили о том, что аминокислоты, соединяясь друг с другом посредством пептидных связей, образуют полипетиды.
!!! Белками являются полипетиды, способные образовывать и самостоятельно стабилизировать свою пространственную структуру.
Эта способность приобретается благодаря наличию большого числа слабых нековалентных взаимодействий и связана с числом аминокислотных остатков, образующих полипептидную цепочку.
Как правило, белками называют полипетиды, содержащие более 50 аминокислотных остатков.
Вместе с тем длина полипептидной цепи может достигать до нескольких тысяч остатков аминокислот; молекулярная масса белков колеблется от 6000 до 1 миллиона и более килодальтон.
 2015-01-21
2015-01-21 8421
8421








