Третий закон термодинамики формулируется как принцип недостижимости абсолютного нуля температур. Как известно, все вещества при температуре Т →ОК находятся в конденсированном состоянии.
Для конденсированных термодинамических систем в соответствии с тепловой теоремой Нернста кривые тепловых эффектов 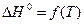 и свободной энергии Гиббса
и свободной энергии Гиббса 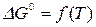 при температуре Т=0К сходятся и имеют общую касательную.
при температуре Т=0К сходятся и имеют общую касательную.
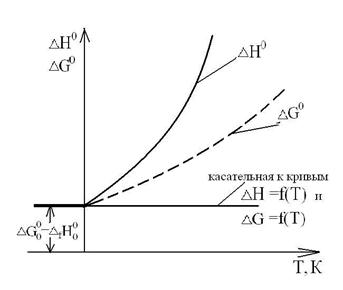
Эта касательная параллельна оси температур, т.к. свойства твердых и жидких веществ вблизи Т=0К перестают зависеть от температуры.
По определению 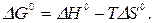
При Т=0К 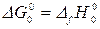 , а
, а
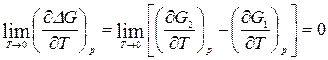 ,
,
где 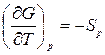 по определению.
по определению.
Тогда
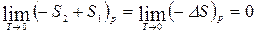 ,
,
Следовательно, при Т →0, 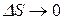 и
и 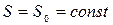 , т.е. процесс является адиабатным, т.к.
, т.е. процесс является адиабатным, т.к. 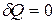 и dS =0. Планк предложил считать, что при Т
и dS =0. Планк предложил считать, что при Т 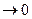
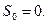
Таким образом, вблизи абсолютного нуля температур изотермический процесс является одновременно и адиабатным процессом, и термодинамическая система не обменивается с окружающей средой теплотой. При этом достичь температуры Т=0К невозможно как путем адиабатного расширения рабочего тела, т.к. 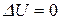 и
и 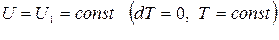 , так и путем изотермического расширения рабочего тела, поскольку рабочее тело перестает отдавать тепло окружающей среде, т.к.
, так и путем изотермического расширения рабочего тела, поскольку рабочее тело перестает отдавать тепло окружающей среде, т.к. 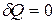 и dS =0.
и dS =0.
3-ий закон термодинамики позволяет определить начало отсчета энтропий и вычислить абсолютное значение энтропии веществ при различных температурах, если известны теплоемкости и тепловые эффекты фазовых превращений в диапазоне температур от Т 0=0 до Т:
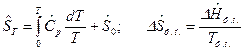 , где
, где 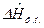 - тепловой эффект фазового превращения;
- тепловой эффект фазового превращения; 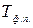 - температура фазового превращения.
- температура фазового превращения.
 2015-01-21
2015-01-21 522
522








