С точки зрения возможности практического применения ценность энергии определяется не только ее количеством, но прежде всего тем, насколько она в конкретных условиях может быть использована. Мера пригодности любого вида энергии для получения энергии в обратимом процессе взаимодействия с окружающей средой была названа эксергией [от ех (лат.) - извне, ergon (лат.) - работа].
Эксергия Е равняется величине наибольшей (максимально полезной) работы, которые ее может выполнить энергоноситель в обратимом процессе перехода из неравновесного состояния в состояние равновесия с окружающей средой. Поскольку эксергия характеризует работоспособность энергоносителя относительно окружающей среды, она дает возможность оценить качество энергии. Согласно определению эксергия зависит не только от параметров системы, но и (в противоположность энергии) от параметров окружающей среды. Итак, возможный случай, когда большую тепловую энергию системы нельзя полезно использовать, если и окружающая среда имеет такую самую температуру. Аналогичная ситуация может быть и при одинаковых давлениях (даже высоких) в системе и окружающей среде. В обеих случаях эксергия системы равняется нулю. И наоборот, чем выше температура или давление энергоносителя относительно параметров окружающей среды, тем больше практическая пригодность энергии выполнять работу и превращаться в другие виды.
В расчете эксергии все источники энергии разделяют на энтропийные и неэнтропийные.
Неэнтропийные источники энергии (электрическая, магнитная, механическая) не имеют энтропии, а потому они полностью превращаются в любые другие виды энергии и такие превращения ограничиваются условиями первого закона термодинамики. Эксергия неэнтропийного источника равняется его энергии Энтропийные источники энергии (энергия излучения, внутренняя энергия вещества, энергия теплового потока, химическая энергия и т.п.) имеют энтропию, поэтому преобразование энергии с одной формы в другую происходят не полностью исопровождаются энергетическими потерями. При этом изменению энтропии ∆Sотвечает появление определенного количества "связанной"" энергии, превращение которой в эксергию в условиях равновесия с окружающей средой принципиально невозможно.
Свойства энергии и эксергии отличаются между собой, что можно увидеть из такого сравнения:
| Энергия системы 1. Зависит от параметров системы и не зависит от параметров окружающей среды. 2. Всегда имеет величину, которая отличается от нуля и равняется, по уравнению Эйнштейна, тс2. 3.Подчиняется закону сохранения энергии в любых процессах и уничтожаться не может. 4. Превращаемость одних форм энергии в другие ограничивается условиями второго закона термодинамики (в том числе и для обратимых процессов). | Эксергия системы 1.Зависит как от параметров системы, так и от параметров окружающей среды. 2.Может иметь величину, которая равна нулю (в состоянии равновесия с окружающей средой). 3.Подчиняется закону сохранения энергии лишь в обратимых (идеальных) процессах, в реальных необратимых процессах частично или полностью уничтожается. 4. Превращаемость одних форм энергии в другие для обратимых процессов не ограничивается условиями второго закона термодинамики. |
При условии стабильного химического состава потока вещества удельную эксергию Е (в расчете на единицу массы) рассчитывают по уравнению
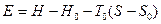 (39)
(39)
где Н и S - соответственно энтальпия и энтропия вещества в этом состоянии; H0 и S0 то же самое для вещества в состоянии термодинамического равновесия с окружающей средой; Т0 - температура окружающей среды.
При этом потери эксергии в адиабатической системе определяются произведением температуры окружающей среды на прирост энтропии вследствие необратимости процесса. Они равны
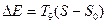 (40)
(40)
Если давление системы отличается от давления окружающей среды, то удельную эксергию рассчитывают по такому уравнению:
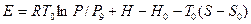 (41)
(41)
где Р - давление системы; Ро - давление окружающей среды.
Критерием термодинамической эффективности процесса есть эксергетический коэффициент полезного действия ηэкс который в общем виде записывается так:
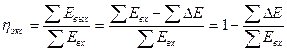 (42)
(42)
Где 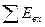 - сумма потоков эксергии на входе в систему,
- сумма потоков эксергии на входе в систему, 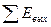 сумма потоков эксергии на выходе из системы.
сумма потоков эксергии на выходе из системы.
По разности величин 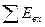 и
и 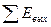 определяют суммарную величину потерь эксергии, которая возникает от необратимости преобразований в системе. Для идеальных процессов ηэкс= 1, для реальных процессов всегда ηэкс < 1.
определяют суммарную величину потерь эксергии, которая возникает от необратимости преобразований в системе. Для идеальных процессов ηэкс= 1, для реальных процессов всегда ηэкс < 1.
Рассмотрим процесс теплообмена между горячим потоком А холодным потоком В в элементарном объеме теплообменника. Горячий поток А передает тепловую энергию холодному потоку В, величину которой для элементарного объема обозначим dQ.
Тогда, учитывая, что энтропия S=Q/T, можно записать величину
эксергии, которую может передать горячий поток при переходе к состоянию равновесия с окружающей средой
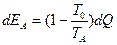 (43)
(43)
Холодный поток В при теплообмене получает лишь часть этой величины
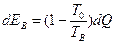 (44)
(44)
Разность между этими величинами дает потери эксергии в элементарном объеме
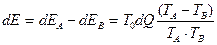 (45)
(45)
Полученное уравнение (45) показывает, что потери эксергии в системе зависят от конечной разности температур потоков и температурного напора. Потери эксергии при одинаковой разности температур намного меньше в условиях высокой температуры, чем в условиях низкой. Поэтому с точки зрения энергетики выгоднее осуществлять процессы при высокой температуре, поскольку энергия высокотемпературных отходящих потоков может быть использована со значительно меньшими потерями.
По величине рассчитанного эксергетического КПД делают вывод о термодинамической эффективности того или другого процесса. Как правило, значение энергетического и эксергетического КПД не совпадают. Последний показатель для большинства химико- технологических процессов, в которых водяной пар или отходящие газы полезно не используются, имеют более низкое значение чем энергетический (энтальпийный) КПД, что служит основанием для возможностей и резервов усовершенствования процесса. Эксергетический анализ разных способов производства одинакового продукта дает возможность выбрать наивыгоднейший с эксергетического точки зрения способ, меньше рассеивать в окружающую среду энергетические запасы Земли и уменьшить затраты энергии на производство того или другого продукта.
 2015-01-07
2015-01-07 2273
2273