Биоэнергетика — раздел биохимии, который изучает биохимические механизмы, приводящие к генерации различных форм биологической энергии. Каждое органическое соединение обладает определённым запасом внутренней энергии (Е). Часть этой внутренней энергии молекулы может быть использована для совершения полезной работы. Эту энергию называют свободной энергией (G) молекулы. Она представляет собой энергию валентных электронов, участвующих в образовании химических связей.
Источники энергии для организма - это химические реакции, в которых молекулы, содержащие атомы углерода в восстановленном состоянии, подвергаются окислению. При этом специальные дыхательные переносчики (молекулы НАД1" и ФАД) присоединяют протоны и электроны (восстанавливаются) и в таком виде транспортируют атомы водорода к дыхательной цепи. Эндергонические реакции - это химические реакции, требующие притока энергии для их осуществления. В этих реакциях изменение свободной энергии AG положительная величина.
Экзергонические реакции - это реакции, в которых энергия выделяется, т.е. они идут с выделением энергии. В таких реакциях изменение свободной энергии AG - отрицательная величина.
Внутриклеточные химические реакции могут быть представлены в виде:
1. Катаболических (экзергонических) реакций;
2. Анаболических (эндергонических) реакций.

Пример сопряжённых реакций:
Реакция фосфорилирования глюкозы свободным фосфатом с образованием глюкозо-6-фосфата является эндергонической:
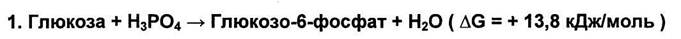
Самопроизвольно такая реакция осуществиться не может. Её течение требует притока энергии. Для течения этой реакции в сторону образования глюкозо-6-фосфат необходимо её сопряжение с другой реакцией, в которой энергия выделяется. Причем выделение энергии заведомо больше, чем требуется для фосфорилирования глюкозы. Такой реакцией является реакция гидролиза АТФ.

При сопряжении процессов (1) и (2) в реакции, катализируемой гексокиназой, фосфорилирование глюкозы легко протекает в физиологических условиях; равновесие реакции сильно сдвинуто вправо и она практически необратима:

В живых системах в отношении направления химических реакций и биологических процессов действует принцип: эндергонические реакции текут за счет энергии освобождающейся в экзергонических реакциях.
Анаболические (биосинтетические) процессы, требующие притока энергии, текут за счет энергии катаболических процессов (процессов распада молекул).
 2015-01-07
2015-01-07 24716
24716
