I А тобы элементтеріне сипаттама. Бір жағынан натрий мен литийдің, екінші жағынан калий топшасы элементтерінің кейбір физикалық және химиялық қасиеттерін салыстыру натрийдің анық сілтілік металдарға (калий топшасы) жақын екенін көрсетеді.
Барлық сілтілік металдарға ортақ қасиет – айқын көрінетін оң электрлік және радиустарының үлкен шамасы, иондану потенциалы және СЭТ-тің аз мәні болып табылады.
Төменде I А тобы элементтерінің кейбір қасиеттері келтірілді:
| Тұрақтылары | 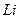 | 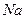 | 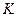 | 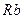 |  |
| Жер қыртысындағы мөлшері, мас.үлес, % | 3,4·10-3 | 2,64 | 2,6 | 1,5·10-2 | 3,7·10-4 |
| Валенттік эл-дық конфиг. | [He]2s1 | [Ne]3s1 | [Ar]4s1 | [Kr]5s1 | [Xe]6s1 |
| Атомдық радиус, нм | 0,155 | 0,189 | 0,236 | 0,248 | 0,267 |
Иондық радиус 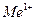 , нм , нм | 0,068 | 0,098 | 0,133 | 0,149 | 0,165 |
Иондану потенциалы, В 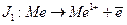 | 5,39 | 5,14 | 4,34 | 4,18 | 3,89 |
| СЭТ | 0,95 | 0,90 | 0,80 | 0,80 | 0,75 |
| Балқу т-расы, 0С | 180,0 | 97,8 | 63,5 | 38,7 | 28,5 |
| Қайнау т-расы, 0С | 1340,0 | 882,5 | 758,5 | 696,0 | 706,0 |
| Тығыздығы, г/см3 | 0,53 | 0,97 | 0,86 | 1,52 | 1,89 |
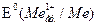 , В , В | -3,045 | -2,714 | -2,924 | -2,925 | -2,923 |
Барлық сілтілік металдар ақ-күміс түсті, оттегінің өте аз қоспасы цезийге сары-алтын бояу береді. Натрий мен калий судан жеңіл, ал цезий екі есеге жуық ауыр. Барлық сілтілік металдар жұмсақ, созылғыш, құрғақ ауа атмосферасында тез күңгірттенеді. Онда 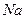 және
және 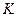 оксидтер
оксидтер 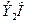 түзеді,
түзеді, 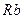 және
және 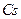 -пероксидтер
-пероксидтер 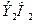 түзеді. Натрий сумен қызу әрекеттеседі, калий – қопарылыс шығарады, ал
түзеді. Натрий сумен қызу әрекеттеседі, калий – қопарылыс шығарады, ал 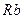 мен
мен 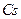 мұзбен жанасқанда да тұтанады. Ылғал ауамен әрекеттескенде барлық сілтілік металдар ақырында карбонаттарға айналады. Сондықтан натрий мен калийді әдетте керосин астында сақтайды, ал рубидий мен цезийді – эвакуацияланған ампулаларда. Оттегі атмосферасында сілтілік металдар жанады. Онда натрий
мұзбен жанасқанда да тұтанады. Ылғал ауамен әрекеттескенде барлық сілтілік металдар ақырында карбонаттарға айналады. Сондықтан натрий мен калийді әдетте керосин астында сақтайды, ал рубидий мен цезийді – эвакуацияланған ампулаларда. Оттегі атмосферасында сілтілік металдар жанады. Онда натрий 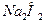 пероксид, ал қалғандары надпероксидтер (
пероксид, ал қалғандары надпероксидтер (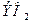 ) түзеді. Калий, рубидий және цезий үшін озонидтер
) түзеді. Калий, рубидий және цезий үшін озонидтер 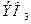 белгілі. Кәдімгі жағдайда сілтілік металдар фтор мен хлор атмосферасында жанады, ал аздап қыздырғанда күкірт, сутегі, бром және басқа металл еместермен оңай әрекеттеседі.
белгілі. Кәдімгі жағдайда сілтілік металдар фтор мен хлор атмосферасында жанады, ал аздап қыздырғанда күкірт, сутегі, бром және басқа металл еместермен оңай әрекеттеседі.
Натрий оксиді түссіз, ал калған оксидтер сары және қызғылт-сары (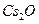 ) түсті. Олардың барлығы өте гигроскопті, су қосып алып тән гидроксидтеріне айналады.
) түсті. Олардың барлығы өте гигроскопті, су қосып алып тән гидроксидтеріне айналады.
Сілтілік металдардың гидроксидтері 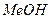 - суда және спирттерде еритін кристалл заттар. Олардың су ерітінділері – күйдіргіш сілтілер – нағыз күшті негіздер. Гидроксидтерді хлоридтердің су ерітінділерін электролиздеп алады. Онда катод кеңістігінде сутегі бөлінеді және сілтілік металдың гидроксиді түзіледі.
- суда және спирттерде еритін кристалл заттар. Олардың су ерітінділері – күйдіргіш сілтілер – нағыз күшті негіздер. Гидроксидтерді хлоридтердің су ерітінділерін электролиздеп алады. Онда катод кеңістігінде сутегі бөлінеді және сілтілік металдың гидроксиді түзіледі.
Құрамында оттегі бар қышқылдар тұздарының ішіндегі ең маңыздылары карбонаттар. Сода 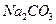 негізгі химия өндірісі өнімдеріне жатады Оны аммиакты әдіспен алады. Онда концентрлі
негізгі химия өндірісі өнімдеріне жатады Оны аммиакты әдіспен алады. Онда концентрлі 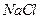 ерітіндісін аммиакпен қанықтырады, сосын көміртегі диоксидімен өңдейді. Бұл процесте гидрокарбонат тұнбаға түседі, оны қуырып қыздырып карбонатқа айналдырады:
ерітіндісін аммиакпен қанықтырады, сосын көміртегі диоксидімен өңдейді. Бұл процесте гидрокарбонат тұнбаға түседі, оны қуырып қыздырып карбонатқа айналдырады:
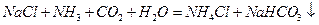
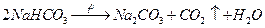
Поташ 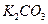 табиғи
табиғи 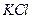 өңдегенде, сол сияқты жапырақты ағаш тұқымдарының және күнбағыстың күлдерін шаймалау арқылы алынады. Натрий сульфаты және нитраты, сол сияқты калий сульфаты көп мөлшерде жаратылыста кездеседі.
өңдегенде, сол сияқты жапырақты ағаш тұқымдарының және күнбағыстың күлдерін шаймалау арқылы алынады. Натрий сульфаты және нитраты, сол сияқты калий сульфаты көп мөлшерде жаратылыста кездеседі. 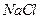 -дің аз ерігіштігін пайдаланып, калий нитратын
-дің аз ерігіштігін пайдаланып, калий нитратын 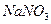 пен
пен 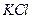 -дің арасындағы алмасу реакциясы арқылы алады.
-дің арасындағы алмасу реакциясы арқылы алады.
 2015-02-27
2015-02-27 2730
2730







