1. ХИМИЧЕСКОЙ РЕАКЦИИ Fe2O3(k) + 3C(k) = 2Fe(k) + ЗСО (к)
ΔН0 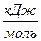 -822 0 0 -110,5
-822 0 0 -110,5
ВОССТАНОВЛЕНИЯ ОКСИДА ЖЕЛЕЗА ПРИ СТАНДАРТНЫХ УСЛОВИЯХ СООТВЕТСТВУЕТ ИЗМЕНЕНИЕ ЭНТАЛЬПИИ (кДж/моль):
А.+490,5.–933,6 С.+936,6 D.+712,4 E.+1154,8
2. МАТЕМАТИЧЕСКОМУ ВЫРАЖЕНИЮ ИЗМЕНЕНИЯ ЭНТРОПИИ ПРОЦЕССА: 2NO = N204 СООТВЕТСТВУЕТ
A.Sx.p.=SN204 – 2SNO В. Sx.p.= 2SNO - SN204 C. Sx.p.=SN204 – SNO
D. Sx.p = 2SN204 - 2SNO E. Sx.p =SN204 + SNO
3.ОТРИЦАТЕЛЬНОМУ ЗНАЧЕНИЮ ЭНТРОПИИ СООТВЕТСТВУЕТ ПРОЦЕСС
А. 2Р(к) + 3CI2 - 2РСlз(г) В. CO2 + С - 2CO С. 4NH3 + 5O2 -4NO + 6HzO
D. РСl5(Г) - РСlз(г) + Cl2(г) Е. СН4(г) + СО2(г) - С0(г) + 2Н20(Г)
4. ИЗМЕНЕНИЕ СВОБОДНОЙ ЭНЕРГИИ ГИББСА В РЕАКЦИИ ВОССТА-НОВЛЕНИЯ ОКСИДА ВОЛЬФРАМА ВОДОРОДОМ (Δ H0x.p=117 кДж;
Δ S0x.p=127,34 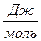 ) ПРИ ТЕМПЕРАТУРЕ 6000 К РАВНО (кДж.моль)
) ПРИ ТЕМПЕРАТУРЕ 6000 К РАВНО (кДж.моль)
А.+79023,0 В.+196,14 С.-61400,0 D.+40,59 Е.–78843
5. ТЕМПЕРАТУРА, ПРИ КОТОРОЙ НАСТУПИТ РАВНОВЕСИЕ В СИСТЕМЕ: Mg(OH)2= Mg0+ H2O ПРИ (Δ H0x.p=81,36 кДж; ΔS0x.p=152,61 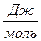 ) PABHA (К)
) PABHA (К)
А. 297,9К В. 24947,7К C. 25446,6K D. 533,1K E. 1,123K
6. ПРИ СТАНДАРТНЫХ УСЛОВИЯХ ТЕПЛОВОЙ ЭФФЕКТ
РЕАКЦИИ 4HCI(г) + 02(г) = 2Н20(г) + 2Сl2(г)
Δ Н0 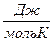 -92,31 0 -241,81 0
-92,31 0 -241,81 0
РАВЕН (кДж/моль)
А.-334,14 В.-149,52 С.-975,32 D.+114,38 Е.+154,41
7. ОБРАТИМОЙ РЕАКЦИИ СаО(т) + С02—> СаСОз(т) СООТВЕТСТВУЕТ МАТЕМАТИЧЕСКОЕ ВЫРАЖЕНИЕ КОНСТАНТЫ РАВНОВЕСИЯ
А. Кр - [СаСОз| / |СаО| |СО2| В. Кр - 1/|СаО| С. Кр - 1/|СаОЗ| [С02|
D. Кр - 1/[С02| Е. Кр – |СО2 ||СаО|/|СаСОз|
8. СМЕЩЕНИЕ РАВНОВЕСИЯ ВПРАВО В СИСТЕМЕ
СаО + CO2 —> СаСОз ВОЗМОЖНО ПРИ УСЛОВИИ
А. Увеличения концентрации |СО2| В. Уменьшения концентрации |СаО|
С. Увеличения концентрации |СаСОз| D. Понижение давления
Е. Уменьшения концентрации |СаО| И |CO2|
9. ЦЕПНЫЕ РЕАКЦИИ ПРОТЕКАЮТ ЧЕРЕЗ СТАДИИ ОБРАЗОВАНИЯ
А. Атомов В. Свободных радикалов С. Молекул D. Ионов Е. Комплексов
10. ИЗБЫТОЧНАЯ КИНЕТИЧЕСКАЯ ЭНЕРГИЯ МОЛЕКУЛ, ХАРАКТЕРИ-ЗУЮЩАЯ НАЧАЛО ХИМИЧЕСКОГО ПРОЦЕССА, НАЗЫВАЕТСЯ
А. Энергией натяжения В. Энергией активации С. Свободной энергией
D. Внутренней энергией Е. Силами Ван-дер-Ваальса
11.ЭНЕРГИЯ ПОЛОЖЕНИЯ И ВЗАИМОДЕЙСТВИЯ ЧАСТИЦ СИСТЕМЫ, НАЗЫВАЕТСЯ
А. Потенциальной В. Внутренней С. Кинетической D. Поступательной
Е. Вращательной
12. ОБРАТИМОЙ РЕАКЦИИ С0 + СI2 – СOCI2 СООТВЕТСТВУЕТ МАТЕМАТИЧЕСКОЕ ВЫРАЖЕНИЕ КОНСТАНТЫ РАВНОВЕСИЯ
А. К =1/ (COCI2) В. К =CI2/COCI2 С. К = (COCI2)/(СО) (Сl2) D. К =(C0) (CI2)/(COCI2)
Е. К =1/(CI2)
13. СМЕЩЕНИЕ РАВНОВЕСИЯ ВЛЕВО В СИСТЕМЕ: Zn0 + С0 = Zn +CO2 ВОЗМОЖНО ПРИ УСЛОВИИ
А. Увеличения давления В. Уменьшения давления С. Увеличения концентрации СО2
D. Увеличения концентрации С0 Е. Уменьшения концентрации С02
14. ПЕРЕХОД ИЗ ЖИДКОГО СОСТОЯНИЯ В ГАЗООБРАЗНОЕ НАЗЫВА-ЕТСЯ
А. Парообразованием В. Сжижением С. Сублимацией D. Десублисмацией
Е. Плавлением
15. ПЕРЕХОД ИЗ ТВЕРДОГО СОСТОЯНИЯ В ГАЗООБРАЗНОЕ НАЗЫВАЕТСЯ
А. Парообразованием В. Сжижением С. Сублимацией D. Десублисмацией
Е. Плавлением
16. СИСТЕМУ, ЛИШЕННУЮ СТЕПЕНЕЙ СВОБОДЫ, НАЗЫВАЮТ
А. Инвариантной В. Моновариантной С. Бивариантной D. Тривариантной
Е. Пентавариантной
17. ПЕРЕХОД ТЕРМОДИНАМИЧЕСКОЙ СИСТЕМЫ ИЗ ОДНОГО СОСТОЯНИЯ В ДРУГОЕ ПРИ ПОСТОЯННОМ ДАВЛЕНИИ НАЗЫВАЕТСЯ
А. Изохорическим В. Изобарическим С. Изотермическим
D. Адиабатическим Е. Изохорно-изотермическим
18. ПЕРЕХОД ТЕРМОДИНАМИЧЕСКОЙ СИСТЕМЫ ИЗ ОДНОГО СОСТОЯНИЯ В ДРУГОЕ ПРИ ПОСТОЯННОМ ОБЪЕМЕ НАЗЫВАЕТСЯ
А. Изохорическим В. Изобарическим С. Изотермическим
D. Адиабатическим Е. Изохорно-изотермическим
19. КОЛИЧЕСТВО МОЛЕКУЛ, УЧАСТВУЮЩИХ В ЭЛЕМЕНТАРНОМ АКТЕ БИМОЛЕКУЛЯРНОЙ РЕАКЦИИ, РАВНО
 2015-02-04
2015-02-04 589
589







