Теплоемкостью тела называется физическая величина, числено равная количеству теплоты, которую нужно сообщить телу, чтобы повысить его температуру на 1 градус. Теплоемкость, отнесенная к единице массы, называется удельной теплоемкостью c, а к одному молю – молярной теплоемкостью С. Молярная и удельная теплоемкости связаны через молярную массу М: С = Мс. Это соотношение справедливо как для теплоемкости при постоянном давлении, так и для теплоемкости при постоянном объеме.
Важное значение в термодинамике имеет отношение теплоемкости при постоянном давлении ср к теплоемкости при постоянном объеме сv. Это отношение называется показателем адиабаты g, и его можно определить через число степеней свободы i молекулы газа: g = ср / cv = (i + 2) / i. Значение величины g играет большую роль при изучении адиабатических процессов. Например, от этой величины зависит скорость распространения звука в газах и течение газов по трубам со сверхзвуковыми скоростями.
Всякое достаточно быстрое изменение объема газа можно с достаточной степенью точности рассматривать как адиабатическое, т.к. теплообменом с окружающей средой можно пренебречь. При быстром расширении газ охлаждается, а при быстром сжатии – нагревается.
Одним из самых простых методов определения g является метод Клемáна и Дезóрма. Рассмотрим его сущность.
Пусть в закрытом стеклянном баллоне объемом V находится исследуемый газ при комнатной температуре Т 1 и давлении р 1, несколько превышающем атмосферное давление р 0.
Если открыть кран, соединяющий баллон с атмосферой, то давление в сосуде упадет до атмосферного, а температура сначала несколько понизится из-за быстрого расширения газа в атмосферу, а затем поднимется до комнатной (вследствие теплообмена через стенки сосуда). Так как отверстие крана достаточно велико, а теплопроводность стекла низка, то время выравнивания давления D tP во много раз меньше времени выравнивания температуры D tТ. Пусть кран был открыт в течение малого промежутка времени D t такого, что D tT >> D t >> D tP. В этом случае можно теплообменом пренебречь и считать процесс выхода газа в атмосферу адиабатическим. Уравнение адиабаты в переменных р и Т запишем в виде:
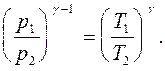 (1)
(1)
Заметим, что в конце адиабатического расширения давление р 2 равно атмосферному р 0, а температура Т 2 оказывается несколько ниже комнатной температуры Т 1. Затем, если кран на баллоне закрыт, то вследствие теплообмена с окружающей средой происходит медленное изохорное нагревание газа до тех пор, пока установившаяся температура газа Т 3 не сравняется с комнатной Т 1. Для изохорного процесса можно записать:
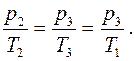 (2)
(2)
Исключая с помощью уравнения (2) отношение температур 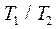 из (1), найдем:
из (1), найдем:
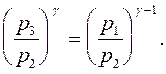 (3)
(3)
Разрешим это уравнение относительно g:
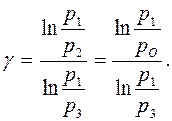 (4)
(4)
В нашем случае давления р 1 и р 3 мало отличаются от атмосферного р 0 и формулу (4) можно существенно упростить. Введем обозначения:
р 1 = р 0 + h 1, p 3 = p 0 + h 2.
Разлагая логарифмы в ряд и пренебрегая членами второго порядка малости, получим:
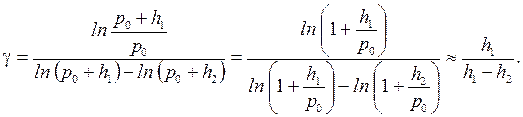 (5)
(5)
Как видно из уравнения (5), для вычисления g необходимо измерить избыточное давление в баллоне до адиабатического расширения газа h 1 и его избыточное давление после изохорного нагревания h 2. Следует подчеркнуть, что обе величины должны измеряться в состоянии термодинамического равновесия, т.е. после прекращения теплообмена.
 Описание установки
Описание установки
Установка (рис. 1) состоит из баллона, который при помощи верхнего крана может сообщаться с атмосферой. Через гибкую трубку баллон соединен с U -образным манометром. Избыточное давление в баллоне создается резиновой грушей, которая подает воздух через нижний кран в баллон. Нижний кран служит для того, чтобы отсекать объем баллона от атмосферы, после того, как в баллоне возникает избыточное давление.
|
 2015-02-04
2015-02-04 749
749








