Изучение адреналиновой нервной системы явилось толчком в развитии идеи о существовании рецепторов. Впервые был найден нейромедиатор и установлена его химическая формула.
Сначала, по ошибке, за нейромедиатор приняли адреналин (впервые выделенный в 1898 г. из надпочечников крупного рогатого скота), и только после 1946 г. было установлено, что это вещество является гормоном, а не нейромедиатором, а также был установлен путь синтеза этого вещества в организме: начинается он с фенилаланина, который под действием фермента (фениланилазы) превращается в тирозин. Затем тирозин превращается в L-дофу, которая далее превращается в дофамин (нейромедиатор головного мозга), а дофамин – в норадреналин (тоже являющийся нейромедиатором). Норадреналин превращается в адреналин:
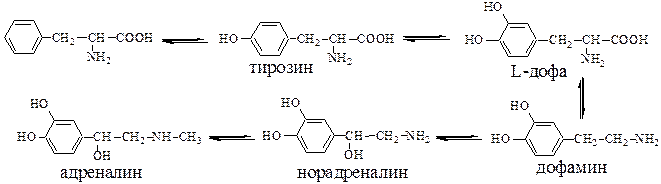 Схема 4
Схема 4
α1-, α2-, β1-, β2 – рецепторы
ФЕНИЛАЛКИЛАМИНЫ:
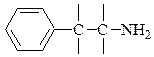
Схема 5
от 2 до 4 атомов углерода в алифатической цепи.
Заместители в алифатической части молекулы:
 –ОН (чаще в α-положении к ароматическому ядру);
–ОН (чаще в α-положении к ароматическому ядру);
–СН3 (чаще в β-положении к ароматическому ядру);
|
|
|
иногда –С2Н5, часто –СН2ОН, С=О (в α-положении).
Как правило, вещества, имеющие 2 атома углерода в алифатической цепи, являются бронхолитиками; веществами, стимулирующими работу сердца или артериальное давление.
Как правило, вещества, имеющие 4 атома углерода в алифатической цепи, являются нейролептиками.
Изменения характеристик при варьировании структуры фенилалкиламина:
При наличии группы –ОН в 3, 4 -положениях лекарство очень быстро разрушается ферментами; а при наличии тех же групп в 3, 5 -положениях действие лекарства можно пролонгировать (увеличить) во времени.
Наличие в структуре первичной аминогруппы как правило делает вещество нетоксичным, введение же заместителей по аминогруппе повышает токсичность вещества; с другой стороны, вещества с первичной аминогруппой – плохо растворимы и плохо доставляются к месту действия. Поэтому часто всего используют соединения с вторичной аминогруппой (как правило, используют простые алкильные группы: метильную, этильную, изо -пропильную). Введение же алкильного заместителя с разветвленной углеродной цепью по аминогруппе приводит к тому, что вещество действует исключительно на β-адренорецепторы.
Часто по аминогруппе вводят дифенилметильную группу, и иногда вводят длинную линейную углеводородную цепь (из трёх атомов углерода) и также трет -бутильную группу.
При исследовании структуры фенилалкиламинов также были установлены следующие закономерности: –ОН -группа в α-положении к ароматическому ядру повышает активность соединения и одновременно может снижать его токсичность.
|
|
|
Третичные аминогруппы обычно приводят к резкому повышению токсичности вещества.
Полное симпатомиметическое действие проявляется только при наличии двух гидроксильных групп в ароматическом ядре.
Исходными соединениями для синтеза фенилалкиламинов явл. вератрол и пирокатехол.
 2015-02-04
2015-02-04 984
984








