Абсолютная температура 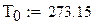
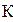
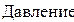
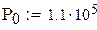
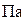
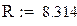
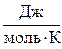
Универсальная газовая постоянная
Объем 1 моля газа при нормальных условиях
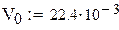
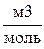
Cтехиометрические коэффициенты в уравнении реакции
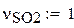
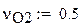
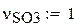
Мольный состав смеси
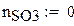
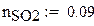
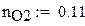
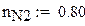
Доля стехиометрической смеси исходных компонентов в реальной смеси b
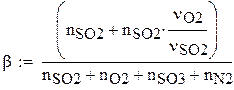
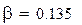
Коэффициент изменения объема в системе x
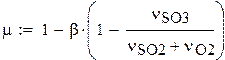
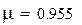
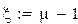
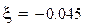
Молярные массы компонентов смеси
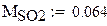
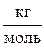
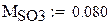
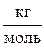
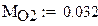
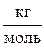
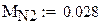
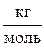
Молярная масса газовой смеси
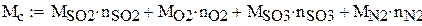
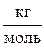
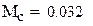
Плотность газовой смеси 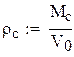
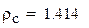
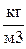
Коэффициент теплообмена 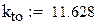
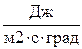
Температура смеси на входе в реактор 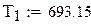
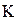
Удельная теплоемкость газовой смеси 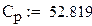
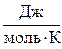
Температура смеси на выходе из реактора 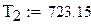
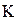
Температура хладагента 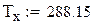
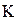
Расход реакционной смеси 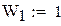
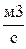
РАСЧЕТ q xp
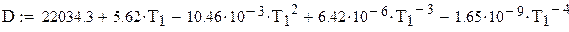
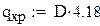
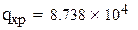
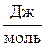
РАСЧЕТ Кp
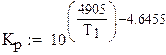
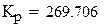
РАСЧЕТ РАВНОВЕСНОЙ СТЕПЕНИ ПРЕВРАЩЕНИЯ ПРИ 460 С
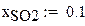
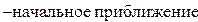
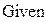
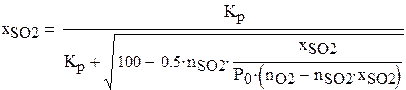
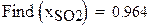
РАСЧЕТ КОНСТАНТЫ СКОРОСТИ (ДЛЯ ВАНАДИЕВОГО КАТАЛИЗАТОРА)
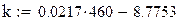
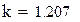
РАСЧЕТ СКОРОСТИ ОКИСЛЕНИЯ ПО УРАВНЕНИЮ БОРЕСКОВА-ИВАНОВА
Начальное приближение 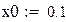
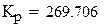
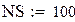
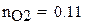
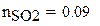
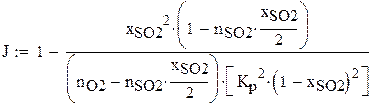
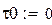
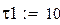
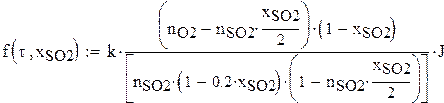
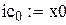
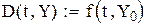
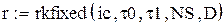
Начальная степень превращения 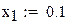
Конечная степень превращения 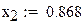
Время пребывания реакционной смеси в реакторе 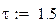
Скорость реакции
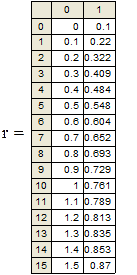
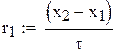
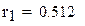
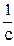
РАСЧЕТ РИС-П
1. Объем реактора
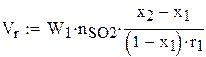
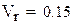
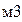
2. Поверхность теплообмена
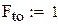
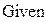
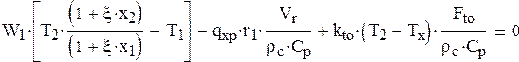
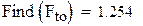
РАСЧЕТ РИС-Н- И
1. Объем реактора
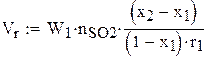
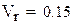
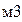
2. Поверхность теплообмена
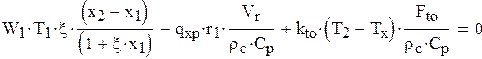
Find(Fto) 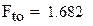
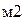
РАСЧЕТ РИС-Н-А
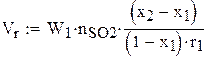
1. Объем реактора
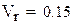
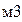
2. Адиабатическая температура
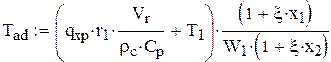
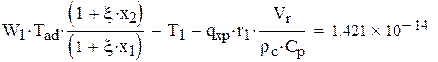
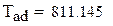
Литература
1. Бретшнайдер С., Кавецкий В., Лейко Я. И др. Общие основы химической технологии. Л.: Химия, Лен.отд-е, 1977. 503 с.
2. Рабинович В.А., Хавин З.Я. Краткий химический справочник. Л.:Химия, Лен-е отд-е, 1978. 392 с.
3. Основы химической технологии //И.П.Мухленов, А.Е. Горштейн, Е.С. Тумаркина, Н.В. Кузичкин; под ред. И.П. Мухленова. - М.: Высшая школа, 1991. - 463 с.
4. Общая химическая технология// под ред. А.Г.Амелина. М.:Химия, 1977. 400 с.
5. Бесков С.Д. Технохимические расчеты. М.:Высшая школа, 1966. 520 с.
6. Кутепов А.М., Бондарева Т.И., Беренгартен М.Г. Общая химическая технология. -М.: Высшая школа, 1990. 520 с.
7. Ахметов К. Windows 95 для всех. М.: ТОО "КомпьютерПресс", 1997. 256 с.
8. Додж М., Кайнет К. Эффективная работа с Excel 7.0 для Windows 95. Санкт-Петербург: Питер, 1996. 1000 с.
9. Гарнаев А.Ю. Использование MS Excel и VBA в экономике и финансах. СПб.:БХВ. Санкт-Петербург, 2000. 386 с.
10. Вольфкович С.И., Егоров А.П., Эпштейн Д.А. Общая химическая технология. Изд-е химической литературы, М.-Л., 1953, т.1. 632 с.
11.Справочник сернокислотчика /Под. Ред К.М.Малина: М. Химия, 1971. 744 с.
12. Аладьев В.З., Гершгорн Н.А. Вычислительные задачи на персональном компьютере. К.:Тэхника, 1991. 245 с.
13. Чертов А.Г. Единицы физических величин. М.:Высшая школа, 1977. 287 с.
Приложения
Приложение 1. Термодинамические свойства веществ
Значения Ср, DН 0298, DG 0298, DS 0298 чистых веществ (т – твердое вещество, ж – жидкость, г – газ)
| Вещество | Мольная теплоемкость, кал/моль×К | DН 0298, ккал/моль | DG 0298, ккал/моль | DS 0298, ккал/(моль.К) | |||||
| коэффициенты уравнения | |||||||||
| а | b .103 | с’ .10-5 | с .106 | d .109 | |||||
| А1 (т) | 4,94 | 2,96 | — | — | — | 6,769 | |||
| С (т) - графит | 4,10 | 1,02 | -2,10 | — | — | 1,3609 | |||
| С12 (г) | 6,8214 | 5,709 | — | -5,107 | 1,547 | 53,286 | |||
| Fе-a (т) | 3,37 | 7,10 | -0,43 | — | — | 6,49 | |||
| Н2 (г) | 6,952 | -0,457 | — | 0,9563 | -0,2079 | 31,211 | |||
| N2 (г) | 6,903 | -0,375 | — | 1,930 | -0,6861 | 45,767 | |||
| O2 (г) | 8,643 | 0,202 | -1,030 | — | — | 49,003 | |||
| S (т) ромб. | 3,58 | 6,24 | — | — | — | 7,62 | |||
| А12O3-a (т) | 27,43 | 3,06 | -8,47 | — | — | -399,09 | -376,77 | 12,186 | |
| СО (г) | 6,726 | 0,400 | — | 1,283 | -0,5307 | -26,416 | -32,808 | 47,301 | |
| СО2 (г) | 10,55 | 2,16 | -2,04 | — | — | -94,052 | -94,260 | 51,061 | |
| СаСО3-кальцит | 24,98 | 5,24 | -6,20 | — | — | -288,45 | -269,78 | 22,2 | |
| СаО (т) | 11,67 | 1,08 | 1,56 | — | — | -151,9 | -144,4 | 9,5 | |
| СаSO4 (т) | 18,52 | 21,97 | -1,568 | — | — | -342,42 | -315,56 | 25,5 | |
| Fе2O3 (т) | 233,6 | 17,24 | -3,08 | — | — | -196,5 | -177,1 | 21,5 | |
| НС1 (г) | 6,34 | 1,10 | 0,26 | — | — | -22,063 | -22,769 | 44,17 | |
| Н2O (г) | 7,700 | 0,4594 | — | 2,521 | -0,8587 | -57,798 | -54,636 | 45,106 | |
| НNО3 (ж) | — | — | — | — | — | -41,404 | -19,10 | 37,19 | |
| Н2SO4 (ж) | — | — | — | — | — | -191,4 -104,175 -11,04 21,60 8,091 | (-164,2) | 37,49 | |
| КС1 (т) | 9,89 | 5,20 | 0,77 | — | — | -97,592 | 19,76 | ||
| NH3 (г) | 6,5846 | 6,1251 | — | 2,3663 | -1,5981 | -3,976 | 46,01 | ||
| NO (г) | 6,461 | 2,358 | — | -0,7705 | 0,08729 | 20,719 | 50,339 | ||
| NO2 (г) | 5,48 | 13,65 | — | -8,41 | 1,88 | 12,390 | 57,47 |
Продолжение таблицы
| NаС1 (т) | 10,98 | 3,90 | — | — | — | -98,232 | -91,785 | 17,30 |
| NаОН (т) | 19,2 | — | — | — | — | -102,0 | -91,0 | 15,34 |
| Nа2СО3 (т) | — | — | — | — | — | -271,02 | -251,11 | 32,5 |
| SO2 (г) | 6,157 | 13,84 | — | -9,103 | 2,057 | -70,96 | -71,79 | 59,40 |
| SO3 (г) | 13,70 | 6,42 | -3,12 | — | — | -94,45 | -88,52 | 61,24 |
| SiO2 - a-кварц | 11,22 | 8,20 | -2,70 | — | — | -205,4 | -192,4 | 10,00 |
| СН4 (г) | 4,750 | 12,00 | — | 3,03 | -2,63 | -17,889 | -12,140 | 44,50 |
| С2Н2 (г) | 5,21 | 22,00 | — | -15,59 | 4,349 | 54,190 | 50,000 | 48,00 |
| С2Н4 (г) | 0,944 | 37,35 | — | -19,93 | 4,220 | 12,498 | 16,295 | 52,45 |
| С2Н6 (г) | 1,648 | 41,24 | — | -15,30 | 1,740 | -20,236 | -7,860 | 54,85 |
| С3Н8 (г) | -0,966 | 72,79 | — | -37,55 | 7,580 | -24,82 | -5,61 | 64,51 |
| изо -С4Н10 (г) | -1,890 | 99,36 | — | -54,95 | 11,92 | -31,450 | -4,300 | 70,42 |
| С6Н6 (г) | -8,650 | 115,78 | — | -75,40 | 18,54 | 19,82 | 30,850 | 64,457 |
| С8Н10 (г) | -8,398 | 159,35 | — | -100,03 | 23,95 | -2,98 | 28,62 | 60,95 |
| СН3ОН (г) | 4,55 | 21,86 | — | -2,91 | -1,92 | -48,08 | -38,69 | 56,8 |
| С2Н5ОН (г) | 4,75 | 50,06 | — | -24,79 | 4,790 | -56,24 | -40,3 | 67,4 |
| СН3СНО (г) | 4,19 | 31,64 | — | -5,15 | -3,800 | -39,76 | -31,96 | 63,5 |
| (СН3)2СО (г) | 1,625 | 66,61 | — | -37,37 | 8,37 | -51,79 | -36,5 | 72,7 |
| СН3СООН (г) | 5,20 | 46,16 | — | -18,35 | — | -104,3 | -91,2 | 70,1 |
| СНСl3 (г) | 7,61 | 34,61 | — | -26,68 | 7,344 | -24 | -16 | 70,62 |
| С6Н5Cl (ж) | — | — | — | — | — | 27,80 | 27,8 | 47,2 |
| С6Н5NО2 (ж) | — | — | — | — | — | 5,3 | 34,95 | 53,6 |
| С6Н5ОН (т) | — | — | — | — | — | -37,26 | -9,74 | 34,0 |
| СН3СНClСН3 (г) | 4,49 | 63,46 | — | -22,53 | — | -31,20 | — | 70,5 |
Приложение 2. Средняя мольная теплоемкость веществ
Средняя мольная теплоемкость 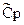 (кал/моль×град) газов в интервале температур 0 - t, 0С
(кал/моль×град) газов в интервале температур 0 - t, 0С
| t, 0С | Н2 | N2 | О2 | СО | NO | Н2O | СO2 | N2O | SO2 | Воздух | SO3 | СН4 | С2Н4 | С2Н2 |
| 6,92 | 6,97 | 7,05 | 6,97 | 7,14 | 8,03 | 9,17 | 9,79 | 9,74 | 6,96 | 12,39 | 8,73 | 11,45 | 11,12 | |
| 6,95 | 7,00 | 7,15 | 7,00 | 7,17 | 8,12 | 9,65 | 10,12 | 10,15 | 7,01 | 12,92 | 9,48 | 12,64 | 11,79 | |
| 6,97 | 7,04 | 7,26 | 7,06 | 7,22 | 8,22 | 10,06 | 10,45 | 10,52 | 7,06 | 13,38 | 10,20 | 13,73 | 12,36 | |
| 6,98 | 7,09 | 7,38 | 7,12 | 7,30 | 8,34 | 10,40 | 10,74 | 10,84 | 7,13 | 13,79 | 10,88 | 14,76 | 12,81 | |
| 6,99 | 7,15 | 7,49 | 7,19 | 7,38 | 8,47 | 10,75 | 11,02 | 11,11 | 7,20 | 14,14 | 11,53 | 15,69 | 13,21 | |
| 7,01 | 7,21 | 7,59 | 7,27 | 7,46 | 8,60 | 11,03 | 11,24 | 11,35 | 7,27 | 14,44 | 12,15 | 16,52 | 13,58 | |
| 7,03 | 7,27 | 7,68 | 7,34 | 7,54 | 8,74 | 11,28 | 11,50 | 11,55 | 7,34 | 14,69 | 12,74 | 17,26 | 13,90 | |
| 7,06 | 7,35 | 7,77 | 7,43 | 7,62 | 8,89 | 11,50 | 11,71 | 11,72 | 7,42 | 14,91 | 13,28 | 18,07 | 14,22 | |
| 7,09 | 7,42 | 7,85 | 7,50 | 7,70 | 9,04 | 11,70 | 11,90 | 11,88 | 7,49 | 15,11 | 13,79 | 18,62 | 14,49 | |
| 7,12 | 7,49 | 7,92 | 7,57 | 7,76 | 9,18 | 11,88 | 12,07 | 12,01 | 7,56 | 15,28 | 14,27 | 19,24 | 14,75 | |
| 7,15 | 7,56 | 7,98 | 7,64 | 7,83 | 9,32 | 12,05 | 12,21 | 12,13 | 7,62 | |||||
| 7,20 | 7,62 | 8,04 | 7,70 | 7,89 | 9,45 | 12,19 | 12,35 | 12,23 | 7,68 | |||||
| 7,24 | 7,67 | 8,11 | 7,76 | 7,94 | 9,58 | 12,32 | 12,48 | 12,33 | 7,73 | |||||
| 7,28 | 7,73 | 8,16 | 7,81 | 7,99 | 9,72 | 12,45 | 12,60 | 12,41 | 7,78 | |||||
| 7,32 | 7,78 | 8,20 | 7,85 | 8,03 | 9,84 | 12,56 | 12,69 | 12,48 | 7,84 | |||||
| 7,36 | 7,82 | 8,24 | 7,90 | 8,08 | 9,96 | 12,66 | 12,78 | 12,55 | 7,88 | |||||
| 7,40 | 7,86 | 8,28 | 7,94 | 8,12 | 10,09 | 12,75 | 12,88 | 12,61 | 7,92 | |||||
| 7,45 | 7,91 | 8,33 | 7,98 | 8,15 | 10,20 | 12,84 | 12,95 | 12,67 | 7,96 | |||||
| 7,49 | 7,94 | 8,38 | 8,02 | 8,19 | 10,30 | 12,92 | 13,01 | 12,71 | 7,99 | |||||
| 7,53 | 7,98 | 8,42 | 8,05 | 8,22 | 10,41 | 12,99 | 13,09 | 12,77 | 8,03 | |||||
| 7,57 | 8,01 | 8,45 | 8,09 | 8,26 | 10,52 | 13,06 | 13,17 | 12,81 | 8,06 | |||||
| 7,62 | 8,05 | 8,48 | 8,12 | 8,29 | 10,61 | 13,13 | 13,21 | 12,85 | 8,08 | |||||
| 7,66 | 8,08 | 8,52 | 8,15 | 8,31 | 10,71 | 13,19 | 13,28 | 12,89 | 8,12 | |||||
| 7,70 | 8,10 | 8,56 | 8,18 | 8,34 | 10,79 | 13,24 | 13,33 | 12,93 | 8,14 | |||||
| 7,74 | 8,14 | 8,59 | 8,21 | 8,36 | 10,87 | 13,30 | 13,38 | 12,96 | 8,18 | |||||
| 7,78 | 8,17 | 8,63 | 8,24 | 8,38 | 10,96 | 13,34 | 13,42 | 12,99 | 8,20 | |||||
| 7,81 | 8,19 | 8,65 | 8,26 | 8,40 | 11,03 | 13,39 | 13,46 | 13,02 | 8,23 | |||||
| 7,85 | 8,22 | 8,68 | 8,28 | 8,42 | 11,11 | 13,43 | 13,51 | 13,04 | 8,25 | |||||
| 7,89 | 8,24 | 8,72 | 8,30 | 8,44 | 11,18 | 13,48 | 13,55 | 13,07 | 8,27 | |||||
| 7,92 | 8,26 | 8,76 | 8,32 | 8,45 | 11,23 | 13,52 | 13,59 | 13,10 | 8,29 |
Приложение 3. Соотношения размерностей физических величин
| Величина | Единица | ||
| Наименование | Обозначение | Соотношение с единицей СИ | |
| Температура | градус цельсия | t,0С | t=T-T0, T0=273,15 K, T - температура Кельвина |
| Давление | килограмм-сила на квадратный сантиметр = 1 ат | Р, ат | 98066,5 Па |
| миллиметр водяного столба | мм вод.ст. | 9,806 Па | |
| миллиметр ртутного столба | мм рт.ст. | 133,322 Па | |
| Количество теплоты, энтальпия, теплота фазового превращения, теплота химической реакции | калория килокалория | Кал ккал | 4,186 Дж 4,186×103 Дж |
| Удельная теплота фазового превращения, удельная теплота химической реакции | килокалория на килограмм | ккал/кг | 4,1868×103 дж/кг |
| Удельная теплоемкость вещества | килокалория на килограмм-кельвин | ккал/(кг×К) | 4,1868×103 Дж/К |
| Теплоемкость системы | килокалория на кельвин | ккал/К | 4,1868×103 Дж/(кг×К) |
| Поверхностная плотность теплового потока | килокалория в ч на квадратный метр калория в секунду на квадратный сантиметр | ккал/(ч×м2) кал/(с×см2) | 1,163 Вт/м2 4,1868×104 Вт/м2 |
| Коэффициент теплоотдачи и теплопередачи | килокалория в ч на квадратный метр-кельвин калория в секунду на квадратный сантиметр-кельвин | ккал/(ч×м2×К) кал/(с×см 2×К) | 1,163 Вт/м2 4,1868×104 Вт/м2×К |
| Теплопроводность | килокалория в ч на метр-кельвин калория в секунду на сантиметр-кельвин | ккал/(ч×м×К) кал/(с×см ×К) | 1,163 Вт/м×К 4,1868×102 Вт/м×К |
| Удельная газовая постоянная | килокалория на килограмм-кельвин калория на грамм-кельвин | ккал/(кг×К) кал/(г ×К) | 4,1868×103 Дж/(кг×К) 4,1868×103 Дж/(кг×К) |
Контрольные вопросы
 2015-03-08
2015-03-08 605
605








