Кондуктометрия основана на измерении электрической проводимости растворов электролитов. В электрохимической промышленности электрохимическая проводимость играет большую роль при составлении энергетических и тепловых балансов электролизеров и химических источников тока, а так же в мембранной технологии.
Экспериментальной величиной в методе кондуктометрии является сопротивление раствора электролита. Для измерения сопротивления применяется мостовая схема Уинстона. Принцип измерения электрической проводимости растворов электролитов приведен на рис.3.
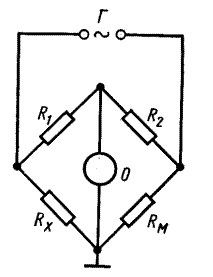 Рис. 3 Схема установки для измерения электрического сопротивления раствора электролита. RМ и Rx – сопротивления магазина и ячейки; Г - источник переменного тока; О – осциллограф. Рис. 3 Схема установки для измерения электрического сопротивления раствора электролита. RМ и Rx – сопротивления магазина и ячейки; Г - источник переменного тока; О – осциллограф. |
В основе этой схемы лежит метод компенсации. Во избежание электролиза, влекущего за собой изменение концентрации электролита и поляризацию электродов, при компенсационном способе измерения сопротивления используется переменный ток высокой частоты. Форма и расположение электродов во всех измерениях должны быть постоянным. По экспериментально определенному сопротивлению исследуемого раствора рассчитывают значения удельной и молярной электрической проводимости электролитов.
Метод кондуктометрии используется для определения ряда физико-химических характеристик растворов электролитов.
1. Степень диссоциации слабых электролитов рассчитывается по уравнению
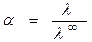 , (2.9)
, (2.9)
где 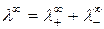 определяется по значениям предельной молярной электрической проводимости ионов
определяется по значениям предельной молярной электрической проводимости ионов
2. Константу диссоциации бинарного электролита можно рассчитать по уравнению (1.3):
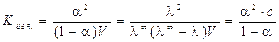 . (2.10)
. (2.10)
3. По данным кондуктометрии можно рассчитать pH раствора, образованного растворением электролита, при диссоциации которого образуются ионы водорода. Так, для бинарного электролита
pH = -lg aС. (2.11)
4. По данным кондуктометрии можно рассчитать растворимость (С) и произведение растворимости (Lр) малорастворимой соли:
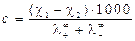 и
и 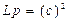 . (2.12)
. (2.12)
 2015-04-01
2015-04-01 2894
2894








