При одинаковых условиях объемы вступающих в реакцию газов относятся друг к другу и к объемам образующихся газообразных продуктов реакций как небольшие целые числа.
Эквивалент
Эквивалент (Э) – это реальная или условная частица вещества X, которая эквивалентна одному атому водорода или половине атома кислорода в данной ионообменной реакции или одному электрону в данной окислительно-восстановительной реакции.
Э(Х) = 1/z·Xz≥1,
где z - эквивалентное число или число эквивалентности.
Например: Э(NaOH) =1/1NaOH, Э(H2SO4) = 1/2H2SO4, Э(AlCl3) = 1/3AlCl3.
Фактор эквивалентности fэкв – это число, обозначающее, какая доля от реальной частицы эквивалентна одному иону водорода в данной кислотно-основной реакции или одному электрону в данной окислительно-восстановительной реакции. Это величина – обратная эквивалентному числу z:
fэквХ = 1/z, Э(Х) = fэквХ fэкв ≤ 1
Количество вещества эквивалентов – это отношение количества вещества к фактору эквивалентности:
n(fэквХ) = 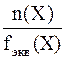 или n(fэквХ) = z∙n(Х)
или n(fэквХ) = z∙n(Х)
Единица измерения – моль.
 2015-04-01
2015-04-01 464
464








