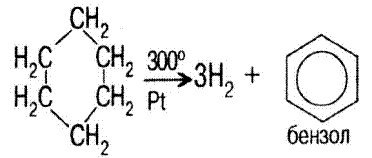СnH2n+2
| Углеводороды | метан CH4 этан С2Н6 пропан С3Н8 бутан С4Н10 пентан С5Н12 | гексан С6Н14 гептан С7Н16 октан С8Н18 нонан С9Н20 декан С10Н22 | Одновалентные радикалы | метил СН3- этил С2Н5- пропил С3Н7- бутил С4Н9- пентил С5Н11- (амил) | гексил С6Н13- гептил С7Н15- октил С8Н17- нонил С9Н19- децил С10Н21- |
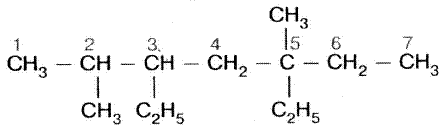
| Номенклатура: 1) выбрать самую длинную цепь; 2) пронумеровать атомы С в цепи; 3) определить радикалы и к какому по счету атому С они присоединены; 4) дать название цепи. |
1С – первичный, т.к. связан с одним С; 4,6С – вторичные, (с двумя С); 2,3С – третичные;
|
| Физические свойства: СН4 – газ без цвета и запаха, легче воздуха, нерастворим в воде. | С – С4 – газ, С5 – С15 – жидкость, С16 и больше твердое вещество |
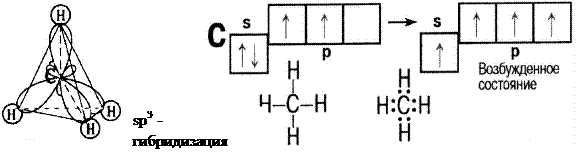
Строение СН4
| |||
| Химические свойства | |||
| Разрыв С-Н связи | Разрыв С-С связи | ||
1. Свободнорадикальное замещение С галогенами: CH4+Cl2=CH3Cl+HCl. CH3Cl – хлористый метил Механизм: Cl2 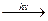 2Cl× CH4+Cl×→CH3×+HCl CH3×+Cl×→CH3Cl 2. Нитрование CH4+HNO3→CH3NO2+H2O. CH3NO2 – нитрометан 3. Дегидрогенизация(высок. t, катализатор) С4Н10→С4Н8+Н2. 3. Горение 1)СН4+2О2=СО2+2Н2О (голубое пламя); 2) СН4 2Cl× CH4+Cl×→CH3×+HCl CH3×+Cl×→CH3Cl 2. Нитрование CH4+HNO3→CH3NO2+H2O. CH3NO2 – нитрометан 3. Дегидрогенизация(высок. t, катализатор) С4Н10→С4Н8+Н2. 3. Горение 1)СН4+2О2=СО2+2Н2О (голубое пламя); 2) СН4 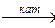 СН3ОН метиловый спирт; 3) СН4 СН3ОН метиловый спирт; 3) СН4 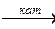 НСОН формальдегид НСОН формальдегид | Крекинг 1. Каталитический – в присутствии катализатора, при высоких t, p. Происходят реакции расщепления, изомеризации, дегидрирования, полимеризации. 2. Температурный – при высоких t (450-550˚C) и P. Молекула с большим числом атомов углерода расщепляется на молекулы с меньшим числом атомов: С4Н10→С2Н6+ С2Н4. | ||
| Получение: 1) CH3COONa+NaOH→Na2CO3+CH4; 2) Al4C3+12H2O→3CH4↑+4Al(OH)3; 3) C+2H2→CH4 (кат. Ni, t); 4) реакция Вюрца: C2H5 Br+2Na+Br C2H5→C2H5–C2H5 + 2 NaBr; 6) в технике: синтетический бензин nCO + (2n+1)H2→CnH2n+2+nH2O. (200˚С, кат., давл.) |
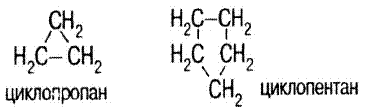
Циклоалканы СnH2n – предельные углеводы с замкнутой цепью.
| |||
| Химические свойства | |||
Химические свойства циклоалканов аналогичны химическим свойствам алканов. Циклоалканы относительно легче циклизуются при дегидрогенизации:
циклогексан |
 2015-04-01
2015-04-01 1201
1201