Одним из характерных процессов, протекающих при сварке плавлением, является окисление металла.
Под термином «окисление» в узком смысле понимают химическое взаимодействие того или иного элемента с кислородом.
Окисление металла в сварочной ванне происходит различными способами, если имеется одно или несколько из нижеперечисленных условий:
а) наличие в газовой фазе свободного кислорода (при сварке открытой дугой) или сложных газовых молекул (СО 2 и Н 2 О), способных при диссоциации выделять кислород;
б) присутствие на свариваемых кромках металла и присадочном металле окислов, способных при взаимодействии с жидким металлом окислять последний;
в) растворение в металле находящиеся в шлаке окислов;
г) использование для сварки химически активных шлаков, отдающих кислород металлу в результате обменных окислительно-восстановительных реакций с металлом сварочной ванны.
Характер окисления различных металлов при сварке может быть различным [4].
Некоторые металлы в жидком и твёрдом состоянии практически не растворяют кислород (Al, Mg, Zn и др.). Окисление этих металлов при сварке (в сварочной ванне) приводит к образованию обособлённой фазы – окислов, которые могут находиться либо в виде плёнки (поверхностной), либо в виде отдельных частиц во взвешенном состоянии.
Другие металлы (Fe, Cu, Ni, Ti) обладают способностью растворять кислород. При этом растворимость кислорода в жидкой фазе значительно больше, чем в твёрдой и увеличивается с повышением температуры. Окисление этих металлов сопровождается растворением в ванне жидкого металла образующихся окислов, если концентрация О 2 в ванне не достигает предела насыщения.
На практике приходится сваривать не чистые металлы, а сплавы, поэтому при наличии окислительных условий происходит окисление не только металлической основы, но и примесей.
Возможность окисления элемента определяется его сродством к кислороду при данной температуре, которое зависит от концентрации элемента и упругости диссоциации окислов в свободном состоянии.
Окисление металла может происходить следующими способами:
1. Окисление металла в сварочной ванне свободным кислородом газовой фазы. Если в газовой фазе имеется свободный (молекулярный) кислород, то последний может реагировать с металлом по реакции
nMe + O 2 = mMen/m O 2 /m .
Константа равновесия этой реакции выражается парциальным давлением кислорода, называемым упругостью диссоциации окисла:
KP = Po 2.
Значение упругости диссоциации окисла (т.е. равновесное парциальное давление кислорода для образования окисла), когда окисел и металл является конденсированными фазами и не находятся в растворе, позволяет определять действие газовой среды [6].
Упругость диссоциации окислов, находящихся в растворе 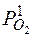 , отличается от упругости диссоциации свободных окислов Po 2:
, отличается от упругости диссоциации свободных окислов Po 2:
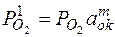 ,
,
где 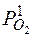 – упругость диссоциации окисла, растворенного в металле;
– упругость диссоциации окисла, растворенного в металле;
Po 2 – упругость диссоциации свободного окисла;
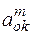 – степень насыщения металлического раствора окислом.
– степень насыщения металлического раствора окислом.
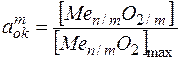 | – концентрация окисла в металле; |
| – концентрация насыщения. |
Так, для закиси железа, растворённой в жидком железе:
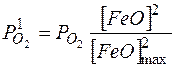 .
.
Для закиси железа концентрация насыщения определяется по уравнению
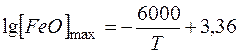 .
.
Упругость диссоциации закиси железа FeO в виде конденсированной фазы описывается уравнением
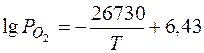 .
.
Можно рассчитать равновесное парциальное давление кислорода в газовой фазе при различных содержаниях закиси железа в жидком металле, например для электродов ЦМ-7.
Парциальное давление кислорода Ро 2 в металле, наплавленном электродами ЦМ-7, определяется как:
Т =2073 °К (1800 °С); 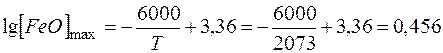 .
.
[ FeO ] = 0,0271 %; [ FeO] max = 2,86 %; 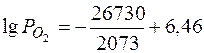 ат; Po 2 = 3,44×10-7 ат.
ат; Po 2 = 3,44×10-7 ат. 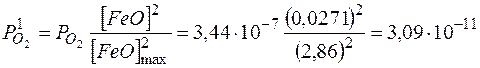 ат.
ат.
Для закиси железа концентрация насыщения определяется по уравнению
[ Po 2] >>> 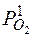 .
.
Если какой либо элемент растворён в металле, а его окисел нерастворим ни в металле, ни в шлаке (например, Mn и Si растворяются в металле, а окислы SiO 2, MnO нет), то константа равновесия реакции
m [ Me ] + 2[ O ] = (MemO 2 )
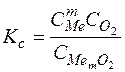 , а через парциальное давление Kc = Po 2.
, а через парциальное давление Kc = Po 2.
Поскольку окисел MemO 2 нерастворим в металле и шлаке, то его концентрацию, как величину постоянную, вводим в константу равновесия. Концентрацию кислорода Co 2 заменяем парциальным давлением кислорода 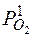 , необходимым для образования окисла, т.е. искомой упругостью диссоциации окисла.
, необходимым для образования окисла, т.е. искомой упругостью диссоциации окисла.
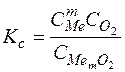 ;
; 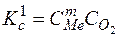 ;
; 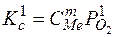 ;
; 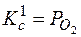 ;
; 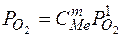 ;
; 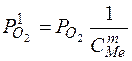 .
.
Таким образом, упругость диссоциации окислов растворённого элемента будет тем меньше, чем больше концентрация элемента в растворе, т.е. элемент будет окисляться тем легче, чем больше его концентрация.
Если окислы растворимого в металле элемента растворимы в металле или шлаке, то 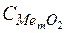 и
и 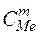 являются переменными и вводить их в константу нельзя:
являются переменными и вводить их в константу нельзя:
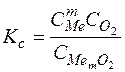 ;
; 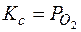 ;
; 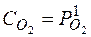 ;
; 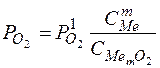 ;
; 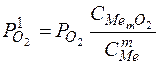 .
.
Отсюда следует, что упругость диссоциации окисла будет тем меньше, а окисление тем интенсивнее, чем больше концентрация элемента и чем меньше концентрация окислов этого элемента.
Обычно окислы раскислителей практически нерастворимы в металле (Fe), и переходят в шлак. Следовательно, употребляя какой либо раскислитель, необходимо, чтобы концентрация его окислов в шлаке была по возможности меньше и даже при возможности удалять окислы раскислителя из шпака.
В приложении к сварочной металлургии изложенное позволяет прийти к выводу о несовместимости раскислителя и его окисла в покрытиях электродов.
Если в состав покрытия или флюса введен какой-либо элемент в качестве раскислителя, то в качестве шлакообразующей фазы не следует использовать окисел того же элемента, так как это уменьшает силу действия раскислителя.
Если в состав покрытия введен элемент как легирующий, то одновременно следует ввести в покрытие и окисел этого элемента, чтобы предохранить от выгорания легирующий элемент.
2. Окисление сварочной ванны сложными газами. При наличии в газовой фазе сложных молекул, способных при диссоциации выделять кислород, также возможно окисление жидкого металла при сварке. Так, при высокой концентрации в газовой фазе CO 2 и H 2 O имеем
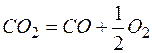 , , | 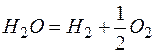 , , |
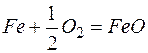 , , | 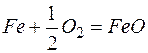 , , |
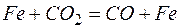 , , | 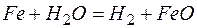 . . |
Образующаяся закись железа (FeO) растворяется частично в расплавленном металле, а частично в шлаке по константе распределения
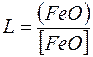 .
.
3. Окисление зоны плавления поверхностными окислами. Окисление сварочной ванны (зоны плавления) может происходить за счет окислов, находящихся на поверхности свариваемых кромок. К таким окислам относится окалина (Fe3O4) и ржавчина (Fe2O3).
Fe3O4 + Fe = 4 FeO; Fe2O3 + Fe = 3 FeO.
4. Окисление сварочной ванны шлаками, содержащими закись железа. Окисление металла окислами, находящимися в шлаке и растворяющимися в металле, происходит в связи с распределением таких окислов между шлаками и металлом по константе распределения (табл. 2)
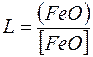 .
.
Таблица 2
Содержание FeO в шлаке в зависимости от содержания кислорода
в металле шва
| Содержание FeO в шлаке, % | 14,2 | 15,0 | 22,7 | 26,8 | 56,0 | 61,0 |
| Содержание кислорода в металле шва, % | 0,036 | 0,039 | 0,062 | 0,118 | 0,187 | 0,211 |
5. Окисление сварочной ванны химически активными шлаками. При электродуговой сварке сталей наличие в зоне сварки шлаков, содержащих окислы (например, SiO и MnO) в высокотемпературной части зоны плавления, делает возможным интенсивное окисление железа.
SiO 2 + 2 Fe = 2 FeO + Si; MnO + Fe = FeO + Mn.
В высокотемпературной части сварочной ванны эти реакции идут предпочтительно слева направо, так как:
а) при высоких температурах сродство к кислороду у всех элементов уменьшается и выравнивается;
б) высокая концентрация железа уменьшает упругость диссоциации, т.е. повышает сродство (силу) к кислороду железа.
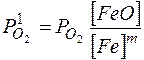 .
.
6.Окисление сварочной ванны при наличии в ней элементов-раскислителей. При наличии окислительных условий концентрация кислорода в сварочной ванне может быть значительно ограничена, если жидкий металл содержит элементы-раскислители, обладающие сродством к кислороду больше, чем металл-растворитель [2].
На рис. 5 представлены упругости диссоциаций окислов некоторых элементов в зависимости от их концентраций в сварочной ванне. Упругость диссоциации FeO приведены для сталей, когда концентрация FeO равна концентрации насыщения.
Анализ кривых показывает:
– раскислительное действие Al, Ti, Si, Mn наиболее эффективно в низкотемпературной части сварочной ванны;
– увеличение концентрации элемента-раскислителя в сварочной ванне уменьшает упругость диссоциации (увеличивает сродство к кислороду), что обеспечивает достаточно полное раскисление.
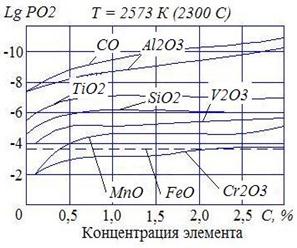 | 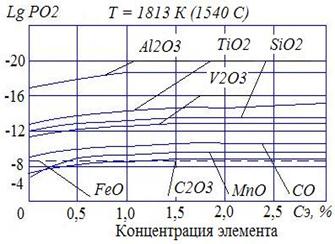 |
| Рис. 5. Упругость диссоциации окислов в зависимости от концентрации в сварочной ванне |
Однако введение элементов-раскислителей в сварочную ванну более 1,5...2,0 % не увеличивает эффективность раскисления, поэтому в состав покрытий электродов вводят не один раскислитель в большом количестве, а несколько в пределах 1,5...3,0 %.
При некоторых процессах сварки в результате взаимодействия жидкого металла с газовой фазой и шлаками наблюдается значительное увеличение содержания кислорода в металле шва по сравнению с его содержанием в основном металле и сварочной проволоке (табл. 3).
Таблица 3
Суммарное содержание кислорода в основном металле
и металле шва
| Материал | Суммарное содержание кислорода, % |
| Сталь (кипящая) Мст3 | 0,010...0,020 |
| Сталь (спокойная) Мст3 | 0,003...0,008 |
| Проволока Св-08 | 0,010...0,020 |
| Металл шва при газовой сварке (С 2 Н 2 +О 2) | 0,050...0,055 |
| УОНИ-13/45 | 0,020...0,030 |
| ОСЦ-45 (АН-348А) | 0,030...0,050 |
| ЦМ-7 | 0,080...0,090 |
| Меловое покрытие | 0,210...0,215 |
| Голый электрод | 0,250...0,280 |
Последствиями окисления являются:
– изменение механических свойств;
– возможность образования пор;
– засорение неметаллическими включениями;
– выгорание легирующих элементов.
 2015-04-01
2015-04-01 1695
1695








