Среди равновесных процессов, происходящих в термодинамических системах (газах), выделяют изопроцессы, при которых один из параметров состояния остается постоянным.
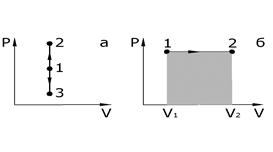
Изохорный процесс (V = const). В координатах P, V изохорный процесс изображается прямой параллельной оси ординат (рис. 6.3, а). В изохорном процессе газ не совершает работы, т. е. 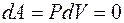 . Тогда из первого начала термодинамики количество теплоты выражается зависимостью вида:
. Тогда из первого начала термодинамики количество теплоты выражается зависимостью вида:
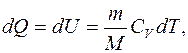
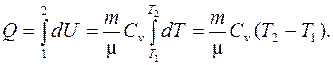 (6.21)
(6.21)
| Таким образом, в изохорном процессе все тепло, сообщенное газу, идет на увеличение его внутренней энергии. |
| Рис. 6.3 |
Изобарный процесс (P = const). Диаграмма этого процесса (изобара) изображается прямой параллельной оси x. Работа при расширении газа от V 1 до V 2 определяется как
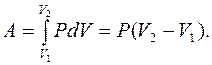 (6.22)
(6.22)
Работа численно равна площади заштрихованного прямоугольника на рис. 6.3, б. Если воспользоваться уравнением Менделеева – Клапейрона (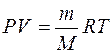 ), откуда следует, что
), откуда следует, что 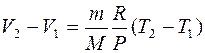 , то выражение (6.22) примет вид
, то выражение (6.22) примет вид
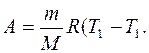 (6.23)
(6.23)
С учетом выражений параграфа 6.4 первое начало термодинамики для изобарного процесса в дифференциальной форме можно представить в виде
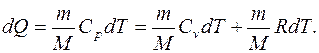 (6.24)
(6.24)
Изотермический процесс (T = const). Уравнением изотермического процесса является закон Бойля-Мариотта
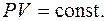 (6.25)
(6.25)
Диаграмма изотермического процесса приведена на рис.6.4.
Работа в изотермическом процессе (T = const) может быть определена как
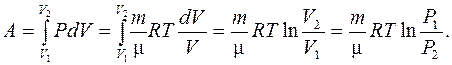 (6.26)
(6.26)
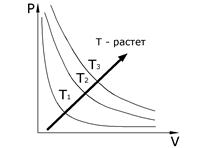 Рис. 6.4
Рис. 6.4
| Согласно первому началу термодинамики 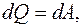 так как так как 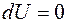 при при 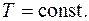 В изотермическом процессе все количество теплоты, сообщаемое газу, расходуется им на совершение работы против внешних сил
В изотермическом процессе все количество теплоты, сообщаемое газу, расходуется им на совершение работы против внешних сил
|
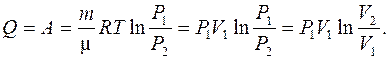 (6.27)
(6.27)
Теплоемкость изотермического процесса стремится к бесконечности, т. е.
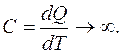 (6.28)
(6.28)
 2015-04-20
2015-04-20 438
438








